химия cәттілік жуз алдык(1) (копия). Химия фармацевтикалы пндер кафедрасы
 Скачать 1.78 Mb. Скачать 1.78 Mb.
|
|
*сутектік 21). Атомдардың ядро арасын қосатын түзу бойында электрон бұлттарының қаптасуынан түзілген молекулалық орбиталь * 22). Атомы sр2-гибридті түрде болатын молекуланың геометриялық пішіні *үшбұрыш 23). Валенттік бұрышы 109028/ болатын СН4 молекуласының гибридтену түрі *sp3 24). Қоршаған ортамен энергиясымен де, массасымен де алмасатын термодинамикалық жүйе *ашық 25). Изобаралық-изотермиялық жағдайдағы жүйенің энергия қорын сипаттайтын күй функциясы *энтальпия 26). Изобаралық-изотермиялық жағдайда химиялық реакция нәтижесінде бөлінетін немесе сіңірілетін жылу мөлшері *реакцияның жылу эффектісі 27). Қоршаған ортамен энергиясымен алмасатын, массасымен алмаспайатын термодинамикалық жүйе *жабық 28). Термодинамикалық жүйеде өтетін процестегі энтропиясы артатын реакция *2Н2O2 2H2O + O2 29). Изобаралық процестегі жылу эффектісін Qp есептейтін өрнек *Qp = ∆H 30). Термодинамикалық жүйеде өтетін процестегі энтропиясы өзгермейтін реакция *H2 + Сl2 2НСl 31). Иондар - бұл… *электрлік заряды бар біратомдық немесе көпатомдық бөлшектер 32). Диссоциацияны сипаттайтын және ерітінді концентрациясына тәуелді емес бірлік… *диссоциация константасы 33). К *судың иондық көбейткіші 34). Барий карбонатының тұз қышқылымен әрекеттесуін сипаттайтын қысқартылған иондық теңдеу: *BaCO3 + 2H+ = Ba2+ + CO2↑ +H2О 35). Барий хлориді қандай затпен алмасу реакциясына түседі *CuSO4 36). Көптеген тұздардың сулы ерітіндісі сілтілік немесе қышқылдық орта болуы мүмкін. Оның себебі … *тұздардың гидролизі 37). Қай зат суда толық гидролизденеді *Al2S3 38). Таза судың 250С температурадағы иондық көбейтіндісінің мәні: *10-14 39). Реакция ортасының қышқылдық жаққа ығысуы: *ацидоз 40). Молярлық концентрациясы 0,1 моль/л HCI ерітіндісінде: *pH = 1 41). СNaOH = 0,001моль/л ерітіндісінің рН-ы: *11 42). Химиялық реакцияның жылдамдығы – бұл: *уақыт бірлігінде әрекеттесуші заттардың концентрациясының өзгеруі 43). aA + bB ↔ dD+eE түріндегі жалпы кері реакцияға тепе-теңдік константасы К жазылады: * 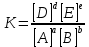 Тік жақшалар тепе-теңдік концентрациясын білдіреді; a,b,d,e – стехиометриялық коэффициенттер. 44). Химиялық реакция жылдамдығының әрекеттесуші заттардың концентрациясына тәуелділігін сандық түрде сипаттайды: *Вант-Гофф ережесі 45). w = k·c2 кинетикалық теңдеуге сәйкес келетін реакция реті: *екіншілік 46). Ферменттердің каталитикалық әсерінің ерекшелігі: *жоғары таңдамалылық әсері 47). Реакция жылдамдығына катализатордың әсері: *реакцияны активтендіру энергиясы төмен реакцияның бағытына бағыттайды 48). Бимолекулалық реакцияны көрсетіңіз *H2 + J2 2HJ 49). Жүйенің қысымын 5 есе арттырғанда СаСО3(т) = СаО(т) + CO2(г)тура реакцияның жылдамдығы: *өзгермейді 50).γ = (Kt + 10) / Кt теңдеуіндегі γ шамасы: *реакция жылдамдылығының температуралық коэффициенті 51). Химиялық реакцияның элементарлық актысына қатысатын молекулалар саны: *реакцияның молекулалығы 52). Қан плазмасына гипертонды болатын ерітінді *10,0 % NaCl-нің ерітіндісі 53). Гипотонды ерітіндідегі жасушаның ісініп, содан соң жарылу құбылысы *гемолиз 54). Қан тамырына егу үшін қолданатын ерітінді *изотонды 55). Вант-Гофф заңы бойынша ерітінді концентрациясы тәуелді *ерітіндінің осмостық қысымына 56). Ерітіндіде жоғары молекулалық қосылыстардың болуынан туындайтын осмостық қысымның бір бөлігі *онкотикалық қысым 57). Вант-Гофф заңы: 58). [Co(CN)4(H2O)2] – комплексті иондағы комплекстүзушінің тотығу дәрежесі *+3 59). Калий монобромопентанитроплатинат (IV) қосылысының формуласы *K2[Pt(NO2)5Br] 60). Нитрокомплексті қосылыс *K2 Na[Co(NO2)6] 61). Ацидокомплексті қосылыс *К3[Fe(СN)6] 62). [Co(NH3)5СI]CI2 комплексті қосылыстағы лиганда *[Co(NH3)5СI]2+. 63). Комплексті қосылыстағы орталық атом өзін қоршай орналасқан лигандалармен … құрайды *ішкі координациялық сфераны 64). Әрекеттесетін заттар құрамындағы элемент атомдарның тотығу дәрежесі өзгере жүретін реакцияларды ... деп атайды *тотығу-тотықсыздану 65). Берілгендерден диспропорциялық реакцияны таңдаңыз *6KOH + 3S = K2SO3+ 2K2S +3H2O 66). CrCI3 + H2O2 + NaOH→Na2CrO4 + H2O + NaCI реакциясындағы Н2О2 –тің көрсететін қасиеті *тотықтырғыш 67). Этиленнің калий перманганатымен бейтарап ортада тотығуынан түзілетін өнімдер *HOCH2CH2OH + MnO2↓+ KOH 68). Төменгі схема бойынша 2МеNO3 →600 M2O + 2NO2 + ½O2 қай элементтің нитраты ыдырайды *Li 69). Натрий ионын ашуға қолданатын калий дигидроантимонатынқосқанда қандай зат пайда болады *K2Na2SbO4 70). Калий иондары жалынды қай түске бояйды *күлгін 71). Қорғасын, барий тұздарымен уланғанда беретін және іш айдағыш глаубер тұзының формуласы *Na2SO4•10H2O 72). Калий хроматы барий- ионымен сары түсті кристалдық тұңба, ал аммоний сульфаты –ақ түсті түңба береді . Осы тұңбалардың формулалары *BaCrO4, BaSO4 73). Ca(OH)2ериді *HCl 74). Стенокардия ауруында тамырды кеңіту үшін натрийдің қай тұзын қолданады *NaNO3 75). Суда аз еритін және ортакүшті негіз қай элементтің гидроксиді *Mg 76). Сүйекте кальций иондарының сіңіруіне және шығуына әсер ететін дәрумен *Д 77). Қай металдың оксиді асқазан қышқылдығын төмендетеді,қышықлдармен уланғанда ем ретінде пайдаланады , тіс ұнтағының құрамына кіреді *MgO 78). Реакция орталығы сілтілік жаққа ығысуы аталады *алколоз 79). Сірке қышқылының ерітіндісінде сутек иондарының концентрациясының есептеуге болады формуламен  *[H+] = Ккты Скты 80). Кв = Сн+ . Сон- қалай аталады *судың иондық көбейтіндісі 81). Кобальт атомының электрондық конфигурациясы *…3d74s2 82). Магнитті теміртас минералының формуласы *Fe3O4 83). Сидерит минералының формуласы *FeCO3 84). Лимонит минералының формуласы *Fe2O3 ·nH2O 85). Темір пассивтенеді *H2SO4 конц 86). Темір концентрлі H2SO4 ерігенде түзіледі *Fe2(SO4)3 87). Темір (II) иондарын қанда ашуға қолданатын реагент K3[Fe(CN)6] 88) . “Берлин көгі”-нің формуласы *Fe4[Fe(CN)6]3 89). “Турнбуль көгі ”-нің формуласы *Fe3[Fe(CN)6]2 90) .Темір (II) қосылысының қайсысы ауаға тұрақты *(NH4)2SO4 •FeSO4 •6 H2O 91). Темір (III) хлориді ерітіндісінен H2S жібергенде түзіледі *Fe2S3 92). FeCl3 тұзының гидролизін үлғайту үшін қосады *NH4Cl 93). Ең күшті гидролизденетін тұз *NaFeO2 94). Fe2O3 калий карбонатымен балқытқанда түзіледі *KFeO2 95). Дезинфициялау және қан тоқтатқыш темір тұзы *FeCl3 • 6H2O 96). Витамина В12қай элементтің комплексі *Co 97). Кобальт (II)гидроксиді неде ерімейді *NaOH(cүйық) 98). Ең тұрақты комплексті ион
99). Малахит минералының формуласы *CuCO3·Cu(OH)2 100). Неде мыс ерімейді *NaOHразб 101). HNO3 (ω =65%) мыспен әрекеттескенде түзіледі *NO2 102). Күміс ауада қарайғанда қай зат түзіледі *Ag2O 103). Аммиактың артық мөлшерін CuSO4 қосқанда түзіледі *[Cu(NH3)4]SO4 104). Медицинада қолданатын антисептикалық және қуырғыш қасиеттері бар мыс тұзы * СuSO4 •5H2O 105). Ең тұрақты комплексті ион *+[Ag(S2O3)2]3- 106). Комплексті ионың [Cu(NH3)4]2+ кеңістіктегі пішіні *тетраэдр 107). Қышқылдық қасиеті бар гидроксид *Au(OH)3 108). Металдық хром әрекетеседі *HCl (суйық) 109). Натрийдің гексанитрокобальтаты (III) калий ионымен әрекеттескенде қандай тұңба түзіледі *K2Na[Co(NO2)6] 110). Аммоний оксалатын кальций тұзына қосқанда қандай түсті тұңба түзіледі *CaC2O4 111). Барий мен қорғасының тұздарымен уланғанда «глаубер тұзы» қолданылады, осы тұздың формуласы *Na2SO4·10H2O 112). Кальций хлоридін қабынуға, аллергияға және іссікке қарсы зат ретінде қолданады, оның қандай қасиетіне негізделген *капилляр қабығының өткізгіштігін реттейді 113). Судың тұрақты кермектілігін беретін тұздар *CaSO4, MgSO4 , MgCl2 , CaCl2 114). “+3” тотығу дәрежесі қай элементке тән *хром 115). Металдық хром немен әрекеттеседі *HCl сүйық 116). Қышқылдық қасиеті бар оксиді *CrO3 117). VIВ топ элементі қыздырғанда хлормен әрекеттесіп қандай қосылысты түзеді *СrСl3 118). СrCl3 пен (NH4)2S ерітінділері әрекеттескенде түзілетін қосылыс *Сr(OH)3 119). Реакция схема бойынша жұреді : К2Cr2O7 + (NH)2S + H2O Реакция нәтижесінде түзілетін хром қосылысы *Cr(OH)3 120). Таза марганецті оксидтерінен алу үшін қолданатын тотықсыздандырғыш *Si 121). Марганец қай қышқылда пассивтенеді *HNO3 (холод) 122). Марганец силициді *Mn2Si 123). Суда жақсы еритін марганец(ІІ) тұзы *MnSO4 124). KMnO4 қыздырғанда түзіледі * KMnO4 125). MnO2 мен K2CO3 пен KClO3 қоспаларын балқытқанда түзілетін марганец қосылысы *K2MnO4 126). Жасыл түсті марганц ионы *MnO42- 127). Тек тотықсыздандырғыш қасиеті бар марганец қосылысы *KMnO4 128). Сілтілік ортада KMnO4 тотықсызданғанда марганецтің тотығу дәрежесі *+6 129). Сутек тотықсыздандырғыш қасиетін көрсететін реакция *Н2+Сl2 130). Қай реакцияда су молекуласы тотықтырғыш қасиет көрсетеді *+NaH + H2O = NaOH + O2↑ 131). Түрлі микроорганизмдерден тазартқан су қалай аталады  *+апирогенді 132). Сутек пероксиді тотықсыздандырғыш қасиет көрсететін реакция *+KMnO4+H2O2+H2SO4 суйық→ 133). Ағзада сутек пероксидінің ыдырауын тездететін фермент *каталаза 134). Карбин мен графитте көміртек атомдары қандай жағдайда болады *+sp - гибридизация мен sp2- гибридизация 135). Кремнийдің толық еруі үшін ... қолдануға болады *+концентрлі азот және балқытқыш қышқылдарының қоспасын 136). Қыздырған кезде көміртек (II) оксиді көптеген металлдармен ұшқыш сұйықтық түзеді, олар аталады *+карбонил 137) Көміртек қышқылы – екінегізді; ол ... аталатын орта және қышқылды тұздар түзеді *+карбонат және гидрокарбонат 138). Көміртек қышқылының тұздарына сапалық реакциялар *+күшті қышқылдардың әсері 139). Карбонаттар ішінде суға еритін карбонат… *+сілтілік металдар мен аммоний 140). Сілтілік металдардың гидрокарбонаты қыздырған кезде *+карбонаттар, көмірқышқыл газы мен суға ыдырайды 141). Көміртек қышқылдарының ішіндегі практикалық маңызы зоры *сода 142). Кремний (IV)оксиді |
