овтетаввыф. коллоид было предложено
 Скачать 2.89 Mb. Скачать 2.89 Mb.
|
Парные вопросыКак называются зависимости, характеризующие адсорбцию? А = f(T), при Р = const; - С А = f(р), при Т = const; - А р = f(T), при А = const; - В А = f(Т), при С = const; - D А = f(С), при Т = const. - А изотерма; изостера; изобара; изопикна. За счет каких физических тел адсорбтив удерживается на поверхности адсорбента? Адсорбтив Адсорбент полярный полярный - В полярный неполярный - С неполярный полярный - С неполярный неполярный - А дисперсионных; ориентационных индукционных; водородных связей. Как называются представленные на рисунках различные зависимости, характеризующие процесс адсорбции? 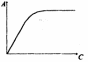 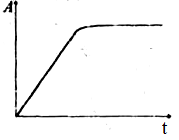 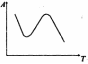  1. - B 2. - D 3. - A 4. - C  изобара адсорбции; изотерма мономолекулярной адсорбции; изотерма полимолекулярной адсорбции; кинетическая кривая адсорбции. Какими буквами обозначаются в уравнении полимолекулярной адсорбции (БЭТ) следующие величины? давление насыщенного пара при данной температуре; - В относительное давление пара; - С константа равновесия полимолекулярной адсорбции; - D максимальная адсорбция. - Е α; ps; p/ps; С; ничего из перечисленного. Какие участки изотермы мономолекулярной адсорбции описывают уравнения ………? Бедекера – Фрейдлиха; - С Ленгмюра; - D Генри. - А 1; 1 и 2; 2; 1, 2, 3. Охарактеризуйте понятия: интегральная теплота адсорбции; - В дифференциальная теплота адсорбции; - Е емкость поверхностного слоя; - А гиббсовская адсорбция; - С теплота смачивания; - F поверхностная концентрация. - D количество адсорбированного вещества, приходящееся на единицу массы адсорбента; общее количество тепла, выделившееся при адсорбции вещества, отнесенное к единице массы адсорбента; избыток числа молей адсорбтива в поверхностном слое по сравнению с его равновесной концентрацией в объемной фазе; количество адсорбированного вещества приходящегося на единицу поверхности адсорбента; тепло, выделившееся при дополнительной адсорбции малого количества адсорбтива; теплота, выделяющаяся при взаимодействии жидкости с поверхностью другой жидкости или твердого тела. Допишите ответТеория мономолекулярной адсорбции газа на поверхности твердых тел разработана Ленгмюром. Причиной адсорбции являются межмолекулярные силы, а причиной десорбции – тепловое движение молекул. Зависимость времени пребывания молекулы на поверхности адсорбента от температуры описывается уравнением Френкеля. ?? (возможно, Ленгмюр) Адсорбция, обусловленная действием вандерваальсовых сил межмолекулярного взаимодействия, называется физической адсорцией. Кинетика адсорбции подчиняется уравнению первого порядка. Лимитирующей стадией адсорбции является диффузия (либо энергетический барьер). Фаза, на которой происходит адсорбция, называется адсорбентом. Вещество, которое адсорбируется, называется адсорбатом или адсорбтивом. Условием протекания адсорбции как самопроизвольного процесса является уменьшение энергии Гиббса. Адсорбция газов или паров на твердом теле всегда является экзотермическим процессом и протекает с выделением тепла. Межмолекулярные силы, проявляющиеся между мгновенными диполями и возникающие при сближении молекул за счет флуктуаций электронной плотности, называются дисперсионными силами. Процесс выравнивания химических потенциалов компонентов между поверхностью и объемом, приводящий к изменению концентрации на поверхности называется адсорбцией. Хемосорбция всегда монослойна, т.к. хемосорбционный слой препятствует диффузии адсорбата. При значениях теплоты адсорбции в пределах 2,0 – 40 кДж/моль в системе протекает физическая адсорбция, при значениях 60–160 кДж/моль протекает химическая адсорбция. При адсорбции адсорбент находится в виде фазы, а адсорбат находится в молекулярно-дисперсном состоянии. Потенциальная теория Поляни описывает полимолекулярную адсорбцию. |
