оптика. Практикум Оптика и атомная физика
 Скачать 2.29 Mb. Скачать 2.29 Mb.
|
|
| Uа, В | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | 110 | 120 | 130 |
| Іа, мкА | | | | | | | | | | | | | |
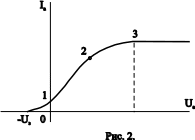
Постройте график зависимости силы фототока от анодного напряжения .
По графику построенной Вами ВАХ определите силу тока насыщения Ін.
По таблице 2 найдите соответствующий расстоянию световой поток Ф
По формуле γ=Ін/Ф мкА/лм определите интегральную чувствительность исследуемого фотоэлемента .
| Расстояние r от лампы до фотоэлемента, см | 30 | 31 | 32 | 33 | 34 | 35 | 36 |
| Интенсивность света, Вт/м2 | 450 | 425 | 400 | 375 | 350 | 325 | 300 |
| Световой поток, Ф, лм | 0,9 | 0,85 | 0,80 | 0,75 | 0,70 | 0,65 | 0,60 |
Проверка 1 закона фотоэффекта .
1. Установите анодное напряжения , соответствующее току насыщения
( U 100 В )
Изменяя расстояние между лампой r и фотоэлементом от 30 до 36 см. через 1 см. , снимите зависимость силы тока насыщения от интенсивности света . Постройте график этой зависимости и убедитесь , что ток насыщения , а следовательно и число вылетающих с поверхности катода за единицу времени электронов пропорциональна интенсивности света .
Контрольные вопросы .
Что называется фотоэффектом ? ( 3 вида ) .
Законы фотоэффекта и их объяснения на основе квантовой теории света .
Какой из законов и как проверяется в работе ?
Уравнения Эйнштейна для фотоэффекта и его анализа .
Что называется красной границей фотоэффекта ?
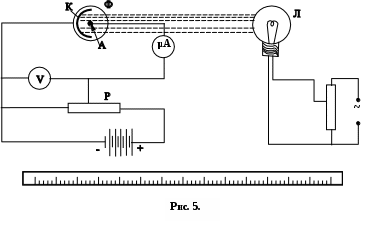
Фотоэлементы , их виды , устройство и принцип действия .
Что называется интегральной чувствительностью фотоэлемента .
Вольтамперная характеристика фотоэлемента , ее анализ .
Рабочая схема , выполнение работы .
Литература
1. И.В.Савельев Курс общей физики, т2.- М.: «Наука» 1978, С.34
2. Т.И.Трофимова Курс физики, М.: «Высшая школа», 2002г., С.376-381
3. Б.М.Яворский, А.А.Детлаф Курс физики, т.3. – М.: «Высшая школа», 1979г. С.216-225
Лабораторная работа № 3.10
Изучение сериальных закономерностей в спектре излучения
атомарного водорода и определение постоянной Ридберга .
На основании опыта по рассеянию - частиц , доказавших сложное строение атома , Резерфорд предложил планетарную модель атома , в которой принималось , что в центре атома находится положительно заряженное ядро , а вокруг него вращаются отрицательно заряженные электроны . Однако , модель атома Резерфорда противоречива . Действительно , движение электрона по орбите есть движение ускоренное . Но в этом случае согласно классической электродинамике, электрон непрерывно излучает электромагнитные волны , причем спектр излучения должен быть сплошным . Процесс излучения сопровождается потерей энергии электрона , при этом траектория его будет спиральной , и за время 10-8с электрон должен будет упасть на ядро . Такой вывод , полученный на основании классической физики , противоречит известной стабильности атомов и линейчатому характеру атомных спектров .
Выход из создавшегося тупика был найден в 1913 г. Н. Бором , правда , ценой введения предположений , противоречащих классическим представлениям . Допущения , сделанные Бором , содержатся в трех постулатах :
1 постулат ( постулат стационарности ) .
Электроны могут двигаться в атоме только по стационарным , определенным орбитам , находясь на которых они не излучают .
2 постулат ( постулат квантования ) .
Стационарной является орбита , находясь на которой электрон имеет квантованные значения момента импульса , удовлетворяющие условию :
где L - момент импульса электрона на орбите ,
m - масса электрона ,
υ- скорость электрона на n - ой орбите ,
r - радиус n - ой орбиты ,
n - главное квантовое число ( целое , не равное нулю число ,
означающее номер орбиты ) ,
h - постоянная Планка , h=6,625 10-34 Дж с
3 - постулат .
Атом излучает квант электромагнитной энергии , когда электрон переходит с орбиты большего на орбиту меньшего радиуса . При поглощении энергии происходит обратный переход : с орбиты меньшего на орбиту большего радиуса .
Энергия кванта h равна разности полных энергий электрона на орбитах до и после перехода :
где - частота кванта , n1 и n2 - значения главного квантового числа (номера орбиты) до и после перехода .
Рассмотрим механизм излучения атома водорода по Бору . Вокруг положительно заряженного ядра по круговым орбитам , разрешенным условием (1) , может вращаться электрон . Центростремительная сила , удерживающая его на орбите , по своей природе является кулоновской силой , поэтому можно записать :
Исключив скорость υ из уравнения (1) и (3) , можно рассчитать дискретные значения радиусов электронных орбит в атоме по формуле (4) , придавая главному квантовому числу значения n = 1,2,3,...
Т
 ак , для первой боровской орбиты в этом атоме водорода r1 = 0,53
ак , для первой боровской орбиты в этом атоме водорода r1 = 0,53 Из уравнения (3) следует , что
Подстановка (6) в уравнение (5) позволяет определить полную энергию электрона в виде
И , наконец , используя выражение (4) для радиусов боровских орбит , можно вычислить разрешенные значения энергий электрона в атоме
Подчеркнем следующее : т.к. полная энергия электрона в атоме отрицательна , то уменьшение ее абсолютного значения соответствует ее возрастанию . Энергия достигает максимального значения Е = 0 при n = .
Это соответствует тому , что электрон получил максимально возможную энергию и стал свободным , т.е. произошла ионизация атома .
Схема энергетических уровней для электрона в атоме водорода , рассчитанных по формуле (8) , приведена на рис.2 . При увеличении номера орбиты , т.е. по мере удаления электрона от ядра, увеличивается потенциальная энергия их взаимодействия , а значит уменьшается устойчивость системы ядро - электрон . Следовательно , из всех стационарных разрешенных орбит ближайшая к ядру (n=1) является наиболее устойчивой , поэтому такое состояние электрона называется основным , или нормальным . Электрон , находящийся на орбите с n > 1 , пребывает в возбужденном состоянии и по истечении времени τ10-8с переходит на одну из более близких к ядру орбит , испустив при этом квант электромагнитной энергии согласно уравнению (2). Энергии электрона на этих орбитах
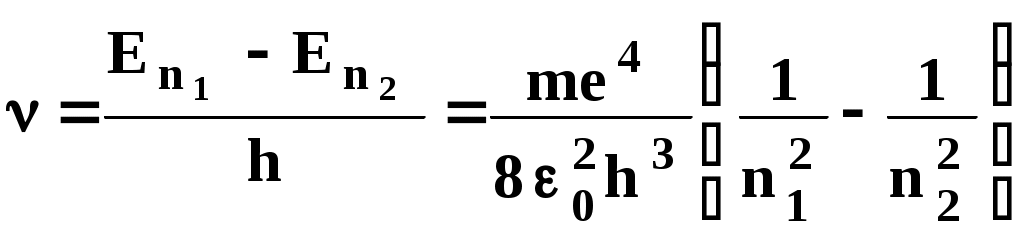 ( 9 )
( 9 )где n2 - номер орбиты , с которой совершался переход ,
n1 - номер орбиты , на которую совершался переход .
Выражение (9) есть обобщенная формула Бальмера - Ридберга , в которой
называется постоянной Ридберга .
Если , в соответствии с (9) , совершаются переходы на некоторую выделенную орбиту со всех более удаленных орбит , то говорят , что высвечивается серия линий .
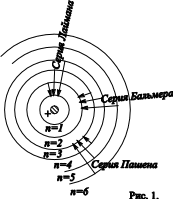
Для атома водорода опытно установлены несколько серий излучения (рис.1, 2):
n1 =1 , a n2 =2,3,4,... - серия Лаймана :
n1 =2 , a n2 =3,4,5,... - серия Бальмера :
n1 =3 , a n2 =4,5,6,... - Пашена : и т.д.
Поэтому формулу (9) называют еще сериальной формулой и записывают в виде :
Отметим , что лишь серию Бальмера можно наблюдать визуально , тогда как серия Лаймана находится в ультрафиолетовой , а серия Пашена и другие лежат в инфракрасной областях спектра .
К
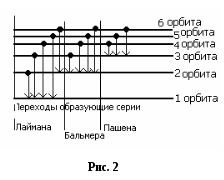 ак видно из рис.2, серия Бальмера , как и любая другая , состоит из бесчисленного множества линий . Однако , человеческий глаз способен различить три , реже - четыре линии , остальные лежат вне участка видимости (400 - 700 нм) В порядке возрастания частоты излучаемых квантов эти четыре характерные линии серии Бальмера следующие : H - ярко красная , H - зелено голубая , H - фиолетовая, H - слабо - фиолетовая (плохо различимая) . Таким образом, определив на опыте длины волн излучения линий серии Бальмера и учитывая
ак видно из рис.2, серия Бальмера , как и любая другая , состоит из бесчисленного множества линий . Однако , человеческий глаз способен различить три , реже - четыре линии , остальные лежат вне участка видимости (400 - 700 нм) В порядке возрастания частоты излучаемых квантов эти четыре характерные линии серии Бальмера следующие : H - ярко красная , H - зелено голубая , H - фиолетовая, H - слабо - фиолетовая (плохо различимая) . Таким образом, определив на опыте длины волн излучения линий серии Бальмера и учитывая где с - скорость света ,
можно определить постоянную Ридберга, воспользовавшись для расчетов формулой (11).
С другой стороны , постоянная R выражается через известные физические постоянные и может быть рассчитана по формуле (10) . Совпадение величин R , рассчитанных по формуле (10) и опытно определенных по формуле (11) , одно из самых точных в физике . Это является подтверждением правильности теории Бора для атома водорода . Однако эта теория имеет и существенные недостатки : она не применима для расчетов спектров атомов более сложных , чем водород ; она не пригодна для расчетов интенсивности сериальных линий ; теории свойственна внутренняя противоречивость , т.к. она носит полуклассический характер .
Последовательной теорией, объяснившей не только огромное многообразие явлений в микромире, но и вскрывшей физическую природу самих боровских постулатов, явилась квантовая механика.

 кое кольцо или сетка , помещенные в центре баллона .
кое кольцо или сетка , помещенные в центре баллона .