 348 348
V3
|
Термодинамиканың бірінші бастамасының {изотермдік, изохоралық
және изобаралық) процестерге қолданылуы
|
1
|
T= const dQ dA
|
0
|
Q dS pdVV=const
|
1
|
dQ dU V=const
|
0
|
Q dT pdV V=const
|
1
|
Q dU pdV P=const
|
0
|
dU= pdV - TdS V=const
|
349
V3
|
Қатты байланыстағы {біратомды, екіатомды, үшатомды} идеал газ
молекулаларының ішкі энергиясының дұрыс формулалары
|
1
|
U 3 mRT
2
|
0
|
U 7 mRT
2
|
1
|
U 5 mRT
2
|
1
|
U 3RT
|
0
|
U 5 mkT
2
|
0
|
U 3 mkT
2
|
350
V3
|
{Фик, Фурье, Ньютон} заңдарының математикалық жазылуы
|
1
|
Q kTSt
x
|
0
|
m D S
|
0
|
m D St
|
1
|
m D St
x
|
0
|
F
|
1
|
F S
x
|
351
V3
|
Диффузия D және тұтқырлық коэффициенттерінің өзара байланыстыратын дұрыс формулалар
|
1
|
= D
|
0
|
D =
|
1
|
DpM
RT
|
0
|
= D cv
|
0
|
D
|
1
|
D
|
352
V3
|
Газдардағы тұтқырлық және жылу сиымдылық
коэффициенттерінің өзара байланыстыратын дұрыс формулалар
|
1
|
= cv
|
0
|
= cv
|
0
|
= cv
|
1
|
iR
2 M
|
0
|
iR
2
|
1
|
;
cV
|
353
V3
|
Бір моль Ван-дер-Ваальс газының ішкі энергиясына арналған дұрыс
формула
|
1
|
U(V,T)=CvT - a/V
|
0
|
U(V,T)=CvT + a/V
|
1
|
U(V,T) iRT a
2 V
|
1
|
U(V,T) i a
2 AV
|
0
|
U(V,T)=CvT - aV
|
0
|
U(V,T)=CvT + a/V3
|
354
V3
|
Сенімді оқиғаның ықтималдылығы
|
1
|
P(A) = 1
|
0
|
P(A) 1
|
0
|
P(A) 1
|
1
|
P(A) =100%
|
1
|
сенімді оқиғаның ықтималдылығы бірге тең 1
|
0
|
сенімді оқиғаның ықтималдылығы 1 бірден үлкен
|
 355 355
V3
|
Идеал газдың тығыздығына арналған дұрыс формуласы (М-газдың молярлық массасы)
|
0
|
pV
RT
|
1
|
pM
RT
|
0
|
RT
pV
|
1
|
pMNAkT
|
1
|
pm0
kT
|
0
|
pm
kT
|

     356 356
V3
|
Өлшемсіз жылдамдық u /варқылы жазылған,жылдамдықтың
модуліне арналған Максвеллдің үлестірім заңының дұрыс формуласы
|
1
|
fu 4 u2eu2
|
0
|
fu 4 ueu2
|
0
|
fu 4 ueu2
|
0
|
fu 4 u2eu
|
1
|
4 2
fu eu
2

â
|
1
|
f 4 u2eu2
â
|
0
|
fu 4 u2eu
|
    357 357
V3
|
Барометрлік формуланың дұрыс өрнегі (m – ауа молекуласының
массасы, M – ауаның молярлық массасы)
|
1
|
p p0e kT
|
0
|
mgh
p p0eRT
|
0
|
p p0e RT
|
0
|
mh
p p0ekT
|
1
|
p p0 e RT
|
1
|
p mgh
e kT
p0
|
0
|
p mgh
ekT
p0
|
  358 358
V3
|
Газдардағы {изотермдік, изохоралық және изобаралық} процестерге
арналып жазылған термодинамиканың бірінші заңы
|
1
|
V
2
Q = =mRTln V1
|
1
|
Q = dU = mCdT
M v
|
0
|
Q = dU = mRT
M
|
0
|
Q = dU = mRTdT
M
|
1
|
Q = mCdT
M p
|
0
|
Q = = mRdT
M
|
0
|
Q = dU = mRT
M
|
359
V3
|
Газдардағы {изотермдік, изохоралық және адиабаталық} процестерге
|
|
арналып жазылған термодинамиканың бірінші заңы
|
1
|
Q = = mRTln V2
V1
|
1
|
mCdT
Q = dU = M v
|
0
|
Q = dU = mRTdT
M
|
1
|
= - dU = mCdT
M v
|
0
|
Q = dU = mRT
M
|
0
|
Q = dU = mRT
M
|
360
V3
|
Больцман үлестіріміне арналған дұрыс формула (Еп –сыртқы күш
өрісіндегі бір молекуланың потенциальдық энергиясы)
|
0
|
kT
n n0 e
En
|
0
|
n neEn
0
|
1
|
n n0ekT
|
0
|
n n0eRT
|
1
|
N N0 ekT
|
1
|
n n0e RT
|
0
|
En
N N0ekT
|
361
V3
|
Политроптық процестің көрсеткіш дәрежесінің n дұрыс өрнегі
|
1
|
C Cp
n
C CV
|
0
|
n C CV
C Cp
|
1
|
n C Cp
C C R
p
|
0
|
n C CV
C Cp
|
1
|
n C CV R
C CV
|
0
|
C Cp
n
C CV
|
0
|
n C CV R
C CV
|
362
V3
|
Газдардағы D - диффузия коэффициентінің дұрыс формуласы
|
0
|
D l
|
0
|
D 1
3
|
1
|
D 1 l
3
|
0
|
D 1 c
3 V
|
1
|
D 1 l 8kT
3 m0
|
1
|
D 1 1
3 2 d2n
|
0
|
D 1 1
3 2 d2n
|
   363 363
V3
|
Изобаралық процесс үшін дұрыс көрсетілген n политропа
көрсеткішінің мәні
|
1
|
p = const, n = 0
|
0
|
p = const, n =
|
1
|
dp = 0, n = 0
|
0
|
T = const, n = 0
|
0
|
V = const, n = 0
|
1
|
изобара, n = 0
|
0
|
dТ = 0, n = 0
|
   364 364
V3
|
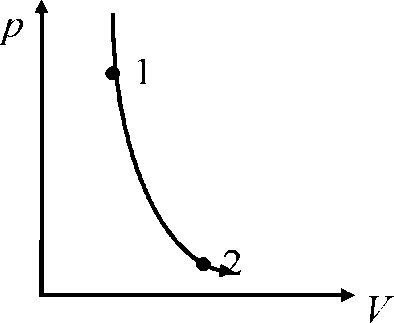
Адиабатада (суретті қараңыз) жүйенің 1-ші күйден 2-ші күйге өту процесі кескінделген, осы суретте температураның өзгерісі, ішкі энергия, жылу берілген немесе алынған және жұмыстың таңбасы дұрыс берілген
|
0
|
dT > 0, dU > 0, Q >.0, A > 0;
|
0
|
dT < 0, dU < 0, Q.< 0, A > 0;
|
1
|
dT < 0, dU < 0, Q.= 0, A > 0;
|
0
|
dT < 0, dU < 0, Q.= 0, A < 0;
|
1
|
dU < 0, dT < 0, Q.= 0, A > 0;
|
1
|
A > 0, dT < 0, dU < 0, Q.= 0;
|
0
|
dU > 0, dT > 0, Q >.0, A > 0.
|
365
V3
|
Молекулалардың < l > орташа еркін жүру жолына арналған дұрыс
формула ( - молекулалардың орташа жылдамдығы, < f >- молекулалардың 1 с уақыттағы орташа соқтығысу саны)
|
0
|
< l > = f
|
0
|
< l > = 2 f
|
0
|
2
< l > = f
|
1
|

< l > = f
|
0
|
l 1 8kT
f M
|
1
|
l 1 8kT
f m
|
1
|
l 1 8RT
f M
|
  366 366
V3
|
Молекулалардың < l > орташа еркін жүру жолына арналған дұрыс
формула
|
0
|
l 1 2 d2
|
0
|
l 1 2d2n
|
0
|
l 1
d2n
|
1
|
l 1 2d2n
|
0
|
l RT
2 d2 p
|
1
|
l kT
2 d2 p
|
1
|
l RT
2 d2 pN
A
|
    367 367
V3
|
Газдардың диффузия коэффициентіне D арналған дұрыс формулалар
|
0
|
D l
|
0
|
D 1
3
|
1
|
D 1 l
3
|
0
|
D 1 c
3 V
|
1
|
D 1 l 8kT
3 m0
|
1
|
D 1 1
3 2 d2 n
|
0
|
D 1 1
3 2 d2 n
|
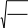   368 368
V3
|
Газдардың тұтқырлығына арналған дұрыс формулалар
|
0
|
1 l
3
|
1
|
1 l
3
|
0
|
1 l c
3 V
|
0
|
l
|
0
|
1
3
|
1
|
1 l pM
3 RT
|
1
|
1 l 8RT
3 M
|
0
|
1 l 8RT
3 M
|
 
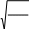 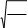 369 369
V3
|
Газдардың жылуөткізгіштігіне арналған дұрыс формула
|
0
|
1 l c
3 V
|
1
|
1 l c
3 V
|
0
|
l cV
|
0
|
1 l c
3 V
|
1
|
1 l pMc
3 RT V
|
0
|
1 iR
3 2M
|
1
|
1 l iR
3 2M
|
      370 370
V3
|
Қысым тұрақты p = const болған кездегі диффузия D коэффициентінің
температураға T тәуелділігінің дұрыс формуласы
|
0
|
D T
|
0
|
D не зависит от Т
|
1
|
3
D T2
|
0
|
1
D T
|
1
|
D T1,5
|
1
|
D T3
|
0
|
D T2
|
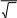 
   371 371
V3
|
Температура тұрақты T = const болған кездегі диффузия D
коэффициентінің қысымға р тәуелділігінің дұрыс формуласы
|
0
|
D p
|
1
|
1
D p
|
0
|
1
D p
|
0
|
D қысымға тәуелді емес
|
1
|
D p const
|
1
|
D p-1
|
0
|
D constp
|
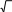 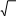 372 372
V3
|
Температура тұрақты T = const болған кездегі тұтқырлық
коэффициентінің және жылуөткішгіштік коэффициентінің қысымға р тәуелділігінің дұрыс формуласы
|
1
|
және қысымға тәуелді емес
|
0
|
p, p
|
0
|
p, p
|
0
|
1 1
p, p
|
1
|
жәнеқысым р өзгергенде өзгермейді
|
1
|
жәнеқысым р өзгергенде тұрақты
|
0
|
және қысымға сызықты тәуелді
|
373
V3
|
Бір моль { O2 , C02 , H2O} массасы
|
1
|
32 г
|
1
|
44 г
|
0
|
22,4 г
|
1
|
18 г.
|
0
|
18 кг
|
0
|
32 кг
|
0
|
16 г
|
 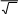 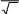 374 374
V3
|
Молекулалардың жылулық қозғалысының жылдамдық модуліне
арналған Максвелдің үлестірім заңының дұрыс формуласы
|
0
|
2 2
m
f 4 m 3 e 2kT 2

2kT
|
0
|
3 2
m
f 4 m 2 e2kT 2
2kT
|
0
|
3 2
m
f 4 m 2 e 2kT
2kT
|
1
|
3 2
m
f 4 m 2 e 2kT 2
2kT
|
0
|
3 2 2
m
f 4 M 2 e 2kT
2RT
|
1
|
3 2
m
f 4 M 2 e 2kT 2
2RT
|
1
|
3 2
M
f 4 m2 e 2 RT 2

2kT
| |
 Скачать 350.43 Kb.
Скачать 350.43 Kb. 348
348 355
355



 356
356


 357
357
 358
358

 363
363
 364
364
 366
366


 367
367

 368
368

 369
369




 370
370
 371
371
 372
372
 374
374



