1
|
p
RT
|
0
|
pm
NT
|
0
|
nm
kT
|
0
|
1
nm
|
0
|
nm
RT
|
93
V1
|
Идеал газда изотермдік процесте тұрақты болып қалады
|
1
|
энтальпия және энтропия
|
0
|
температура және қысым
|
0
|
қысым және көлем
|
0
|
көлем және тығыздық
|
0
|
тығыздық және масса
|
94
V1
|
Идеал газдың күй теңдеуі өзара байланыстырады
|
0
|
жылдамдық
|
0
|
тығыздық
|
1
|
қысым, теппература, көлем
|
0
|
орташа кинетикалық энергия
|
0
|
ішкі энергия
|
95
V1
|
Температураның дұрыс тұжырымдамасы
|
0
|
температура – дененің қыздырылу деңгейі
|
0
|
температура – дененің энергиясына пропорционал физикалық шама
|
0
|
температура - өзара молекулааралық әрекеттесудің потенциальдық
энергиясына тура пропорционал физикалық шама
|
0
|
температура – молекулалардың сыртқы күштер өрісіндегі потенциальдық
энергиясына тура пропорционал физикалық шама
|
1
|
температура – өте көп бөлшектерден тұратын жүйені сипаттайтын
статистикалық шама
|
96
V1
|
Идеал газдың күй теңдеуі (m – газ массасы, M – молярлық масса)
|
0
|
pV MRT
m
|
0
|
pV MRT
|
1
|
pV mRT
M
|
0
|
pV mRT
|
0
|
pV mT
M
|
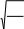 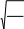 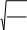
  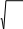  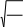  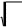 97 97
V1
|
Орташа квадраттық 2 жылдамдықтың дұрыс формуласы
|
0
|
2 2kT
m
|
0
|
2 3kT
m
|
0
|
2 8kT
m
|
1
|
2 3kNAT
M
|
0
|
2 2RT
M
|
   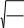 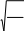 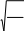 98 98
V1
|
Орташа арифметикалық жылдамдықтың дұрыс формуласы
|
0
|
3kT
m
|
1
|
8kT
m
|
0
|
2kT
m
|
0
|
8kT
m
|
0
|
2 kT
M
|
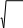 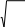 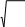 99 99
V1
|
Ең ықтималв.жылдамдықтың дұрыс формуласы
|
0
|
3kT
в m
|
0
|
8kT
в m
|
0
|
2kT
в m
|
0
|
8kT
в m
|
1
|
2kNA Tв M
|
  100 100
V1
|
Жылу мөлшеріне арналған дұрыс формулалар
|
0
|
Q cm
|
1
|
Q mr
|
0
|
Q T
|
0
|
Q rT
|
0
|
Q cT
|
101
V1
|
Изопроцестердегі ішкі энергияның өзгерісі
|
0
|
dU = RT
|
0
|
dU = 3RT
|
0
|
dU = kT
|
1
|
dU = dQ – dA
|
0
|
dU = – dQ
|
102
V1
|
Термодинамиканың бірінші бастамасының дұрыс формулалары
|
1
|
Q dU pdV
|
0
|
Q dS pdV
|
0
|
Q dU pdV
|
0
|
Q dT pdV
|
103
V1
|
Молярлық массасы М екі атомды газдың жылусиымдылығының
дұрыс формуласы, егер газдың тұтқырлығы белгілі болса
|
0
|
7 R
2 M
|
0
|
3 R
2 M
|
0
|
6 R
2 M
|
0
|
3 k
2 M
|
1
|
2,5 R
M
|
104
V1
|
Бір моль идеал газдың ішкі энергиясына арналған дұрыс формуласы
|
0
|
U 1 RT
2
|
0
|
U 3 nkT
2
|
0
|
U inkT
2
|
1
|
U m iRT, m M
M2
|
0
|
U 1 nkT
2
|
105
V1
|
СИ жүйесіндегі Универсал газ тұрақтыcының өлшем бірліктері
|
0
|
Дж/(К)
|
0
|
Дж/моль
|
0
|
ДжК
|
1
|
Дж/(мольК)
|
0
|
1/м3
|
106
V1
|
Жылу ағынының туындау себептері
|
0
|
жылдамдықтың біртексіз үлестірілімі
|
0
|
тұтқырлықтың біртексіз үлестірілімі
|
1
|
температураның біртексіз үлестірілімі
|
0
|
реттелген қозғалыс энергияларының біртексіз үлестірілімі
|
0
|
орта тығыздығының біртексіз үлестірілімі
|
107
V1
|
Көлемі V, p қысымы және температурасы T ыдыстағы молекулалар
саны
|
0
|
N kT
pV
|
0
|
N pVNAkT
|
1
|
N pV
kT
|
0
|
N RT
pV
|
0
|
N NApV
T
|
 108 108
V1
|
А оқиғасының P(A) ықтималдылығының өзгеру шектері
|
0
|
0 P(A) 1
|
1
|
0 P(A) 1
|
0
|
0 P(A) 1
|
0
|
0 P(A) = 1
|
0
|
А оқиғасының P(A) ықтималдылығы 1-ден үлкен
|
109
V1
|
Идеал газ изобарадан, изохорадан және изотермадан тұратын цикл жасайды, ал изотермдік процесс циклдың ең кіші температурасында жүреді. Циклдың қай бөлігінде газ жылу алынады (Q > 0) және қай бөлігінде жылу беріледі (Q < 0)
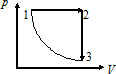
|
0
|
Q12 > 0, Q23> 0, Q31<0
|
0
|
Q12 < 0, Q23< 0, Q31>0
|
0
|
Q12 > 0, Q23< 0, Q31 =0
|
1
|
Q31 < 0, Q12 > 0, Q23 < 0
|
0
|
Q31 < 0, Q12 > 0, Q23 >0 .
|
 110 110
V1
|
Оттегі молекулаларының орташа квадраттық жылдамдығы 2 = 400 м/с болғандағы температура
|
0
|
411 К
|
0
|
104 К
|
1
|
205 К
|
0
|
309 К
|
0
|
(205-273) 0С
|
111
V1
|
Дұрыс формулаларды анықтаңыз
|
1
|
m 2 3
kT
2 2
|
0
|
m 2 3
RT
2 2
|
0
|
m 2 3
NA 2 2 kT
|
0
|
m 2 3
NA 2 2 kT
|
0
|
TEкин + Eпот
|
112
V1
|
Тұрақты көлемдегі (Не) гелийдің молярлық жылусиымдылығы
|
0
|
120 кДж/(моль∙ К)
|
0
|
2,5 Дж/(моль ∙ К)
|
0
|
1,2 кДж/(моль ∙ К)
|
0
|
12 Дж/(кмоль ∙ К)
|
1
|
12 Дж/(моль ∙ К)
|
113
V1
|
Изотермдікпроцескеберілген жылудың жұмсалуы
|
1
|
термодинамикалық жүйеге берілген жылу текжұмыс жасауға жұмсалады
|
0
|
термодинамикалық жүйе ішкі энергияның кемуі арқылы жұмыс жасайды
|
0
|
термодинамикалық жүйеге берілген жылу жүйенің массасын арттыруға
жұмсалады.
|
0
|
термодинамикалық жүйеге берілген жылу жүйенің моль санын
арттыруға жұмсалады.
|
0
|
термодинамикалық жүйеге берілген жылу жүйенің жылуын арттыруға
|
114
V1
|
Изобаралық процеске берілген жылудың жұмсалуы
|
1
|
термодинамикалық жүйеге берілген жылу ішкі энергияны арттыруға
және жұмыс жасауға жұмсалады
|
0
|
термодинамикалық жүйеге берілген жылу толық энергиясын арттыруға
жұмсалады.
|
0
|
термодинамикалық жүйеге берілген жылу жүйенің массасын арттыруға
жұмсалады.
|
0
|
термодинамикалық жүйеге берілген жылу тек жұмыс жасауға
жұмсалады
|
0
|
термодинамикалық жүйеге берілген жылу жүйенің жылуын арттыруға
жұмсалады
|
115
V1
|
Термодинамиканың аксиомалары
|
1
|
энергияның аддитивтілігі
|
0
|
температураның аддитивтілігі
|
0
|
термодинамикалық тепе-теңдік күйдің болмауы
|
0
|
термодинамиканың бірінші заңы
|
0
|
термодинамиканың үшінші заңы
|
116
V1
|
Дұрыс формулалар( - адиабата теңдеуіндегі дәреже көрсеткіші, i - молекулалардың еркіндік дәрежесінің саны) тізбегі
|
0
|
i
i 2
|
0
|
i 2 R
i
|
1
|
1 2
i
|
0
|
i Ri 2
|
0
|
i(i 2)
|
117
V1
|
Интенсивті параметрлерге жатады
|
0
|
ішкі энергия
|
0
|
көлем
|
0
|
жұмыс
|
0
|
энтальпия
|
1
|
концентрация
|
118
V1
|
Жылу мөлшері шамасының дұрыс анықтамасы
|
1
|
жылу мөлшері – процесс
|
0
|
жылу мөлшері - күй функциясы
|
0
|
жұмыс – күй функциясы
|
0
|
жылу мөлшері – процесс, ал ішкі энергия және жұмыс - күй функциясы
|
0
|
жылу мөлшері – күй функциясы, ал жұмыс - күй функциясы
|
0
|
ішкіэнергияжәнежұмыс - күйфункциясы
|
119
V1
|
Карно теоремасының дұрыс жазылған түрі (Т1 – қыздырғыштың
температурасы, Т2 – мұздатқыштың температурасы)
|
0
|
Q1 Q2 T1 T2
Q1 T1
|
0
|
Q1 Q2 T1 T2
Q1 T2
|
0
|
Q1 Q2 T1 T2
Q1 T2
|
1
|
Q- Q T- Tη= 1 2 ≤ 1 2
Q1 T1
|
0
|
η= A T1 + T2
≤
Q T1
|
0
|
Q Q2 Q1
|
 120 120
V1
|
Пайдалы әсер коэффициентінің жүйесіндегі өлшем бірлігі
|
1
|
ПӘК – пайызбен өлшенеді
|
0
|
ПӘК – моль арқылы өлшенеді
|
0
|
ПӘК – тің өлшем бірлігі L
|
0
|
ПӘК – джоуль арқылы өлшенеді
|
0
|
ПӘК – кельвин арқылы өлшенеді
|
0
|
ПӘК –Ньютон арқылы өлшенеді
|
 121 121
V1
|
Идеал газдың дұрыс анықтамасы
|
0
|
молекулалары материальдық нүкте ретінде және олар өзара
әрекеттеспейтін газ ал олардың арасындағы тебу күші арақашытыққа кері пропорционал
|
0
|
молекулалары материальдық нүкте ретінде және олар өзара әрекеттеспейтін газ ал олардың арасындағы тартылыс күші
арақашытыққа кері пропорционал
|
0
|
молекулалары абсолютті қатты шар ретінде ретінде және ал олардың
арасындағы тартылыс күші арақашытыққа тура пропорционал
|
1
|
молекулалардың өзіндік өлшемдері есепке алынбайды және молекулалардың өзара әрекеттесуінің потенциальдық энергиясы
есептелінбейді
|
0
|
молекулалары абсолютті қатты шар ретінде ретінде және ал олардың
арасындағы тебу күші арақашытыққа кері пропорционал
|
0
|
молекулалары материальдық нүкте ретінде және олар өзара әрекеттеспейтін газ ал олардың арасындағы тебу күші арақашытыққа
тура пропорционал
|
112
V1
|
Авагадро NA.тұрақтысының дұрыс сандық мәні
|
0
|
NA = 1023 моль-1
|
0
|
NA = 6,0210-23 моль-1
|
0
|
NA = 6,021015 моль-1
|
0
|
NA = 10 -15 моль-1
|
1
|
NA = 6,021026 кмоль-1
|
0
|
NA = 6,02×1026 кмоль
|
113
V1
|
Кез-келген масса үшін идеал газға арналған U ішкі энергияның дұрыс
формуласы (m – газдың массасы, M – молярлық масса)
|
0
|
U ikT
2
|
0
|
U mnkTM
|
0
|
U minkTM2
|
1
|
U miRT
M2
|
0
|
U iRT
2
|
114
V1
|
Бір моль идеал газға арналған дұрыс күй формулалары (m – газ
массасы, M – молярлық масса)
|
1
|
pV RT
|
0
|
pV mRT
|
0
|
pV MRT
|
0
|
pV nkT
|
0
|
pV NAT
|
0
|
p NkT
|
115
V1
|
Қысымға арналған дұрыс формула
|
0
|
p NkT
|
0
|
p nRT
|
0
|
p NRT
|
0
|
p nT
|
1
|
p NkT
V
|
0
|
pV NAT
|
 116 116
V1
|
Изохоралық процестің дұрыс формуласы
|
0
|
pV const
|
0
|
VT const
|
0
|
p constV
|
1
|
p constT
|
0
|
T constV
|
0
|
pT const
|
 117 117
V1
|
Изобаралық процестің дұрыс формуласы
|
0
|
pV const
|
0
|
pT const
|
0
|
V constp
|
1
|
V mR constT Mp
|
0
|
p constT
|
0
|
VT const
|
   118 118
V1
|
Изотермдік процестің дұрыс формуласы
|
0
|
VT const
|
0
|
V constp
|
0
|
V constT
|
1
|
pV mRT const
M
|
0
|
p constT
|
0
|
V mR constT Mp
|
 119 119
V1
|
Ықтималдылықтың дұрыс нормировкасы
|
0
|
n
Pi 0
i1
|
0
|
n
Pi 0
i1
|
1
|
n
Pi 1
i1
|
0
|
n
Pi 1
i1
|
0
|
n
Pi 1
i1
|
0
|
P(A) =100%
|
120
V1
|
Өзара бірін-бірі болдырмайтын А және В екі оқиға
ықтималдылықтарының дұрыс формуласы
|
0
|
PA B PA PB
|
0
|
PA B PB
PA
|
1
|
PA B PA PB
|
0
|
PA B PA PB
|
0
|
өзара бірін-бірі болдырмайтын А және В екі оқиға ықтималдылығы А
және В оқиғаларының ықтималдылықтарының айырымына тең
|
0
|
әртүрлі оқиғалар үшін әртүрлі жауаптар болуы мүмкін
|
121
V1
|
Жүйедегі флуктацияның рөлі туралы тұжырым
|
0
|
флуктуациялар қарастырылатын аймақтардың өсуіне байланысты
салыстырмалы түрде артады
|
0
|
флуктуациялардың салыстырмалы рөлі, олар қарастырылатын
аймақтардың өлшеміне тәуелді емес
|
0
|
әртүрлі оқиғалар үшін әртүрлі жауаптар болуы мүмкін
|
1
|
қарастырылатын аймақ кіші болған сайын флуктуацияның рөлі артады
|
0
|
жүйедегі флуктуацияның рөлі аймақтың өлшеміне тәуелді емес
|
0
|
өзара бірін-бірі болдырмайтын А және В екі оқиға ықтималдылығы А
және В оқиғаларының ықтималдылықтарының айырымына тең
|
122
V1
|
Термодинамиканың бірінші заңының дұрыс түрі
|
0
|
dU = Q+A
|
1
|
Q= dU+A
|
0
|
Q= dU-A
|
0
|
A = dU+Q
|
0
|
A = dU-Q
|
0
|
dS = dA×T
|
123
V1
|
Молекулалық физикада бірлік масса ретіндекөміртегі атомының 1/12
|
|
масасықолданылатын болса, бірлік массаның мөлшері
|
0
|
mu 1,66 107
кг
|
0
|
m1,66 107
u кг
|
1
|
mu 1,66 1027
кг
|
0
|
mu 1,66 1027 кг/моль
|
0
|
mu 6,02 1027г
|
0
|
m=6.02 кг
|
124
V1
|
Изотермдік процестегі алынған жылу мөлшері жұмсалады
|
0
|
жылуды өзгертуге
|
1
|
жұмыс істеуге
|
0
|
ішкі энергияның өзгерісіне
|
0
|
жүйенің құрылымын өзгертуге
|
0
|
изотермдік процесте жылу алу кезінде газ ұлғаяды және теріс жұмыс
жасайды
|
0
|
жылуды өзгертпеуге
|
125
V1
|
Адиабаталық процесс деп айтамыз
|
0
|
тұрақты жылудағы жүретін процесс
|
0
|
бұл процесс температура өзгермейтін кезде өтеді
|
0
|
бұл процесс ішкі энергия өзгермейтін кезде өтеді
|
0
|
қоршаған ортамен жылу алмасатын процесс
|
1
|
бұл процесс қоршаған ортамен жылу алмаспайды
|
0
|
бұл процесс қоршаған ортамен жылу алмасады
|
126
V1
|
Адиабатаныңтеңдеулері
|
1
|
PV = const
|
0
|
TP(-1) = const
|
0
|
VT(-1) = const
|
0
|
TV = const
|
0
|
PT V(-1) = const
|
0
|
=
|
127
V1
|
Қатты байланыстағы біратомды идеал газ молекуласының еркіндік
|
|
дәрежелер саны
|
0
|
і =7
|
0
|
і =9
|
0
|
і =8
|
0
|
і =4
|
1
|
і =3
|
0
|
i =10
| |
 Скачать 350.43 Kb.
Скачать 350.43 Kb.




 97
97


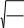
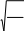
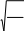 98
98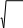
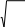
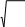 99
99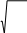
 100
100 108
108 110
110 120
120 121
121 116
116 117
117

 118
118 119
119
