Ответы на 2 семинар физиологии растений. 1. Роль пигментов в фотосинтезе пигментысборщики и пигментыловушки. Состав пигментных систем
 Скачать 43.97 Kb. Скачать 43.97 Kb.
|
|
1. Роль пигментов в фотосинтезе: пигменты-сборщики и пигменты-ловушки. Состав пигментных систем. Еще в 1932 г. Р. Эмерсон (США) разделил фотосинтетические пигменты на две группы: пигменты-сборщики и пигменты-ловушки. Пигменты-сборщики — это пигменты, поглощающие свет и передающие поглощенную энергию квантов пигменту-ловушке. Пигмент-ловушка — это пигмент, который, получив энергию, может потерять электрон. Большинство пигментов являются сборщиками; это вспомогательные пигменты. Пигментами-ловушками являются особые формы хлорофилла а, которые обозначаются как П 700 и П 680. Пигменты работают не изолированно друг от друга, а образуют две системы. В состав первой пигментной системы (ФС-I) входят пигменты-сборщики: хлорофиллы а и b (по 200 молекул), каротин (50 молекул) и 1 молекула пигмента-ловушки П700. В состав второй пигментной системы (ФС- II) тоже входят пигменты-сборщики квантов света: хлорофиллы а и b (по 200 молекул), 50 молекул ксантофиллов и 1 молекула пигмента-ловушки П680 Пигменты-сборщики передают поглощенную энергию с помощью резонанса пигменту-ловушке. Передача энергии происходит от каротиноидов к хлорофиллу и от одной молекулы хлорофилла к другой; от пигментов, поглощающих свет меньшей длины волны, к пигментам, поглощающим свет большей длины. Во время передачи часть энергии теряется в виде тепла. Для того чтобы энергия возбуждения молекулы одного пигмента могла передаться к молекуле другого пигмента, они должны располагаться в определенной последовательности и между ними должны быть очень маленькие расстояния — не более 10 нм; в действительности эти расстояния еще меньше — 0,5 нм. Это возможно благодаря связыванию молекул хлорофилла со специфическими белками и расположению пигментных систем в мембранах тилакоидов. Основные функций пигментов в фотосинтезе. (Пропускай, если останется время, напишем.) • Организация пигментов фотосинтетического аппарата в виде светособи рающих (антенных) комплексов, функционально сопряженных с реакцион ным центром, обеспечивает коллективное и эффективное поглощение энергии фотонов и передачу ее в реакционные центры, где энергия электронного возбуждения используется для фотохимических реакций. • Связь пигментов с белком определяет межмолекулярное расстояние меж ду ними (1,15 нм) и взаимную ориентацию молекул пигментов в светособира ющих (антенных) комплексах, что необходимо для эффективной миграции энергии в реакционные центры. • Стабильные условия микроокружения пигментов в белковой глобуле обес печивают создание устойчивых спектральных форм в ССК, в результате чего формируется широкий, сильно перекрывающийся спектр поглощения, необ ходимый для эффективного экситонного взаимодействия пигментов и направ ленной миграции энергии. • Образование связи пигментов с белками создает возможность участия бел ков в транспорте электронов в первичных процессах фотосинтеза, например, образование «электронной тропы» между QA и QB в электронтранспортной цепи хлоропластов, перенос энергии от тирозина (Tyrz) к П680. • Образование пигмент-белковых комплексов создает возможность регуля ции фотопоглощающей активности пигментов путем изменений конформации белков (в зависимости от pH, ионной силы, фосфорилирования белка) и изме нения ориентации пигментов по отношению к направлению светового луча. 2. Световая фаза фотосинтеза – это вызванный поглощением света транспорт электронов, в результате которого образуется АТФ, НАДФН2. Световая фаза представлена фотофизическим и фотохимическим этапами: Фотофизический – возбуждение молекул пигментов под действием света, передача энергии возбуждения реакционного центра. Например: Каротинхлорофилл bхлорофилл аП700реакционный центр 400-450 650 660-675 Это быстропротекающие процессы (10^-15 до 10^-9 секунд) Фотохимический этап – биохимические процессы, в ходе которых образуются НАДН, АТФ, происходит фотолиз воды. (происходит транспорт электронов) В дальнейшем будет происходить физиологическая фаза (образование органических веществ) в темновой фазе. Световая фаза происходит в фотосистемах (фотосистема состоит из светособирающего комплекса, реакционного центра и молекул-переносчиков). Выделают ФС1 и ФС2. В состав ФС1 входят: Пигментная система 1 (хлорофилл а и b, каротин, П700- реакционный центр), FeS-белок, ферредоксин, цитохромный комплекс b6f, пластоцианин, пластохинон. В этой системе первичный акцептор электронов а 695, вторичный – FeS-белок. В состав ФС2 – ПС2 (включает хлорофилл а и b, ксантофилл, П680), феофетин, пластохинон, цитохромный комплекс b6f, пластоцианин, S-комплекс, в котором происходит окисление воды, в состав входят Cl, Сa, Mn, Zn. В этой системе первичный акцептор феофетин. Пластохинон, цитохромный b6f-комплекс, пластоцианин – связующее звено между фотоситемами. 3. Циклический транспорт электронов и циклическое фотофосфорилирование. 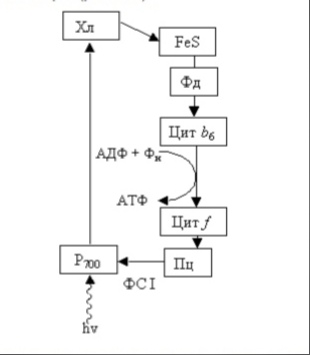 Схему смотреть на листе. Это на всякий случай Циклический транспорт электронов происходит в тилакоидах гран, его суть заключается в том, чтобы закачать протоны из стромы в люмен. Он состоит из одной фотосистемы. Циклическое фотофосфорилирование происходит при запуске процессов фотосинтеза при дневном свете. Смотреть уравнение на листе При циклическом фотофосфорилировании электроны возвращаются на Р700 по цепи переноса электронов. Так же как и при нециклическом фотофосфорилировании, энергия возбуждения электронов используется для синтеза АТФ. 4. Нециклический транспорт электронов и нециклическое фотофосфорилирование. Нециклический транспорт электронов начинается с работы первой фотосистемы, если не запустится первая фото система, то затем не запустится и вторая. Цикл с подписями на листе Чтобы П680 перешел в возбужденное состояние, к нему присоединяется электрон от воды. Электрон от молекулы воды образуется под воздействием света (фотоокисление или фотолиз). В результате молекула воды разрушается, образуя протоны и кислород: Уравнение на листе нециклическое фотофосфорилирование уравнение на листе В результате нециклического фотофосфорилирования образовались: молекулярный кислород, восстановленная форма HAДФ*Н2 5. Псевдоциклический транспорт электронов. Псевдоциклический поток электронов – перенос электронов от воды на кислород – реакция Мелера. Восстановление кислорода может происходить в обоих фотосистемах. При этом поглощение кислорода может компенсировать его выделение в ходе окисления Н2О. В результате единственным продуктом этого процесса будет АТФ, синтезируемая при псевдоциклическом фотофосфорилировании. Псевдоциклический поток электронов приводит к образованию активных форм кислорода, поэтому активация процесса может вызвать нарушение фотосинтетического аппарата. Этот альтернативный транспорт электронов активируется при высоких интенсивностях света в условиях дефицита в хлоропластах оксигенного НАДФ+. 6. Компоненты ЭТЦ хлоропластов (их природа, физико-химические свойства). ЭТЦ хлоропластов включает ряд переносчиков, общих для всех типов редокс-цепей живых организмов. К ним относятся цитохромы, железосерные белки, хиноны, флавиновые ферменты и пиридиннуклеотиды. Вместе с тем в ЭТЦ хлоропластов входят специфические переносчики электронов, такие как циклические тетрапирролы (хлорофиллы реакционных центров, феофитин), Mn-содержащий кластер, осуществляющий окисление воды, некоторые аминокислотные остатки белков (тирозин в ФСII) и медь-содержащий белок пластоцианин. Редокс-агенты ЭТЦ хлоропластов включены в состав трех интегральных мультипептидных комплексов, расположенных в мембранах тилакоидов – ФСI, ФСII и цитохромный b6f-комплекс. Кроме того, некоторые компоненты ЭТЦ свободно перемещаются по поверхности мембраны (пластоцианин, ферредоксин) или в ее толще (пластохиноны) и осуществляют связь между функциональными комплексами. Цитохромы в ЭТЦ хлоропластов представлены двумя цитохромами группы b (цитохром b559 и цитохром b563, или цитохром b6) и цитохромом группы с (цитохром f). Каждый из двух цитохромов группы b найден в хлоропластах в виде двух редокс-форм – низкопотенциальной (L) и высокопотенциальной (H). Цитохромы b6, а также цитохром f входят в состав цитохромного b6f-комплекса и участвуют в окисление пластохинолов и восстановлении пластоцианина, цитохром b559 связан с комплексом ФСII. Железосерные белки. В ЭТЦ хлоропластов входят 3 железосерных центра, содержащих [4Fe-4S]-кластеры, - Fx, FA и FB , и 2 белка с [2Fe-2S]-кластерами – ферредоксин (ФД) и центр Риске. Железосерные кластеры Fx, FA и FB и ферредоксин отличаются низкими окислительно-восстановительными потенциалами (от -0,7 В до –0,42 В). Они участвуют в восстановлении НАДФ+ в ФСI. Центр Риске имеет необычно высокий для железосерных белков окислительно-восстановительный потенциал (около +0,3 В). Он находится в цитохромном b6f-комплексе и осуществляет окисление пластохинолов. Хиноны. Представители двух групп хинонов – бензохиноны (пластохиноны) и нафтохиноны (филлохинон) включены в ЭТЦ фотосинтеза. Филлохинон (витамин К1) является переносчиком электронов на акцепторной стороне ФСI (А1), участвует в переносе электронов от первичного акцептора электронов (Ао) к железо-серному кластеру Fx. Имеет очень низкий окислительно-восстановительный потенциал (около –0,8 В). Пластохиноны осуществляют транспорт электронов на акцепторной стороне ФСII (QA и QB), а также между комплексом ФСII и цитохром b6f-комплексом в составе пула пластохинонов (PQ). Окислительно-восстановительный потенциал пластохинонов близок к нулю. Флавин-содержащие переносчики электронов ЭТЦ хлоропластов - ферредоксин-НАДФ-оксидоредуктаза (ФНР)–фермент, содержащий в качестве редокс-кофактора ФАД. Восстанавливает НАДФ+ в ФСI. Электроны для восстановления получает от восстановленного ферредоксина (ФД). Окислительновосстановительный потенциал – 0,36 В. Пластоцианин (Пц) – водорастворимый белок, содержащий 1 атом меди. Осуществляет перенос электронов по одноэлектронному типу, причем атом меди изменяет свою валентность (Cu+ Cu2+). Окислительно-восстановительный потенциал Пц равен +0,37 В. Пц восстанавливает окисленный пигмент РЦ ФСI П700+ и окисляет цитохром f цитохром b6f-комплекса хлоропластов. Марганецсодержащий кластер (Mn-кластер) располагается в комплексе ФСII и образует систему окисление воды (S). Кластер включает 4 атома марганца, валентность которых меняется в ходе индуцируемых светом окислительновосстановительных реакций. Окислительно-восстановительный потенциал максимально окисленного кластера около +0,9 В. Mn-кластер окисляет воду с образованием молекулярного кислорода. Электроны от Mn-кластера передаются на П680+ через промежуточный переносчик электронов (TyrZ) – остаток тирозина (Tyr161) белка D1 ФСII. Окислительно-восстановительные реакции идут с образованием нейтрального радикала тирозина. Тетрапиррольные переносчики электронов - уникальные компоненты ЭТЦ хлоропластов. Они являются первичными донорами и первичными акцепторами электронов в реакционных центрах ФСI и ФСII. Окислительно-восстановительные реакции циклических тетрапирролов сопровождаются образованием заряженных радикалов. 7. Механизмы транспорта электронов Основное невозбужденное состояние электрона в молекуле хлорофилла – синглетное. Возбужденное состояниеS*2 – квантов синего цвета, S*1 – красный. Переход S*1 – S*0 тепла и красной флюоресценции. Перенос энергии возбуждения между молекулой хлорофилла характеризуется высокой эффективностью и скоростью. Выделают экситонный и индуктивно – резонансный механизмы передачи возбуждения между пигментами. Экситонный перенос энергии – ненаправленный, блуждающий, происходит в системе идентичных молекул. Индуктивно – резонансный – направленный перенос энергии от коротковолновых форм пигмента к длинноволновым формам.ё Природа – молекула хлорофилла поглощает квант света синглетное возбужденное состояние, передает возбуждение соседней молекуле и переходит в основное состояние. В мультипепдидных комплексах наиболее вероятен резонансный механизм, когда перенос электрона от донора к акцептору предполагает резонансные взаимодействия редокс – центров с белковой молекулой, при которых возникает эффект туннелирования электрона через энергетический барьер. Скорость переноса электронов при этом определяется физическим контактом компонентов. Перенос электронов между комплексами предполагает миграцию подвижных низкомолекулярных переносчиков в мембране или по ее поверхности и осуществляется по диффузионному механизму. Диффузионные процессы – более медленные, чем резонансные, поэтому именно они являются скорость - лимитирующими в ЭТЦ 8. Синтез АТФ при фoтосинтетическом фосфорилировании. Хемиосмотическая теория. Строение АТФ-синтазы. Каталитический цикл фермента. Фотосинтетическое фосфорилирование – образование АТФ, сопряженное с электронным транспортом. Механизм фосфорилирования объясняет хемиосмотическая теория синтеза АТФ, разработанная Питером Митчеллом в 1961 г. Суть теории – по обе стороны мембраны создается разность химических потенциалов Н+ и возникает электрохимический мембранный потенциал. В люмене накапливается Н+ и включается работа АТФ-синтазы. АТФ-синтаза состоит из 2 комплексов: 1) водорастворимой, гидрофильной каталитической части, которая обращена к строме хлоропласта (СF1). 2) гидрофобной мембранной части, пронизывающей билипидный слой тилакоидов. Имеет протонный канал (CF0). Сущность теории Митчелла: · Фосфорилирование происходит на мембранах, которые непроницаемы для Н+ и имеют ЭТЦ. · Энергия, высвобождаемая при работе ЭТЦ, запасается в форме протонного градиента. · Обратный поток Н+ через протонный канал АТФ-синтазы сопровождается образованием энергии фосфатной связи АТФ. Три этапа синтеза АТФ: · Присоединение АДФ и Фн к активному центру фермента; · Конформационные изменения фермента, синтез АТФ из АДФ и Фн; · Высвобождение АТФ. Конформационные состояния каталитического центра делятся на 3 вида: О – открытое (open); Т – закрытое (tight); L – слабосвязанное, или неплотное (loose). Они различаются по степени сродства к АДФ, АТФ и Фн. Каталитический цикл АТФ-синтазы (по П. Бойеру, 1993): 1) Связывание АДФ и Фн в О-центре. 2) Поворот γ-субъединицы на 1200С переводит О-центр в Т-состояние. Здесь идут процессы синтеза и гидролиза АТФ. АТФ образуется без затраты энергии, но выйти из Т-центра не может. 3) Переход в состояние L-центра. Равновесие АДФ + Фн↔ АТФ сдвигается в сторону синтеза АТФ. АТФ может покинуть центр и перейти в водную фазу. 4) Следующий этап вращения приводит центр в исходное «открытое» О-состояние: О → Т → L → О |
