1. Взаимодействие света с веществом. Физические свойства обусловленные этим. Взаимодействие света
 Скачать 6.84 Mb. Скачать 6.84 Mb.
|
|
КАЛЬЦИТ — Са[СО3 ]. АРАГОНИТ — Са[СО3 ]. Назван по местности Арагония (Испания), где был впервые установлен. МАГНЕЗИТ—Mg[СО3 ]. Магнезия — область в Фессалии (Греция). Минерал известен с глубокой древности. Синоним: магнезиальный шпат. ДОЛОМИТ — CaMg[CO3 ]2 . СИДЕРИТ — Fe[СО3 ]. От греч. сидерос — железо. Синоним: железный шпат. РОДОХРОЗИТ — Mn[СО3 ]. От греч. родон — роза, хрос — цвет. Название указывает на цвет минерала. Синоним: марганцевый шпат. СТРОНЦИАНИТ — Sr[CO3 ]. Впервые был обнаружен близ местечка Строншиан (Западная Шотландия). ВИТЕРИТ — Ва[CO3 ]. ПАРИЗИТ(Ce) — Ca(Ce,La...)2 [CO3 ]3 F2 .  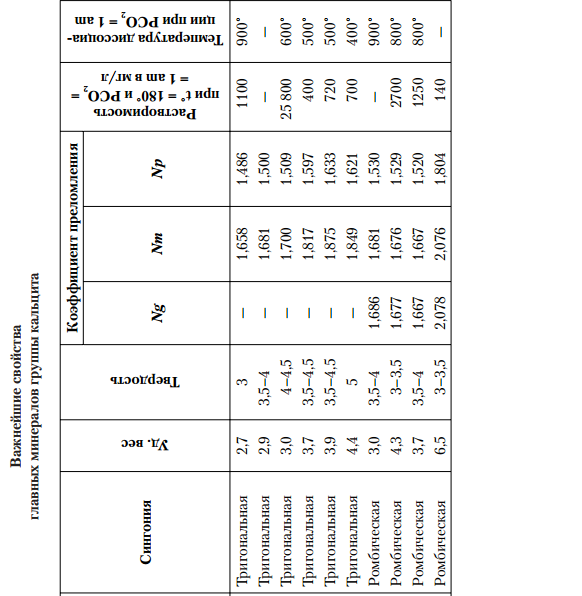 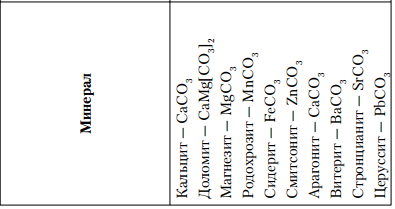 8.Оптические константы их зависимость от симметрии минералов. Падающий на минерал световой поток частью отбрасывается назад, причем частота колебаний не претерпевает изменений. Этот отраженный свет и создает впечатление блеска минерала. Интенсивность блеска, т. е. количество отраженного света тем больше, чем резче разница между скоростями света при переходе его в кристаллическую среду, т. е. чем больше показатель преломления минерала. Блеск почти не зависит от окраски минералов. Зная показатели преломления минералов, нетрудно вычислить показатель отражения света R по формуле Френеля: 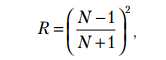 R — показатель отражения; N — средний показатель преломления минерала по отношению к воздуху. Подставляя в эту формулу ряд определенных значений N, легко изобразить графическим путем — в виде кривой — зависимость показателя отражения (блеска) от показателя преломления. Она имеет минимум N=1 ( почти показатель преломления воздуха) 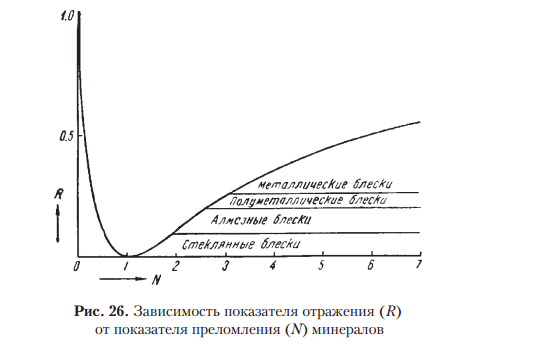 Градации интенсивности блеска: 1. Стеклянный блеск, свойственный минералам с N = 1,3–1,85. К ним относятся: лед (N = 1,309), криолит (N = 1,34–1,36), флюорит (N = 1,43), кварц (N = 1,544); далее следуют многочисленные галоидные соединения, карбонаты, сульфаты, силикаты и другие кислородные соли; заканчивается этот ряд такими минералами, как шпинель (N = 1,73), корунд (N = 1,77) и большинство гранатов (N до 1,85). 2. Алмазный блеск, характерный для минералов с N = 1,85–2,6. В качестве примеров сюда следует отнести: англезит (N = 1,87–1,89), циркон (N = 1,92–1,96), касситерит (N = 1,99–2,09), самородную серу с алмазным блеском на плоскостях граней (N = 2,04), сфалерит (N = 2,3–2,4), алмаз (N = 2,40–2,46), рутил (N = 2,62), часто обладающий полуметаллическим блеском, свойственным густо-окрашенным разностям. 3. Полуметаллический блеск прозрачных и полупрозрачных минералов с показателями преломления (для Liсвета) N = 2,6–3,0. Примеры: алабандин (N = 2,70), куприт (N = 2,85), киноварь (N = 2,91). 4. Металлический блеск минералов с показателями преломления выше 3. В порядке возрастающей отражательной способности приведем следующие примеры: гематит, пиролюзит (кристаллический), молибденит, антимонит, галенит, халькопирит, пирит, висмут и др Слева от минимального показателя, находятся (самородные) металлы: серебро (N = 0,18), золото (N = 0,36), медь (N = 0,64) и др. При определении отражательной способности непрозрачных минералов помимо показателей преломления нельзя не учитывать также коэффициента поглощения (K) данной среды. Для этих случаев показатель отражения (R) выражается следующей формулой 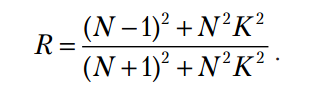 для непрозрачных минералов величины показателей отражения в действительности будут несколько выше, чем это определяется по формуле Френеля. Этим легко объясняются кажущиеся редкие исключения из приведенного выше положения. Например, магнетит обладает показателем преломления 2,42, т. е. должен был бы иметь алмазный блеск, однако благодаря непрозрачности, т. е. значительному поглощению света, показатель отражения несколько повысится, перейдя на диаграмме (см. рис. 26) в полосу полуметаллических блесков. 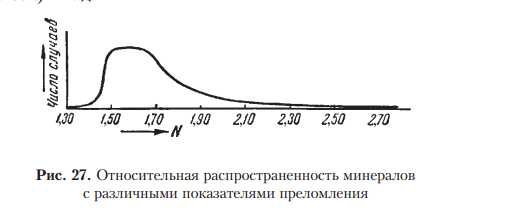 Большая часть минералов имеют показатель преломления, в диапазоне 1,5–1,7 ( 70%) Показатель преломления, как известно, в общем находится в зависимости от рефракции ионов, химического состава минералов, их удельного веса и от особенностей кристаллической структуры. У минералов обладающих одинаковой кристаллической структурой, показатель преломления и удельного веса, увеличивается при увеличение атомного веса катионов. Например, для MgO (уд. в. 3,64) N = 1,73, а для NiO (уд. в. 6,4) N = 2,23; Вхождение изоморфных примесей высоко-валентных ионов — Fe3+, Cr3+, Ti4+, V5+, тоже повышает показатель. В изоструктурных соединениях, например NaCl и КСl, увеличение размеров катиона (Na1+ 0,98 и К1+ 1,33) приводит к менее плотной упаковке размеров и даже к понижению N (для КСl —1,490, тогда как для NaCl — 1,544) Обратная картина для показателя преломления устанавливается в соединениях NaF и NaCl, где анион фтора (ат. вес 19,0) заменяется анионом хлора (ат. вес 35,5): для NaF N = 1,328, а для NaCl N = 1,544. По причине очень низкой рефракцией фтора. Второй важный фактор влияющий на отражение – это характер поверхности, от которой идет отражение. 1.Если минерал в изломе имеет не идеально гладкую, а скрытобугорчатую или ямчатую поверхность, то стеклянные, алмазные и другие блески приобретают чуть тусклый оттенок. Отраженный свет при этом частично теряет свою упорядоченность, подвергаясь некоторому рассеиванию. Создается жировой, или, как чаще говорят, жирный блеск. Наиболее типичными примерами жирного блеска могут служить блеск самородной серы в изломе или блеск элеолита (нефелина), подвергшегося едва заметному разложению. 2.Поверхности с более грубо выраженной неровностью обладают восковым блеском. Особенно это характерно для скрытокристаллических масс и твердых светлоокрашенных гелей. Таковы, например, часто встречающиеся блески кремней, колломорфных масс минералов группы галлуазита и др. 3.Если тонкодисперсные массывдобавок обладают тонкой пористостью, то в этом случае падающий свет полностью рассеивается в самых различных направлениях. 4.Микроскопические поры являются своего рода «ловушками» для света. Поверхности такого рода носят название матовых. Примерами могут служить: мел, каолин. 5.Для некоторых минералов, обладающих явно выраженной ориентировкой элементов строения в одном или двух измерениях в пространстве, наблюдается своеобразное явление, связанное с блеском, так называемый отлив минерала 6.В минералах с параллельноволокнистым строением (асбест, немалит, селенит и др.) мы всегда наблюдаем типичный шелковистый отлив. 7.Прозрачные минералы, обладающие слоистой кристаллической структурой и в связи с этим резко выраженной совершенной спайностью, имеют характерный перламутровый отлив (примеры: мусковит, пластинчатый гипс, тальк и др.).В том, что появление перламутрового отлива связано именно со слоистостью, легко убедиться, если сложить в пачку тонкие покровные или оконные стекла и взглянуть на них сверху. 9. Пегматиты. Процессы образования пегматитов протекают в верхних краевых частях магматических массивов и притом в тех случаях, когда эти массивы формируются на больших глубинах(несколько километров от поверхности Земли) в условиях высокого внешнего давления, способствующего удержанию в магме в растворенном состоянии летучих компонентов, реагирующих с ранее выкристал лизовавшейся породой. Пегматиты как геологические тела наблюдаются в виде жил или неправильной формы залежей, иногда штоков, характеризующихся необычайной крупнозернистостью минеральных агрегатов. Мощность жилообразных тел достигает нередко нескольких метров, а по простиранию они обычно прослеживаются на десятки, реже сотни метров. Пегматитовые образования наблюдаются среди интрузивных пород самого различного состава, начиная от ультраосновных и кончая кислыми. Однако наибольшим распространением. Пользуются пегматиты в кислых и щелочных породах. Пегматиты основных пород не имеют практического значения. По своему составу пегматиты немногим отличаются от материнских пород: главная масса их состоит из тех же породообразующих минералов. Лишь второстепенные (по количеству) минералы, да и то не во всех типах пегматитов, существенно отличаются по составу, так как содержат ценные редкие химические элементы В гранитных пегматитах в дополнение к главнейшим породообразующим минералам (полевые шпаты, кварц, слюды) наблюдаются фтороборсодержащие соединения (топаз, турмалины), минералы бериллия (берилл), лития (литиевые слюды), иногда редких земель, ниобия, тантала, олова, вольфрама и др. Во многих пегматитовых телахнаблюдается зональное строение и довольно закономерное распределение минералов. Например, в пегматитах Мурзинского района на Урале (рис. 53)внешние зоны у контакта с вмещающими гранитами сложены светлой тонкозернистой породой (аплитом). 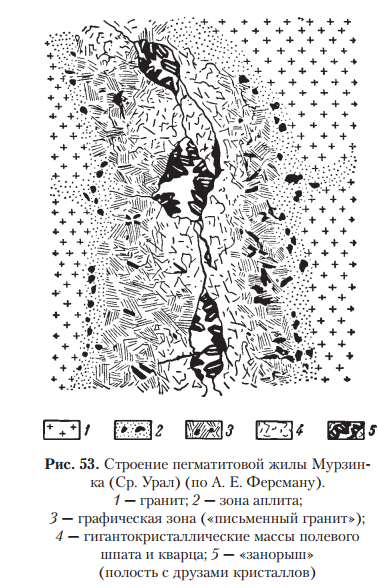 В тех случаях, когда пегматиты проникают во вмещающие интрузив породы, особенно богатые щелочными землями (MgO, CaO), их минеральный состав существенно отличается от состава пегматитов, залегающих в материнских породах. Происхождение пегматитов еще нельзя считать до конца разгаданным. А. Е. Ферсман рассматривал их как продукт кристаллизации остаточных расплавов, обогащенных летучими соединениями. Позже акад. А. Н. Заварицкий и его последователина основании физико-химических соображений допускали возможность образования крупнокристаллических масс путем перекристаллизации материнских пород под влиянием газов, накапливающихся в магматическом остатке, получающемся в процессе кристаллизации магмы. Однако в том и другом случаяхпегматиты образуются в конце собственно магматического процесса и занимают как бы промежуточное положение между глубинными магматическими породами и рудными гидротермальными месторождениями. 10. Принципы минералогической систематики.    11.Причины и способы минералообразования. Свободная кристаллизация, метасоматоз, перекристаллизация. Образование твердого кристаллического вещества может происходить различными путями: а) путем кристаллизации жидкостей (расплавов или растворов); б) путем отложения кристаллов на стенках пустот из газообразных продуктов возгона; в) путем замещения и перекристаллизации твердых масс (в частности, коллоидов). Главная масса природных кристаллических образований является результатом кристаллизации силикатных расплавов и водных растворов .Кристаллизация любого охлаждающегося расплава теоретически должна начинаться при определенной температуре, отвечающей температуре плавления данного вещества. Кристаллизация жидких фаз начинается при некотором переохлаждении или пресыщении. Зарождение кристаллов может бытьвынужденным (гетерогенная нуклеация), если в жидкости уже присутствуют обломки или пылинки каких либо твердых веществ, могущих по своим кристаллохимическим свойствам играть роль затравок, или самопроизвольным, наступающим в отсутствии затравки в пересыщенных или переохлажденных растворах и расплавах (гомогенная нуклеация). При самопроизвольной кристаллизации в разных точках расплава или раствора возникают так называемые центры кристаллизации, представленные кристаллическими зародышами. Вокруг этих центров кристаллизации в условиях свободного развития растут правильныекристаллики до тех пор, пока не создается стесненная обстановка для дальнейшего развития кристаллографических форм. ( 39 а,в) 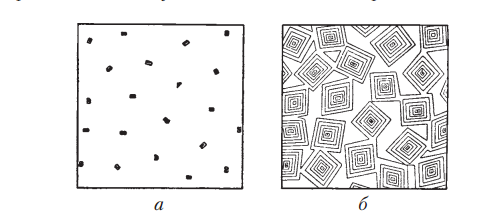 При продолжении кристаллизации начинается борьба за оставшееся пространство, и в конечном счете мы получим агрегат кристаллических зерен с неправильными внешними очертаниями (рис. 39в, г).  : чем сильнее переохлаждена или пересыщена жидкость, тем большее число центров кристаллизации возникает в дан ном объеме в единицу времени.  следовательно, тем меньшими размерами будут обладать кристаллические зерна в результате окончательного затвердевания жидкости. В случаях кристаллизации раствора в условиях очень резкого перенасыщения мы получим скрытокристаллические образования. Глубокое переохлаждение расплава приводит к образованию вулканических стекол. Согласно экспериментальным данным момент зарождения кристаллов в жидкости зависит от разных причин: от химической природы вещества; от примесей, ускоряющих или задерживающих появление кристаллических зародышей; от механических сил иногда действия звука. Однако скорость прироста различных граней кристалла в единицу времени часто бывает неодинакова, что в результате приводит к уменьшению числа граней. Установлено также, что на форму кристаллов оказывают значительное влияние растворенные примеси других веществ. Так, например, хлористый натрий обычно кристаллизуется в форме кубов, но из растворов, содержащих, кроме NaCl, также СаСl2 и MgSO4 , выделяется в виде октаэдров. При быстрой скорости роста, минералы будут неправильной формы. нарушается равномерный приток питающего раствора (например, в средах с увеличившейся вязкостью, в коллоидальных растворах и др.). В этих случаях наибольшее питание получают вершины и ребра растущих кристаллов, т. е. участки кристаллических структур, наименее насыщенные валентностью. Следует заметить, что кристаллы могут расти не только в жидких средах, т. е. за счет диффундирующих к кристаллу пересыщенных порций раствора, но также и в воздушной или газообразной среде при условии питания насыщенным раствором по капиллярным каналам. Наконец, образование кристаллов может происходить в газообразной среде и без питания жидким раствором, т. е. в случаях перехода вещества из парообразного состояния сразу в твердое при соответствующих температурах (ниже температуры плавления) и давлениях. Примером может служить образование снежинок в виде звездчатых кристаллов в воздухе или различных минералов как продуктов возгона в районах вулканической деятельности. |
