|
|
план урока. Атомное ядро-КСП 11 кл. 2. Цели, задачи Изучить определения понятий нейтрон, нуклон, массовое число
Атомное ядро. Нуклонная модель ядра. Изотопы. Энергия связи нуклонов в ядре.
(тема занятия)
.
2. Цели, задачи:
1. Изучить определения понятий «нейтрон», «нуклон», «массовое число», «энергия связи», «дефект масс», «удельная энергия связи», формулы для определения массового числа, энергии связи, дефекта масс, удельной энергии связи.
2. Развивать у учащихся умение пересказывать и анализировать учебный материал, выделять главное, основное; сравнивать, отвечать на вопросы, решать задачи.
3. Воспитывать коммуникативные умения: умение работать в коллективе и самостоятельно, умение говорить самому и слушать других.
2.1 Перечень профессиональных умений, которыми овладеют обучающиеся в процессе учебного занятия: научиться выполнять преобразования по расчёту физических величин.
2.2 Результаты обучения:
1) Знать структуру, свойства и взаимные превращения атомных ядер и другие явления, происходящие в микромире.
2.3 Критерии оценки:
1) Вычисляет энергию связи атомного ядра и объясняет графическую зависимость удельной энергии связи от массового числа ядра;
2) Использует законы сохранения массового и зарядового чисел при написании ядерных реакции.
3. Оснащение занятия
3.1 Учебно-методическое оснащение: дидактические материалы, справочно-инструктивные таблицы, карточки с заданиями, оценочные листы.
Справочная литература:
Б.Кронгарт, Д.Казахбаева, О.Иманбеков, Т.Қыстаубаев. Физика. Учебник. 1, 2 часть. Мектеп. 2019.
С.Туякбаев, Ш.Насохова, Б.Кронгарт, В.Кем , В.Загайнова . Физика. Учебник. Мектеп. 2015.
Н.Закирова, Р.Аширов. Физика. Учебник + СD. Арман-ПВ. 2019.
Н.Закирова, Р.Аширов. Физика. Дарслик. Арман-ПВ. 2019.
А.П.Рымкевич. Сборник задач по физике. Алматы. Мектеп. 2011.
3.2 Техническое оснащение, материалы, ИКТ: мультимедийный проектор, ноутбук, экран.
4. Ход занятия
Заплани-
рованные этапы урока, время
|
Деятельность, запланированная на уроке
|
Ресурсы
|
Начало урока
|
Орг. момент.
|
|
|
Проверка домашнего задания.
Фронтальный опрос.
Протон – стабильная элементарная частица, ядро атома водорода.
Нейтрон – элементарная частица, не имеющая заряда.
Протонно-нейтронная модель ядра Гейзенберга-Иваненко: ядро любого атома состоит из положительно-заряжённых протонов и электронейтральных нейтронов.
Массовое число – сумма числа протонов Z и числа нейтронов N в ядре.
Нуклоны – протоны и нейтроны в составе атомного ядра.
Изотопы – разновидность данного химического элемента, различающиеся по массе атомных ядер, т. е. числом нейтронов.
|
Презентация
|
Середина урока
|
https://docs.google.com/document/d/13AF0MtPCehJV05EmmSpYQOCuA8tsHEVaWBZfgtrfqbI/edit
Ядерные силы – это силы притяжения между нуклонами в ядре.
Дефект масс – разность масс нуклонов, составляющих ядро, и массы ядра
В 1919 году Резерфорд открыл протон при бомбардировке ядра атома азота α-частицами.
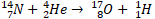
Это была первая ядерная реакция, проведённая человеком. Превращение одних атомных ядер в другие при взаимодействии их с элементарными частицами или друг с другом называют ядерной реакцией.
Протон – стабильная элементарная частица, ядро атома водорода. Свойства протона:
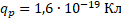
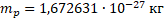
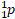 или или 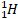 – символ протона. – символ протона.
Нейтрон был открыт в 1932 г. Д. Чедвиком при облучении бериллия α-частицами. Нейтрон - элементарная частица, не имеющая заряда. Свободный нейтрон, который находится вне атомного ядра, живёт 15 минут. Потом он превращается в протон, испуская электрон и нейтрино – безмассовую нейтральную частицу.
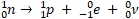
Свойства нейтрона:
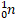 – символ нейтрона – символ нейтрона
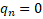
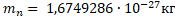
В 1932 году советский физик Д. Д. Иваненко и немецкий физик В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении ядра. Справедливость этой гипотезы была доказана экспериментально. Согласно этой модели ядра состоят из протонов и нейтронов. Так как атом не имеет заряда, т.е. электрически нейтрален, число протонов в ядре равно числу электронов в атомной оболочке. Значит, число протонов в ядре равно порядковому номеру химического элемента Z в периодической таблице Менделеева.
Сумму числа протонов Z и числа нейтронов N в ядре называют массовым числом и обозначают буквой А:
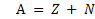
Ядерные частицы – протоны и нейтроны – называют нуклонами.
Радиус ядра находится по формуле:
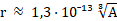
Изотопы – разновидность данного химического элемента, различающиеся по массе атомных ядер, т. е. числом нейтронов.
Устойчивость ядер зависит от отношения числа нейтронов к числу протонов.
Ядерные силы – это силы притяжения между нуклонами в ядре. Это самые мощные силы в природе, их ещё называют «богатырь с короткими рукавами». Они относятся к сильным взаимодействиям.
Свойства ядерных сил:
1) это силы притяжения;
2) примерно в 100 раз больше кулоновских сил;
3) зарядовая независимость;
4) короткодействующие, проявляются на расстояниях порядка 10-12 -10-13 см;
5) взаимодействуют с конечным числом нуклонов.
Масса любого атомного ядра всегда меньше, чем масса составляющих его частиц:
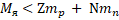
Дефект масс - разность масс нуклонов, составляющих ядро, и массы ядра:
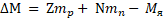
Энергия связи – это минимальная энергия, необходимая для полного расщепления ядра на отдельные частицы:
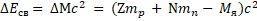
Удельная энергия связи – это полная энергия связи ядра, деленная на число нуклонов:
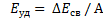
Дефект масс.
а.е.м. – это 1/12 часть изотопа углерода 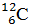 . .
Масса всего атома углерода составляет 12 а.е.м. Ядро состоит из 12 нуклонов, а каждый из них имеет массу большую, чем 1 а.е.м.:
mn 1,00866 а.е.м.
mp1,00728 а.е.м.
Если сложить массу всех нуклонов, которые содержатся в ядре:
6* mp+ 6* mn = 6*1,00728+6*1,00866 = 12,09546 > 12
Это связано с тем, что при объединении нуклонов в ядро, происходит выделение энергии. Это выделение энергии приводит к уменьшению общей массы. Так получается дефект масс (Δm).
Δm = Z* mp+(M-Z)* mn- mя
mя = mатома – Z* me, где me= 0,00055 а.е.м.
Δm = Z* mp+(M-Z)* mn- mатома + Z* me

Зная дефект масс, можно вычислить энергию связи атомного ядра:
Eсв = Δm*с2 [Дж]=931* Δm [МэВ]
с – скорость света
|
Презентация___Закрепление'>Ссылка 1.
Презентация
|
|
Закрепление:
Пример №1
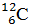 _ Z = 6, M – Z = 6 _ Z = 6, M – Z = 6
Δm = 6*1,00783+6*1,00866-12 = 0,09894 а.е.м.
Eсв = 931*0,09894 = 92,1 МэВ – столько энергии выделяется при образовании ядра атома углерода.
1[МэВ]=1,6 *10-13[Дж]
Удельная энергия связи – это энергия связи ядра, рассчитанная на 1 нуклон. Для разных ядер она имеет разные значения.
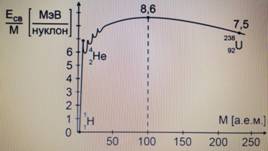
Два способа получения ядерной энергии:
1. Синтез легких ядер (осуществляется на Солнце).
2. Деление тяжелых ядер.
Примеры и разбор решения заданий
1. Заполните пропуски в таблице:
-
Химический элемент
|
Число
протонов
|
Число
нейтронов
|
Массовое число
|
Медь
|
|
35
|
64
|
Бор
|
5
|
|
11
|
Цинк
|
30
|
35
|
|
Решение:
Медь: N = 35, A = 64, Z = A – N, Z = 64 – 35 = 29;
Бор: Z = 5, A = 11, N = A – Z, N = 11 – 5 = 6;
Цинк: Z = 30, N = 35, A = Z + N, A = 30 + 35 = 65.
Ответ: медь: Z = 29; бор: N = 6; цинк: A = 65.
2. Соедините попарно элементы двух множеств:
Заряд частицы:
1) заряд протона;
2) заряд нейтрона;
3) заряд электрона.
Величина заряда:
1) 0;
2) 1,6 ∙ 10-19 Кл;
3) 2 ∙ 10-16 Кл;
4) - 1,6 ∙ 10-19 Кл.
Правильный вариант:
заряд протона = 1,6 ∙ 10-19 Кл;
заряд нейтрона = 0;
заряд электрона = - 1,6 ∙ 10-19 Кл.
|
Презентация
|
Конец урока
|
Рефлексия
Рефлексия «+, -, интересно».
- Понравился ли вам урок?
- Что было трудным для вас?
- Что вам больше понравилось?
|
Слайд
|
|
Домашнее задание:
Написать конспект.
Заполнить таблицу.
Подготовить сообщение на тему «Изотопы».
|
Слайд
|
5.Рефлексия по занятию
Рефлексия «+, -, интересно».
- Понравился ли вам урок?
- Что было трудным для вас?
- Что вам больше понравилось?
6. Домашнее задание
Оценочный лист:
№
|
Выполненное задание:
|
Баллы
|
|
Написать конспект.
|
30
|
|
Заполнить таблицу.
|
30
|
|
Подготовить сообщение на тему «Изотопы».
|
40
|
1. Заполните таблицу:
-
Химический элемент
|
Число
протонов
|
Число
нейтронов
|
Массовое число
|
Алюминий
|
|
|
|
Кремний
|
|
|
|
Железо
|
|
|
|
Фосфор
|
|
|
|
Вольфрам
|
|
|
|
|
|
|
 Скачать 127 Kb.
Скачать 127 Kb.

