Реферат Химия пищи алкалоиды. реферат химия пищи алкалоиды. Алкалоиды
 Скачать 1.97 Mb. Скачать 1.97 Mb.
|
|
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение Высшего профессионального образования Восточно-Сибирский государственный университет технологий и управления Кафедра «Технология продуктов общественного питания» Реферат на тему: «Алкалоиды» Выполнил: ст.гр.___ Поломошнова Е.В. Проверил: _____________________ г. Улан-Удэ 2017 Содержание:
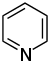
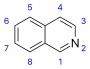
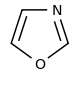
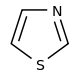
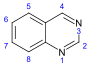
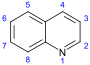
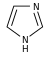
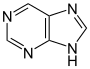
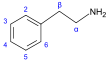
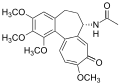
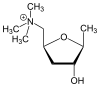
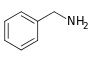
ХАРАКТЕРИСТИКА АЛКАЛОИДОВ Алкалоиды – группа азотсодержащих органических соединений природного происхождения (чаще всего растительного), преимущественно гетероциклических, большинство из которых обладает свойствами слабого основания; к ним также причисляются некоторые биогенетически связанные с основными алкалоидами нейтральные и даже слабокислотные соединения. Аминокислоты, нуклеотиды, аминосахара и их полимеры к алкалоидам не относятся. Иногда алкалоидами называются и синтетические соединения аналогичного строения. Помимо углерода, водорода и азота в молекулы алкалоидов могут входить атомы серы, реже – хлора, брома или фосфора. Многие алкалоиды обладают выраженной физиологической активностью. К алкалоидам относятся, например, такие вещества, как морфин, кофеин, кокаин, стрихнин, хинин и никотин. Многие алкалоиды в малых дозах оказывают лечебное действие, а в больших – ядовиты. Алкалоиды различны по своему физиологическому действию: одни из них угнетают или возбуждают нервную систему, другие парализуют нервные окончания, расширяют или сужают сосуды, третьи обладают обезболивающим действием и т. д. Граница между алкалоидами и другими азотсодержащими природными соединениями различными авторами проводится по-разному. Иногда считается, что природные соединения, содержащие азот в экзоциклической позиции (мескалин, серотонин, дофамин и др.), относятся к биогенным аминам, но не к алкалоидам. Другие же авторы, напротив, считают алкалоиды частным случаем аминов или причисляют биогенные амины к алкалоидам. ХИМИЧЕСКАЯ ФОРМУЛА, КЛАССИФИКАЦИЯ По сравнению с большинством других классов природных соединений, класс алкалоидов отличается большим структурным многообразием. Единой классификации алкалоидов не существует. Исторически первые классификации алкалоидов объединяли алкалоиды в группы по признаку происхождения из общего природного источника, например, из растений одного рода. Это было оправдано недостаточностью знаний о химическом строении алкалоидов. В настоящее время такая классификация считается во многом устаревшей. Более современные классификации используют объединение алкалоидов в классы по признаку сходства строений углеродного скелета (индольные, изохинолиновые, пиридиновые алкалоиды и т. п.) или по биогенетическим предшественникам (орнитин, лизин, тирозин, триптофан и т. п.). Однако при использовании таких схем приходится идти на компромиссы в пограничных случаях: так, никотин содержит как пиридиновое ядро, происходящее от никотиновой кислоты, так и пирролидиновое ядро от орнитина, и поэтому может быть отнесён к обоим классам. 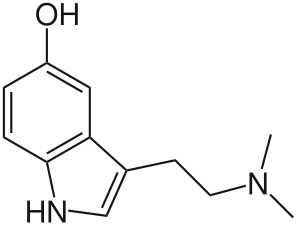 Буфотенин, яд жаб, содержит индольное ядро и синтезируется в живых организмах из аминокислоты триптофана 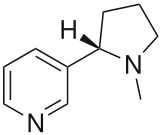 Молекула никотина включает в себя как пиридиновый цикл (слева), так и пирролидиновый (справа) Алкалоиды часто делят на следующие большие группы: Алкалоиды с атомом азота в гетероцикле, биогенетическими предшественниками которых являются аминокислоты. Называются также истинными алкалоидами. Примерами истинных алкалоидов являются атропин, никотин, морфин. К этой группе относят также некоторые алкалоиды, содержащие, кроме азотистых гетероциклов, терпеноидныефрагменты (как эвонин) или имеющие пептидную структуру (как эрготамин). Пиперидиновые алкалоиды кониин и коницеин часто относят также к этой группе, но их предшественники не являются аминокислотами. 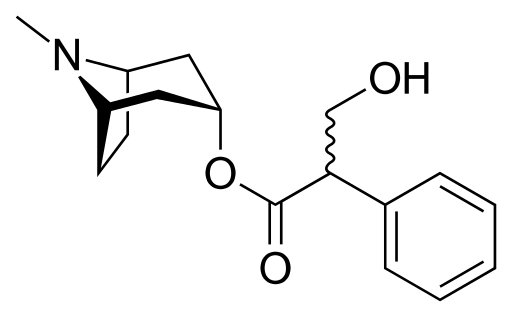 Атропин 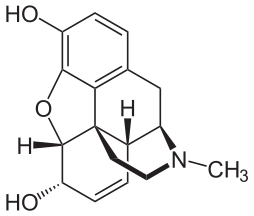 Морфин Алкалоиды с атомом азота в боковой цепи, биогенетическими предшественниками которых являются аминокислоты. Называются также протоалкалоидами. Примерами являются мескалин, адреналин и эфедрин. 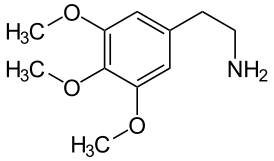 Мескалин 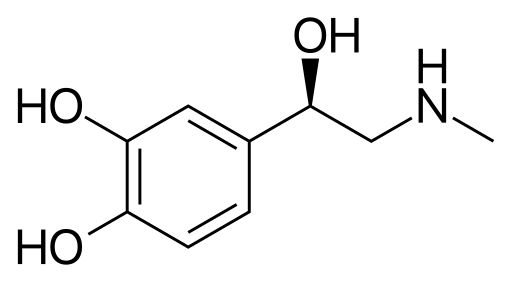 Адреналин Полиаминные алкалоиды (производные путресцина, спермидина и спермина). 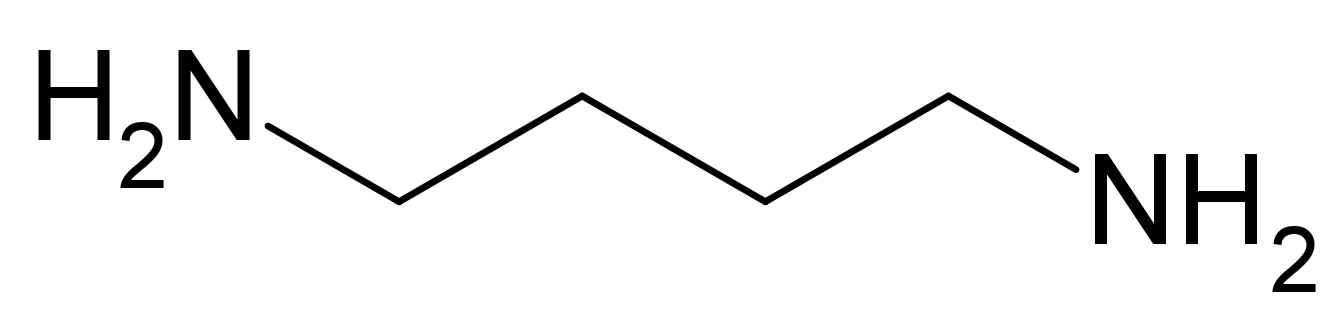 Путресцин 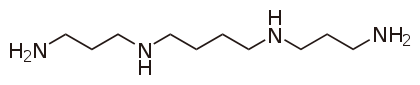 Спермин Пептидные (циклопептидные) алкалоиды. Содержат в молекуле остаток пептида, обычно циклический (поэтому часто их называют циклопептидными алкалоидами). К ним также относят алкалоиды, содержащие в молекуле гидроксистириламиновый фрагмент. 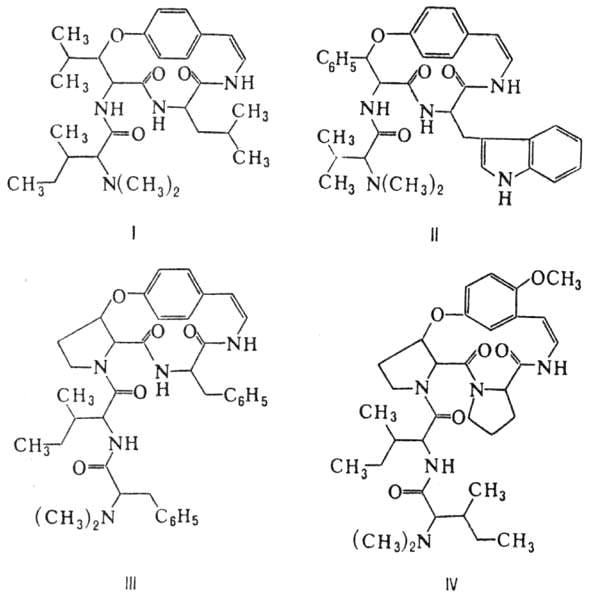 1 – франгуланин, 2 – интегеррин, 3 - амфибин-Б, зизифин-А Псевдоалкалоиды — соединения, похожие на алкалоиды, биогенетическими предшественниками которых не являются аминокислоты. К этой группе относятся, в первую очередь, терпеноидные и стероидныеалкалоиды. Пуриновые алкалоиды, такие как кофеин, теобромин и теофиллин, иногда относят к псевдоалкалоидам в связи со спецификой их биосинтеза. Некоторые авторы относят к псевдоалкалоидам такие соединения, как эфедрин и катинон, которые, хотя и происходят от аминокислоты фенилаланина, но атом азота приобретают не от неё, а в результате реакции трансаминации. 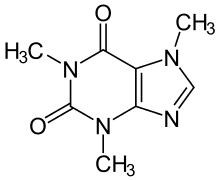 Кофеин 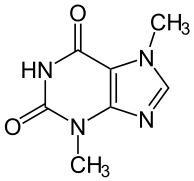 Теобромин Некоторые соединения, относимые по аналогии к тому или иному структурному классу, не имеют соответствующего элемента углеродного скелета. Так, галантамин и гомоапорфины не содержат изохинолинового ядра, но обычно относятся к изохинолиновым алкалоидам. 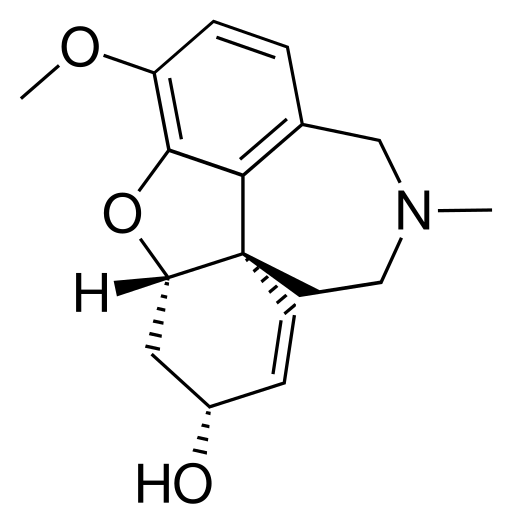 Галантамин Основные классы мономерных алкалоидов перечислены в следующей таблице:
СВОЙСТВА АЛКАЛОИДОВ Алкалоиды, молекулы которых содержат атомы кислорода (что справедливо для подавляющего большинства алкалоидов) при стандартных условиях, как правило, представляют собой бесцветные кристаллы. Алкалоиды, молекулы которых не содержат атомов кислорода, чаще всего являются летучими бесцветными маслянистыми жидкостями (как никотин или кониин). Некоторые алкалоиды не являются бесцветными: так, берберин жёлтый, сангвинарин оранжевый. Большинство алкалоидов обладает свойствами слабых оснований, но некоторые из них амфотерны (как теобромин и теофиллин). Как правило, алкалоиды плохо растворимы в воде, но хорошо растворимы во многих органических растворителях (диэтиловом эфире, хлороформе и 1,2-дихлорэтане). Исключением является, например, кофеин, хорошо растворимый в кипящей воде. При взаимодействии с кислотами алкалоиды образуют соли различной степени прочности. Соли алкалоидов, как правило, хорошо растворимы в воде и спиртах и плохо растворимы в большинстве органических растворителей, хотя известны соли, плохо растворимые в воде (сульфат хинина) и хорошо растворимые в органических растворителях (гидробромид скополамина). Большинство алкалоидов имеет горький вкус. Предполагается, что таким образом естественный отбор защитил животных от вырабатываемых растениями алкалоидов, многие из которых сильно ядовиты. ФИЗИОЛОГИЧЕСКИЕ СВОЙСТВА Большинство алкалоидов действует на нервную систему: в малых дозах они оказывают возбуждающее действие, а в больших дозах – угнетающее. Так, например, кокаин, широко употребляемый в медицине в качестве местного обезболивающего средства, действует на чувствительные окончания периферической нервной системы. Кураре – алкалоид, содержащийся в соке некоторых южноамериканских растений, действует на двигательные окончания нервной системы и поэтому вызывает паралич; именно поэтому он употреблялся индейцами для смачивания стрел. Содержащийся в млечном соке мака морфин действует на цeнтральную нервную систему, вызывая сон; он употребляется в медицине в качестве общего обезболивающего средства. Содержащийся в табаке никотин также действует на центральную и периферическую нервную систему. В ягодах белладонны и дурмана содержится атропин, который оказывает сильное действие на моторные нервы глаза, расширяя зрачок. ПРИРОДНЫЕ ИСТОЧНИКИ Алкалоиды синтезируются различными живыми организмами. Наиболее широко они распространены в высших растениях: по имеющимся оценкам, от 10 до 25 % видов высших растений содержат алкалоиды. Характерно, что в прошлом термин «алкалоид» чаще всего применялся только по отношению к веществам растительного происхождения. К важнейшим растениям-алкалоидоносам, получившим промышленное применение, относятся опийный мак, хинное дерево, табак, белладонна, скополия, анабазис, какао, кокаиновый куст, пилокарпус, хвойник, чилибуха, крестовник, чайный куст. Содержание алкалоидов в растениях, как правило, не превышает нескольких процентов. Обычно концентрация невелика и составляет сотые и десятые доли процента. При содержании 1-3 % растение считается богатым алкалоидами (высокоалкалоидоносным). Только немногие растения, например, культивируемые формы хинного дерева, содержат до 15-20 % алкалоидов. Особенно богаты алкалоидами растения таких семейств, как Маковые, Паслёновые, Бобовые, Кутровые, Мареновые, Лютиковые, Логаниевые. В водорослях, грибах, мхах, папоротниках и голосеменных они встречаются сравнительно редко. В большинстве растений распределение алкалоидов по тканям неравномерно. В зависимости от вида растения максимальное содержание алкалоидов может достигаться в листьях (белена чёрная), плодах или семенах (чилибуха), корнях (раувольфия змеиная) или коре (хинное дерево). В растениях алкалоиды находятся в виде солей органических и неорганических кислот в активно растущих тканях, эпидермальных и гиподермальных клетках, в обкладках сосудистых пучков и латексных ходах. Они растворены в клеточном соке. Кроме того, в разных тканях одного и того же растения могут содержаться разные алкалоиды, например, катарантус розовый содержит более 60 алкалоидов, в млечном соке мака содержится до 22 алкалоидов; по нескольку алкалоидов содержится в коре хинного дерева, в белене, белладонне, скополии. Помимо растений, алкалоиды содержатся в некоторых видах грибов (псилоцибин, содержащийся в грибах рода псилоцибе) и животных (буфотенин, содержащийся в коже некоторых жаб). Биогенные амины, такие как адреналинили серотонин, играющие важную роль в организмах высших животных, сходны с алкалоидами по строению и путям биосинтеза и иногда также называются алкалоидами. Кроме того, алкалоиды содержатся во многих морских организмах. СИНТЕЗ АЛКАЛОИДОВ Биогенетическими предшественниками большинства алкалоидов являются аминокислоты: орнитин, лизин, фенилаланин, тирозин, триптофан, гистидин, аспарагиновая кислота и антраниловая кислота. Все эти аминокислоты, кроме антраниловой кислоты, являются протеиногенными. Никотиновая кислота может быть синтезирована из триптофана или аспарагиновой кислоты. Пути биосинтеза алкалоидов не менее разнообразны, чем их структуры, и их невозможно объединить в общую схему. Тем не менее, существует несколько характерных реакций, участвующих в биосинтезе различных классов алкалоидов: - образование оснований Шиффа; - реакция Манниха; Основания Шиффа могут быть получены в результате реакции аминов с кетонами или альдегидами. Данная реакция является распространённым способом формирования C=N связи. 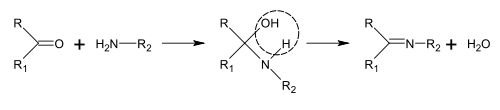 При биосинтезе алкалоидов реакция образования основания может проходить также внутримолекулярно. Примером может являться реакция образования Δ1-пиперидеина, происходящая при синтезе пиперидинового цикла: 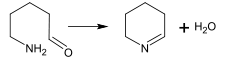 Реакция Манниха В реакции Манниха, помимо амина и карбонильного соединения, участвует также карбанион, играющий роль нуклеофила в процессе присоединения к иону, образованному взаимодействием амина и карбонильного соединения. 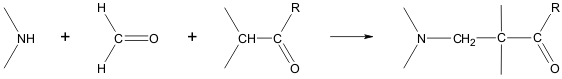 Реакция Манниха также может осуществляться как межмолекулярно, так и внутримолекулярно. Примером внутримолекулярной реакции Манниха может служить синтез пирролизидинового ядра: 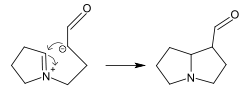 Разновидностью внутримолекулярной реакции Манниха является реакция Пикте – Шпенглера – циклизация шиффовых оснований, образованных из β-фенилэтиламинов с образованием системы тетрагидроизохинолина. У растений биосинтез алкалоидов происходит всегда под действием ферментов, у животных же известны случаи неферментативного синтеза изохинолиновых алкалоидов, включающий две последовательные стадии –образование основание Шиффа из катехоламинов и альдегида и реакцию Пикте –Шпенглера. Обе эти реакции могут протекать в физиологических условиях и в отсутствии ферментов. Обычно неферментативный синтез алкалоидов происходит при нарушениях обмена веществ или интоксикациях, когда в организме имеется избыток аминов или альдегидов. Так, высокий уровень катехоламинов в мозгу человека наблюдается при шизофрении, паркинсонизме. Сопутствующие этим заболеваниям нарушения психики отчасти связывают с неферментативным синтезом изохинолиновых алкалоидов. В результате приёма алкоголя из дофамина и ацетальдегида образуется алкалоид салсолинол, который является одним из факторов развития алкогольной зависимости. БИОЛОГИЧЕСКАЯ РОЛЬ Значение алкалоидов для живых организмов, их синтезирующих, до сих пор изучено недостаточно. Первоначально предполагалось, что алкалоиды являются конечными продуктами метаболизма азота у растений, как мочевина у млекопитающих. Позднее было показано, что во многих растениях содержание алкалоидов может как увеличиваться, так и уменьшаться с течением времени; таким образом, эта гипотеза была опровергнута. Большинство известных функций алкалоидов относятся к защите растений от внешних воздействий. Так, например, апорфиновый алкалоид лириоденин, вырабатываемый лириодендроном тюльпановым, защищает растение от паразитических грибов. Кроме того, содержание алкалоидов в растении препятствует их поеданию насекомыми и растительноядными хордовыми, хотя животные, в свою очередь, выработали способы противодействия токсичному действию алкалоидов; некоторые из них даже используют алкалоиды в собственном метаболизме. Алкалоиды имеют и эндогенное значение. Такие вещества, как серотонин, дофамин и гистамин, иногда также относимые к алкалоидам, являются важными нейромедиаторами у животных. Известна также роль алкалоидов в регулировке роста растений. ПРИМЕНЕНИЕ Медицинское применение растений-алкалоидоносов имеет давнюю историю. В XIX веке, когда первые алкалоиды были получены в чистом виде, они сразу нашли своё применение в клинической практике в качестве лекарственного средства. Многие алкалоиды до сих пор применяются в медицине (чаще в виде солей), например:
Многие синтетические и полусинтетические препараты являются структурными модификациями алкалоидов, разработанными с целью усилить или изменить основное действие препарата и ослабить нежелательные побочные эффекты. Так, например, налоксон, антагонист опиоидных рецепторов, является производным содержащегося в опиуме алкалоида тебаина:  Тебаин  Налоксон Применение в сельском хозяйстве До разработки широкой гаммы относительно малотоксичных синтетических пестицидов некоторые алкалоиды достаточно широко применялись в качестве инсектицидов (соли никотина и анабазина). Их применение было ограничено высокой токсичностью для людей. Психостимулирующее и наркотическое использование Многие алкалоиды являются психоактивными веществами. Препараты растений, содержащих алкалоиды, их экстракты, а позже и чистые препараты алкалоидов использовались в качестве стимулирующего и/или наркотического средства. Кокаин и катинон являются стимуляторами центральной нервной системы. Мескалин и многие индольные алкалоиды (такие как псилоцибин, диметилтриптамин, ибогаин) обладают галлюциногенным эффектом. Морфин и кодеин – сильные наркотические обезболивающие. Кроме того, существуют алкалоиды, не обладающие сильным психоактивным действием, но являющиеся прекурсорами для полусинтетических психоактивных веществ. Например, из эфедрина и псевдоэфедрина синтезируются меткатинон (эфедрон) и метамфетамин. СПИСОК ЛИТЕРАТУРЫ 1. Орехов А. П. Химия алкалоидов. – Изд. 2. – М.: АН СССР, 1955. 2. Кнунянц И. Л. Химическая энциклопедия. – М.: Советская энциклопедия, 1988. 3. Племенков В. В. Введение в химию природных соединений. – Казань, 2001. 4. Семёнов А. А., Карцев В. Г. Основы химии природных соединений. – М.: ICSPF, 2009. 5. Гринкевич Н. И., Сафронич Л. Н. Химический анализ лекарственных растений: Учебное пособие для фармацевтических вузов. – М., 1983. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||