Технология получения антибиотиков. Антибиотики возникли в борьбе за существование почвенных биоценозов, поэтому многие из них служат средствами нападения и защиты, т е. представляют собой своеобразное химическое оружие клетки
 Скачать 177.11 Kb. Скачать 177.11 Kb.
|
|
Антибиотики – специфические продукты жизнедеятельности организмов или их модификации, обладающие высокой физиологической активностью по отношению к определенным группам микроорганизмов или к злокачественным опухолям, задерживая их рост или полностью подавляя их развитие. К антибиотикам относятся низкомолекулярные эффекторы изначально природного происхождения, способные подавлять рост живых клеток. Антибиотики возникли в борьбе за существование почвенных биоценозов, поэтому многие из них служат средствами нападения и защиты, т.е. представляют собой своеобразное химическое «оружие» клетки. Однако эти функции у антибиотиков не единственны. Известно, что они могут участвовать в процессах детоксикации вредных метаболитов, контролировать некоторые стороны обмена веществ и целые процессы развития, например, дифференцировку клеток, служить запасными питательными веществами. В процессе образования антибиотиков задействовано значительное число генов. Массовая расшифровка первичной структуры геномов микроорганизмов показала, что эта величина равна 1 – 2 %. Так, у Bacillus subtilis число таких генов достигает 2 %, что обеспечивает микроорганизму большие возможности для защиты и адаптации. С другой стороны, это обстоятельство затрудняет анализ путей биосинтеза антибиотиков и идентификацию отдельных мутаций, способных увеличить выход продукта. Способность нитчатого гриба зеленой плесени Penicillium notatum вызывать гибель микроорганизмов впервые была установлена в 1928 г. английским микробиологом А. Флеммингом. Однако лечебные свойства этой плесени были описаны еще в 1871 г. русским дерматологом А. Г. Полотебновым. Открытие антибиотиков произвело переворот в лечении инфекционных заболеваний. Ушли в прошлое представления о неизлечимости многих бактериальных инфекций (туберкулез, сепсис, сифилис и др.). Антибиотики применяют в ряде отраслей народного хозяйства (растениеводство, животноводство, ветеринария, пищевая промышленность и др.), где они используются более широко, чем в медицине, например, для лечения сельскохозяйственных животных, борьбы с фитопатогенными микроорганизмами, а также для увеличения биомассы животных (биомицин – производное тетрациклина). Антибиотики широко используют в качестве молекулярных инструментов при исследовании фундаментальных проблем биологии, таких, как расшифровка механизмов биосинтеза белка, нуклеиновых кислот и структуры клеточных стенок бактерий, создание моделей транспорта ионов через биологические мембраны и др. Количество открываемых антибиотиков постоянно растет. В 1940 г. было известно всего 6 антибиотиков, а в настоящее время описано более 12 000 аналогичных соединений, из которых в клинике применяют около 200 препаратов. 97 % известных антибиотиков токсичны, поэтому в практике не используются. Изыскание новых форм антибиотиков обусловлено как потребностями практики, так и накоплением резистентных форм микроорганизмов по отношению ко многим антибиотикам. Устойчивость бактерий к пенициллинам и цефалоспоринам создает присутствующий в их клетках энзим лактамаза (пенициллиназа). Фермент гидролизует амидную связь β-лактамного цикла в молекуле антибиотика с образованием пенициллиновой кислоты, которая пол ностью лишена антимикробной активности:  Пенициллин Пенициллиновая кислота Резистентность микроорганизмов к антибиотикам обеспечивается разнообразием фенотипов резистентности и разнообразием, и стабильностью систем горизонтального генного транспорта. Поэтому главное направление получения новых антибиотиков состоит не в открытии новых соединений, а в химической трансформации природных молекул для создания полусинтетических антибиотиков, характеризующихся значительно меньшей резистентностью и токсичностью, но более широким спектром действия, большим временем жизни, химической и биологической устойчивостью. Важный подход на пути получения устойчивых аналогов антибиотиков – использование природных ингибиторов β-лактамаз – клавулановой и оливановой кислот. Классификация антибиотиков. По типу действия антибиотики делят на:
По спектру действия различают антибиотики
Особенность молекулярного механизма действия антибиотиков – исключительная специфичность их действия. Специфика действия их состоит в избирательном подавлении этими эффекторами одного или нескольких процессов у некоторых микроорганизмов. Таким образом, антибиотики блокируют метаболические мишени в клетках-мишенях. В зависимости от специфики действия антибиотиков на молекулярном уровне различают следующие группы соединений: 1. антибиотики, ингибирующие синтез клеточной стенки (пенициллины, ванкомицин, цефалоспорины, D-циклосерин); 2. антибиотики, нарушающие функции мембран (альбомицин, аскозин, грамицидины, кандицидины, нистатин, трихомицин, эндомицин и др.); 3. антибиотики, избирательно подавляющие синтез (обмен) нуклеиновых кислот: а) РНК (актиномицин, гризеофульвин, канамицин, неомнцин, новобиоцин, оливомицин и др.); б) ДНК (актидион, митомицины, новобиоцин, саркомицин и др.); 4. антибиотики – ингибиторы синтеза пуринов и пиримидинов (азасерин, саркомицин и др.); 5.антибиотики, подавляющие синтез белка (канамицин, метимицин, неомицин, тетрациклины, хлорамфеникол, эритромицин и др.); 6. антибиотики – ингибиторы дыхания (олигомицины, пиоцианин, усниновая кислота и др.); 7. антибиотики – ингибиторы окислительного фосфорилирования (валиномицин, грамицидины, колицины, олигомицин, тироцидин и др.); 8. антибиотики, обладающие антиметаболитными свойствами, т.е. выступают в качестве антиметаболитов аминокислот, витаминов, нуклеиновых кислот (фураномицин – антиметаболит лейцина); 9. антибиотики-иммуномодуляторы (актиномицины С и D, оливомицин, рубомицин). В зависимости от химической природы и ряда других свойств известные антибиотики делят на следующие классы:
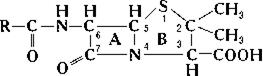
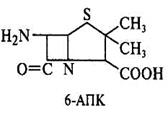
Рис.2. Структура пенициллина. Ядро молекулы – 6-аминопенициллановая кислота (6-АПК) – гетероциклическое соединение, состоящее из 4-членного β-лактамного (А) и 5-членного тиазолидинового (В) колец.
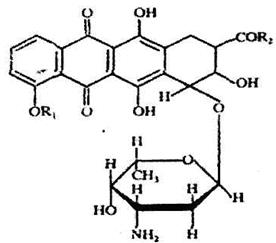
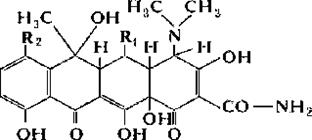 Рис.8.5.Структура тетрациклинов. Тетрациклин: R1 = H; R2 = H; Хлортетрациклин: R1 = H; R2 = Cl;Окситетрациклин: R1 = OH; R2 = H.
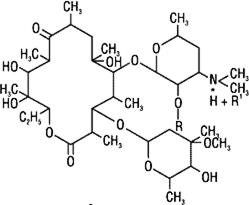
Рис.4 Структура эритромицина
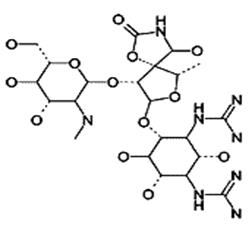
Рис.5.Структура стрептомицина А
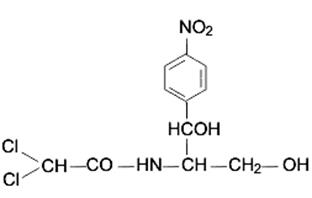 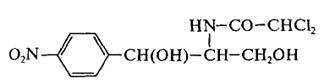 Рис.6 Структура хлорамфеникола и левомицетина
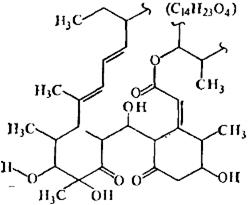
Рис.7 Частичная структура олигомицинов
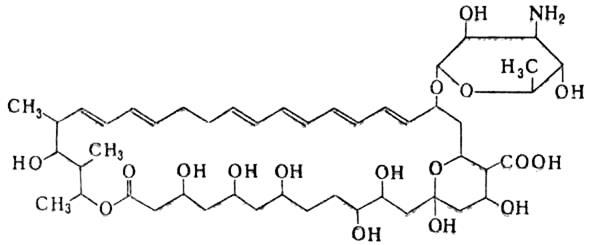 Рис.8.Структура нистатина
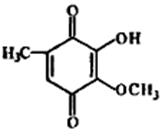
Рис.9. Структура хинонных антибиотиков: а) дауномицин; б) фумигатин; в) плюмбагин
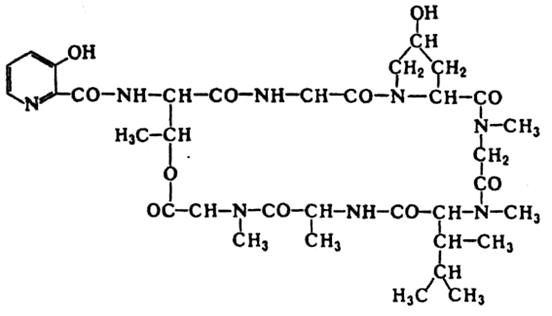 Рис.10. Структура амидомицина В зависимости от биологического происхождения антибиотики подразделяют на:
а) образуемые представителями рода Streptomyces:стрептомицин – S. griseus,тетрациклины – S. aureofaciens, Str. rimosus, новобиоцин – S. spheroides, эритромицин – Saccharopolyspora erythraea,актиномицины – S. antibioticus и др.; б) образуемые представителями рода Nocardia: рифамицины – N. mediterranei, ристомицин – N.fructiferi и др.; в) образуемые родом Actinomadura:карминомицин – A. carminata и др.; г) продуцируемые родом Micromonospora: фортимицины – М. olivoasterospora,гентамицины – М. риrриrеа;
Методы получения антибиотиков. Методы получения антибиотиков путем химического синтеза чрезвычайно сложны и не могут конкурировать с их биосинтезом методами биотехнологии. Существует несколько способов получения как природных, так и полусинтетических антибиотиков:
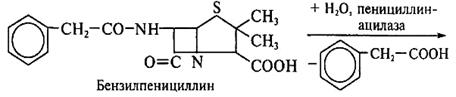
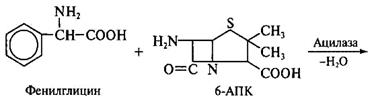
а) предполагаемая последовательность реакций, ведущая к синтезу антибиотика: А→Bфермент→C→D→E→антибиотик б)отсутствие синтеза антибиотика у «блокированного мутанта»: А→В фермент → C→D в) синтез модифицированного антибиотика после введения аналога предшественника (D*): D*→ E*→модифицированный антибиотик Принципы производства полусинтетических пенициллинов. Получение новых более эффективных аналогов пенициллина основано на изменении природы его ацильной группировки при сохранении в неизменном виде ядра пенициллина – 6-аминопенициллановой кислоты (6-АПК). В промышленности 6-АПК получают путем гидролиза природных пенициллинов с помощью специфического фермента ряда штаммов микроорганизмов – пенициллинацилазы. Ацилазы различают по их субстратной специфичности. Некоторые из ацилаз способны катализировать и обратные реакции – процессы ацилирования аминогруппы 6-АПК с образованием модифицированного пенициллина. Во многих случаях 6-АПК не выделяют из культуральной жидкости, например, при превращении бензилпенициллина в ампициллин:
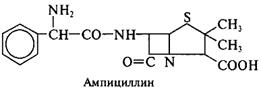
Бензилпенициллин гидролизуют ацилазой мутанта Kluyvera citrophila при рН 7,8 – 8,0 и температуре 40 – 50 °С. Затем в ферментатор вносят мутант Pseudomonas melanogenum и фенилглицин. Условия ферментации изменяют таким образом (рН 5,0 – 5,5), чтобы ацилаза второго мутантного организма осуществляла синтез ампициллина:
Замена ацильного остатка приводит к синтезу других полусинтетических антибиотиков. Технология промышленного получения антибиотиков. Биосинтез антибиотиков, как и любых других вторичных метаболитов, возрастает в фазе замедленного роста клеточной популяции (конец трофофазы) и достигает максимума в стационарной фазе (идиофазе). В конце трофофазы изменяется энзиматический статус клеток, появляются индукторы вторичного метаболизма, освобождающие гены вторичного метаболизма из-под влияния катаболитной репрессии. Поэтому любые механизмы, тормозящие клеточную пролиферацию и активный рост, стрессовые ситуации, активируют процесс образования антибиотиков. Процесс культивирования идиолитов проходит две фазы (двустепенчатое культивирование). На первой фазе происходит накопление достаточного количества биомассы, которая выращивается на среде для роста микроорганизма. Эта фаза должна быть быстрой, а питательная среда дешевой. На второй фазе осуществляются запуск и активный синтез антибиотика. На этой фазе ферментацию ведут на продуктивной среде. Образование антибиотиков регулируется условиями культивирования микроорганизмов. Поэтому оптимизация питательной среды является главным фактором в повышении выхода продукта. Многие антибиотики берут свое начало от промежуточных соединений обмена первичных метаболитов, поэтому их биосинтез регулируется путем ретроингибирования. Так, биосинтез пенициллина культурой гриба Penicillium chrysogenum контролируется по принципу обратной связи L-лизином. Кроме ретроингибирования биосинтез многих антибиотиков тормозится высокими концентрациями своих же антибиотиков. Следует отметить, что в процессе эволюции микроорганизмы выработали механизмы защиты от действия собственных антибиотиков. Эта проблема успешно решается в результате использования иммобилизованных ферментов. Большинство антибиотиков получают при глубинной аэробной ферментации периодического действия в асептических условиях. Период ферментации длится 7 – 10 суток. Технология завершающих стадий процесса определяется природой антибиотика, характером производства и целями даль нейшего использования антибиотиков. Для медицинских целей технология выделения и очистки имеет особое значение. Обычно она включает сложные многоступенчатые комбинации различных операций: экстракцию антибиотиков подходящими растворителями, осаждение и перекристаллизацию их из разных сред, фракционирование на ионообменных смолах, лиофильную и распылительную сушку готовых препаратов. Антибиотики выделяют или в виде сравнительно неочищенных препаратов (натриевая соль пенициллина), или в виде высокоочищенных веществ (прокаиновая соль пенициллина), предназначенных для клинического использования. Выход антибиотиков обычно составляет несколько десятков граммов на 1 л. Все антибиотики проходят биологический и фармакологический контроль. Биологический контроль позволяет определить стерильность готового препарата. Для этого используют метод внесения инактивированного антибиотика в стерильную питательную среду. Фармакологический контроль включает в себя определение спектра действия, токсичности (острой и хронической), устанавливают максимально переносимую дозу (МПД), дозу, вызывающую 50 % гибели животных (LD 50) и дозу смертельную для всех животных (LD 100). После всестороннего изучения препарата может быть рекомендован к практическому применению. | |||||||||||||||||||