Ароматические галогенопроизводные. Ароматические галогенопроизводные
 Скачать 88.15 Kb. Скачать 88.15 Kb.
|
|
Ароматические галогенопроизводные Ароматическими галогенопроизводными называют производные ароматических углеводородов, у которых один или несколько атомов водорода замещены атомами галогенов. В зависимости от положения атомов галогенов различают две группы галогенопроизводных ароматического ряда: – галогенарены – соединения, у которых атомы галогена непосредственно связаны с бензольным кольцом: 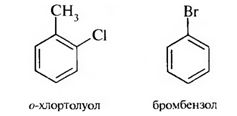 – арилалкилгалогениды – соединения, содержащие атомы галогена в боковой цепи (алкильном радикале): 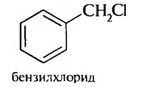 1.3.1. Способы получения Для введения галогена в бензольное ядро используют: 1. Реакцию галогенирования аренов. Реакция протекает по ионному механизму в присутствии катализаторов хлоридов металлов А1С13, FeBr3, SbCl,: 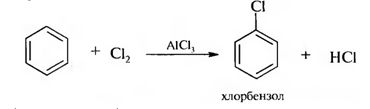 Катализатор способствует образованию положительного иона галогена, который осуществляет замещение в бензольном ядре. 2. Реакцию солей арилдиазония с галогенидами меди: 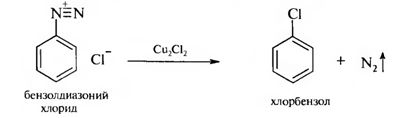 Для введения галогена в боковую углеродную цепь используют: 1. Галогенирование алкиларенов. Реакция идет при нагревании до высоких температур или при облучении УФ-светом. Механизм радикальный: 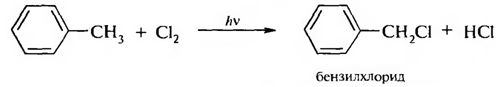 Галогенированию подвергается в основном α-положение относительно бензольного ядра, поскольку в этом случае образуется устойчивый свободный радикал бензильного типа. 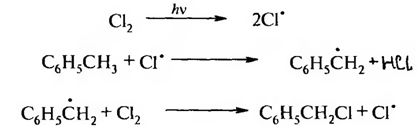 2. Реакцию хлорметилирования. При действии на ароматические углеводороды формальдегида и хлороводорода в присутствии катализатора (А1С13, ZnCl2) атом водорода в кольце замещается на хлорметильную группу: 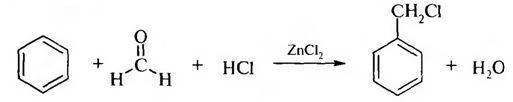 1.3.2. Физические свойства Галогенопроизводные ароматического ряда – это жидкие или кристаллические вещества. Температуры кипения галогенаренов возрастают в ряду: фтор-, хлор-, бром-, йодпроизволные. Соединения этого ряда не растворимы в воде, но легко растворимы в органических растворителях. 1.3.3. Химические свойства Реакционная способность ароматических галогенопроизводных зависит от положения галогенов. Для соединений, содержащих галоген в боковой цепи, характерны все реакции галогеналканов. Соединения, в которых галоген непосредственно связан с бензольным ядром, характеризуются низкой реакционной способностью связи С-Hal. Это обусловлено сопряжением неподеленной пары электронов атома галогена с π-электронной системой бензольного ядра: 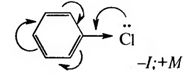 Галогенарены похожи в этом отношении на винилгалогениды. В результате сопряжения происходит укорочение и уменьшение полярности связи С-Hal. Поэтому реакции нуклеофильного замешения идут лишь в очень жестких условиях: 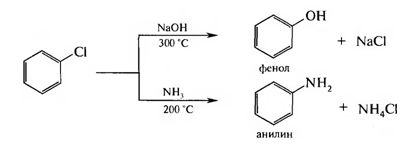 Подвижность атома галогена возрастает с введением в орто- или пара-положения по отношению к галогену электроноакцепторного заместителя в бензольное ядро, который увеличивает дробный положительный заряд на атоме углерода связи С-Hal. Реакция замещения галогена протекает в более мягких условиях и идет по механизму SN2: 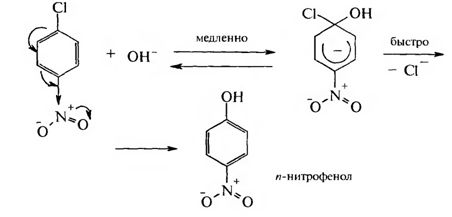 Образование σ-комплекса является лимитирующей стадией реакции. По ароматическому ядру галогенарены вступают в обычные реакции электрофильного замещения. Атом галогена, связанный с бензольным ядром, проявляет –I и +М-эффекты. Поскольку в статическом состоянии –I-эффект > +М-эффекта, то атом галогена проявляет элктроноакцепторные свойства и снижает реакционную способность бензольного ядра в реакциях SE . В динамическом состоянии +М-эффект > –I-эффекта, поэтому атомы галогена выступают как ориентанты I рода, направляя заместители в орто- и пара-положения. Например: 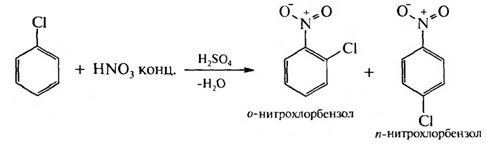 В результате реакции образуются два изомера: о-нитрохлорбензол и п-нитрохлорбензол. |
