Биохимия печени. Лекция Астахова. Биохимия печени Печень самая крупная железа организма. Это своеобразная биохимическая лаборатория, которая играет важную роль в белковом, углеводном и липидном обменах.
 Скачать 3.19 Mb. Скачать 3.19 Mb.
|
|
Биохимия печени Печень – самая крупная железа организма. Это своеобразная «биохимическая лаборатория», которая играет важную роль в белковом, углеводном и липидном обменах. В печени синтезируются важнейшие белки плазмы крови: альбумин, фибриноген, протромбин, церулоплазмин, трансферрин, ангиотензиноген и др. Эти белки участвуют в регуляции АД и объёма циркулирующей крови, необходимы для свёртывания крови, метаболизма железа и др. Основные функции печени
– Глюконеогенез – Синтез и распад гликогена – Пентозофосфатный путь
– Синтез ЖК и жиров из углеводов – Синтез и выведение холестерола – Формирование липопротеинов – -окисление жирных к-т – Синтез кетоновых тел – Синтез желчных кислот
– Синтез белков плазмы крови (включая некоторые факторы свертывания крови) – Орнитиновый цикл (обезвреживание NH3)
– Метаболизм и выделение стероидных гормонов – Метаболизм полипептидных гормонов
– гликогена – витамина A – витамина B12 – железа
– Метаболизм и экскреция Обезвреживающая функция печени. ! Самая важная функция печени: обезвреживание токсических веществ.  Ксенобиотики – это чужеродные вещества, попадающие в организм из окружающей среды и не использующиеся для пластических и энергетических целей организма. Они попадают в организм с пищей, через кожу и легкие. Примеры: нефтепродукты, пластмассы, моющие средства, парфюмерия, красители, пестициды и др. Гидрофильные ксенобиотики выводятся из организма в неизменённом виде в основном с мочой. Гидрофобные ксенобиотики могут накапливаться и, взаимодействуя с белками и липидами клеток, нарушать их структуру и функции. Обезвреживание ксенобиотиков происходит во многих тканях, но наиболее активно в печени. Обезвреживание веществ в печени может состоять из одного или двух этапов. Этапы обезвреживания веществ в печени:
Включает реакции их гидролиза, окисления, гидроксилирования, восстановления и др. ! Наиболее частая модификация гидрофобного в-ва на 1 этапе – гидроксилирование.
Если вещество гидрофобно, то его обезвреживание проходит в 2 этапа, если – гидрофильно, то 1 этап может отсутствовать. Некоторые полярные ксенобиотики выводятся из организма, не подвергаясь никаким превращениям. Метаболизм и выведение ксенобиотиков из организма: 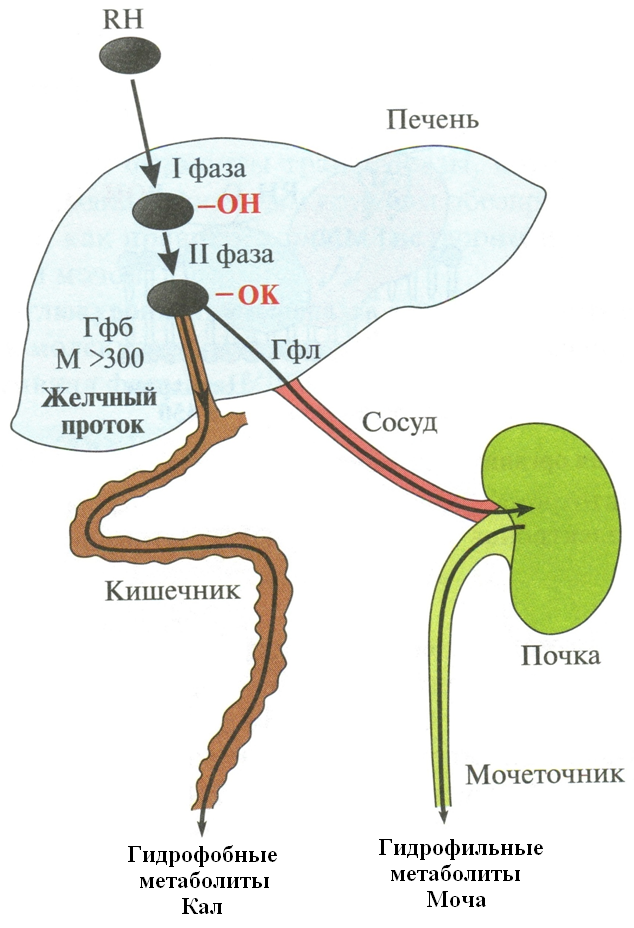 RH – ксенобиотик; K – радикал, используемый при конъюгации. Примеры модификации ксенобиотиков в 1 стадии: – гидроксилирование – окисление по атому S (сульфоокисление) – Окислительное дезаминирование – Дезалкилирование по N, O, S. – Эпоксидирование 1) Система микросомального окисления За 1 стадию обезвреживания отвечает система микросомального окисления (СМО), локализованная в мембранах ЭР. СМО работает практически во всех тканях организма, но наиболее активно в печени. В печени существуют 2 электрон-транспортные цепи СМО, которые катализируют гидроксилирование субстратов и являются монооксигеназами. 1 цепь включает:
2 цепь включает:
Цитохром P450 один атом O2 включает в молекулу субстрата, а 2-й восстанавливает с образованием H2O за счет переноса ē и Н+ от NADPH+H+ при участии цитохром P450-редуктазы (или от NADH+H+ с помощью цитохром b5-редуктазы и цитохрома b5). Примеры модификации ксенобиотиков в 1 стадии обезвреживания: 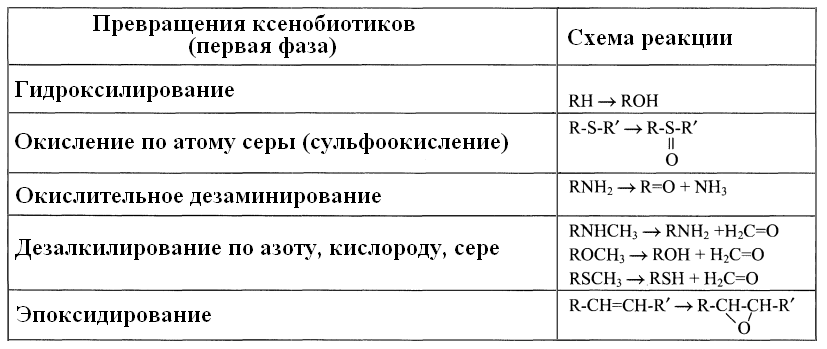 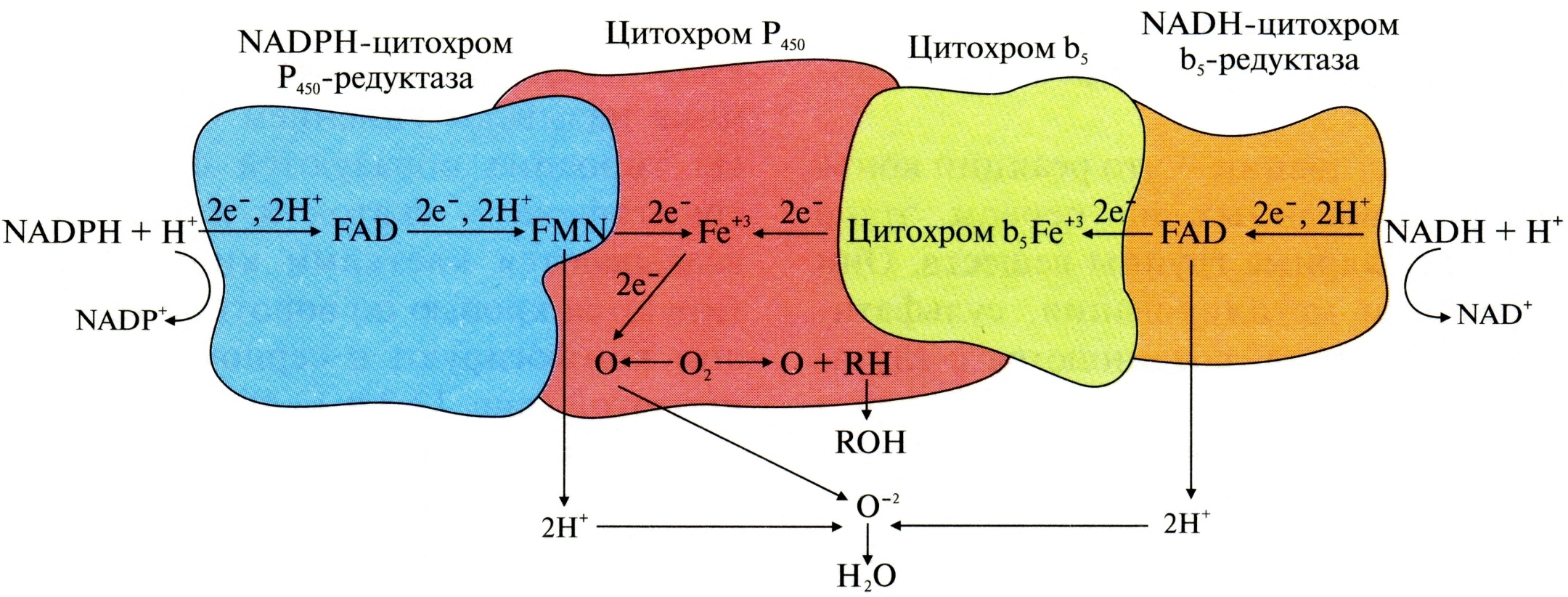 Появление в молекулах субстратов полярных групп в результате микросомального окисления повышает гидрофильность веществ и обеспечивает возможность их вступления в реакции конъюгации. Второй этап инактивации – это реакции конъюгации модифицированных на 1 этапе или содержащих полярные группы веществ. Реакции конъюгации – присоединение к гидрофильным группам какого-либо вещества (глюкуроновая кислота, серная кислота, глицин, глутамин, ацетильный остаток и др.). Эти реакции катализируют трансферазы, имеющие широкую субстратную специфичность. ! Конъюгация снижает реакционную способность веществ и, следовательно, уменьшает их токсичность, повышает гидрофильность и способствует выведению их из организма. Донором CH3– группы является SAM, группы –SO3H – активная форма серной кислоты (ФАФС), ацетильной группы – ацетил-КоА, остатка глюкуроновой кислоты – УДФ-глюкуронат. Примеры реакций конъюгации: 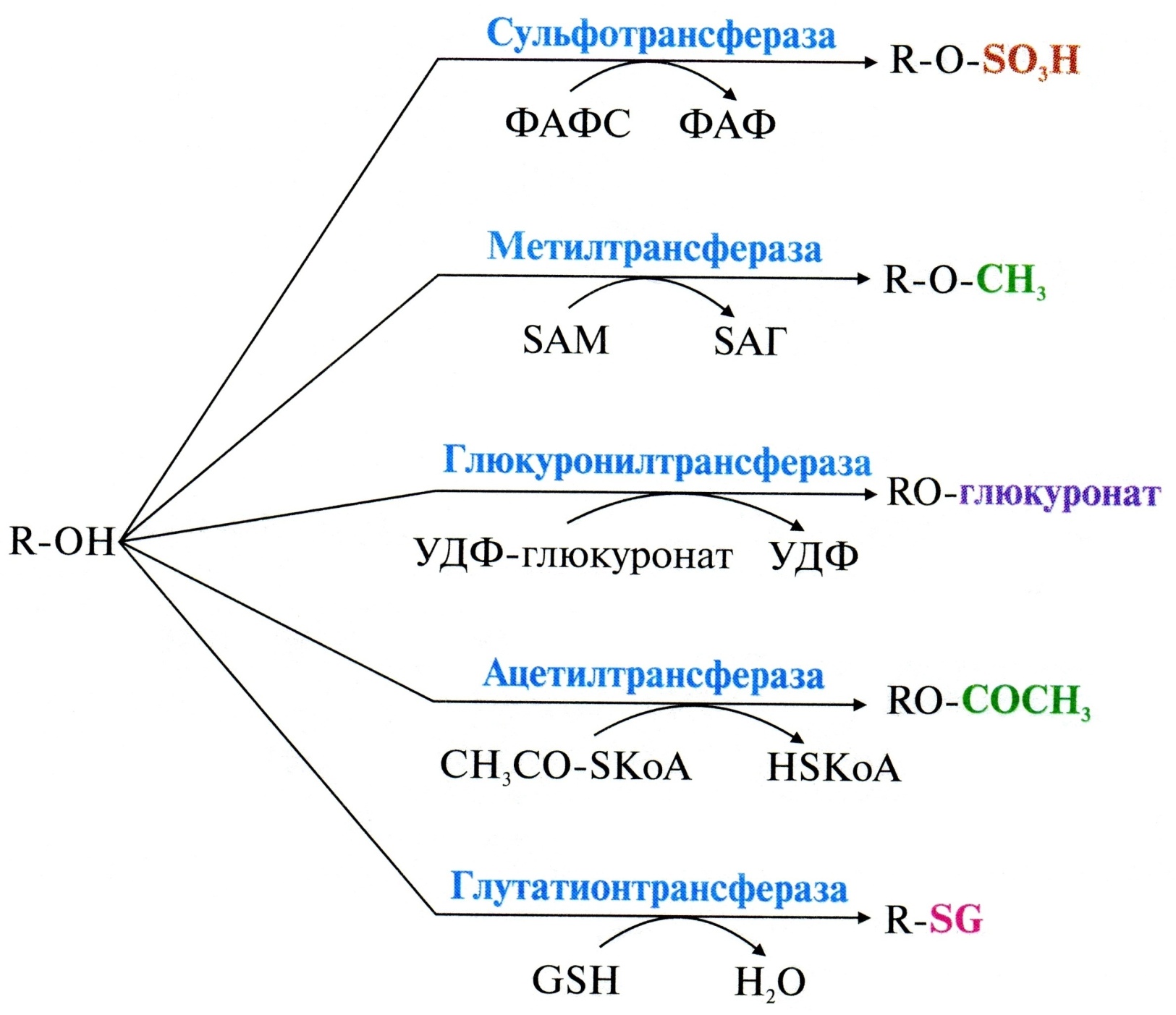
Ферменты: УДФ-глюкуронилтрансферазы Активная форма: УДФ-глюкуронат: 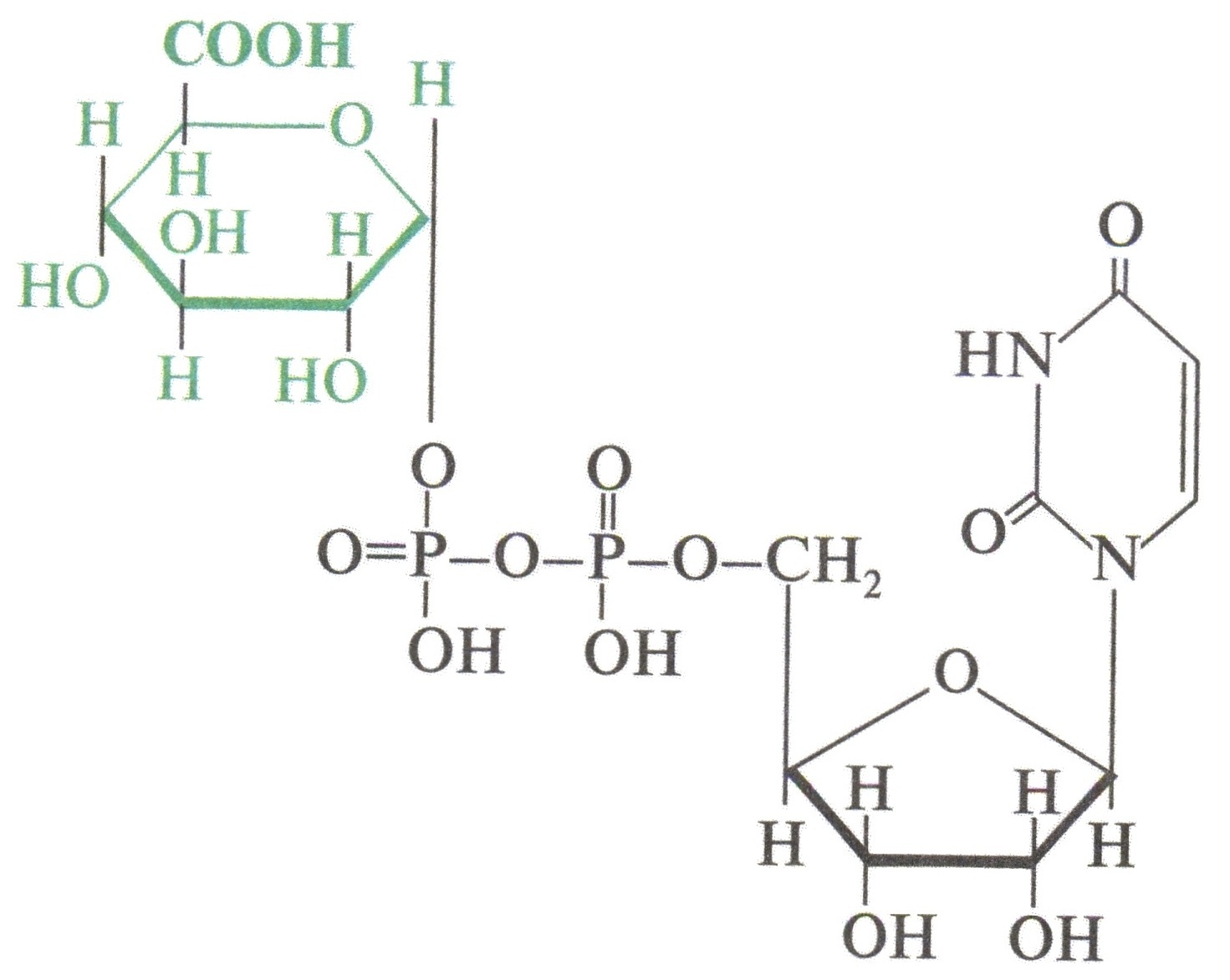 Реакция в общем виде: ROH + УДФ–C6H9O6 RO–C6H9O6 + УДФ
Ферменты: сульфотрансферазы Активная форма: ФАФС – фосфоаденозинфосфосульфат: 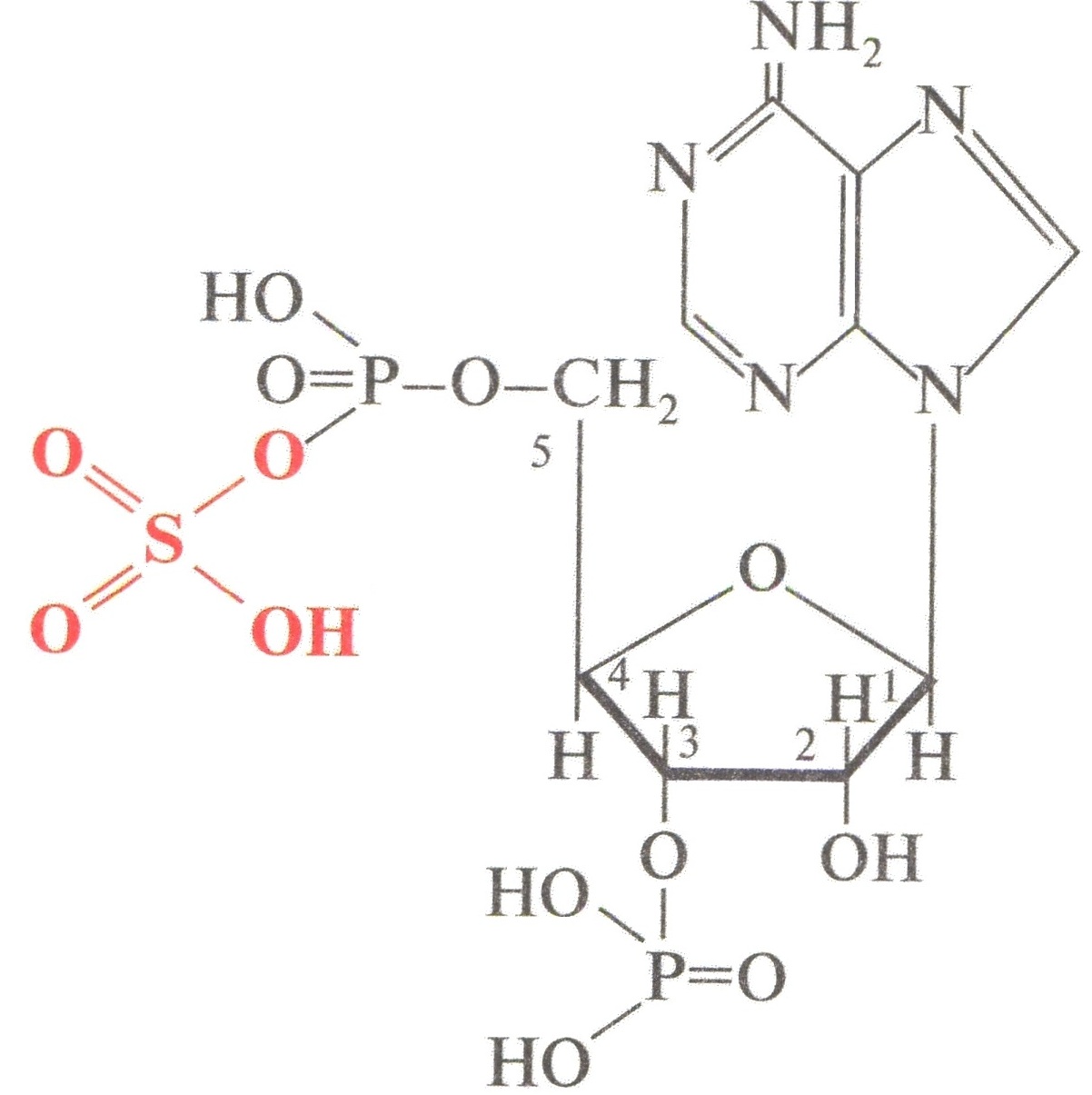 Реакция в общем виде: ROH + ФАФ–SO3H RO–SO3H + ФАФ
Для работы ферментов требуется глутатион. Глутатион – трипептид глу-цис-гли. Остаток Глу присоединен к Цис COOH-группой радикала. Глутатион: 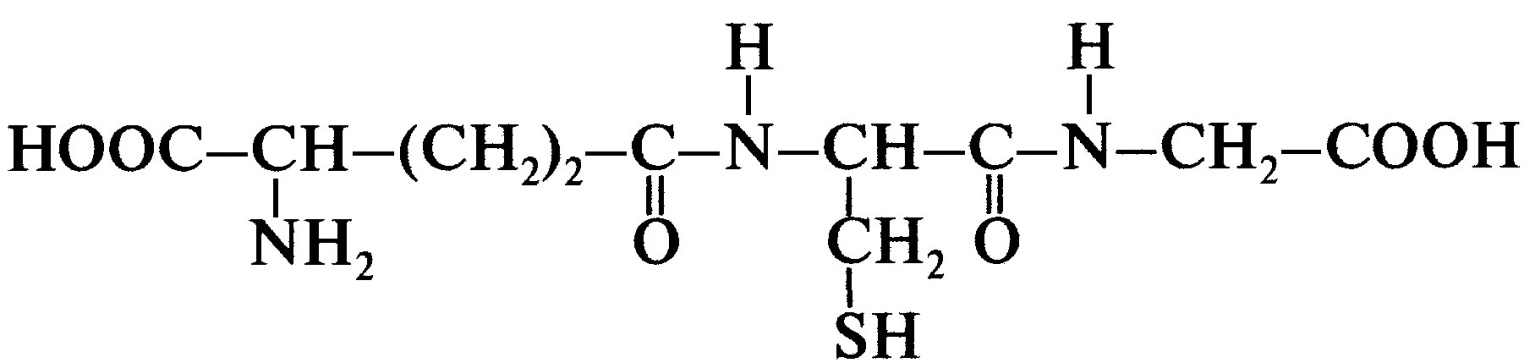 ГТазы имеются во всех тканях (больше всего: в печени). ! Играют важную роль в обезвреживании собственных метаболитов: некоторых стероидных гормонов, простагландинов, билирубина, желчных кислот, продуктов ПОЛ и др. 3 пути обезвреживания ксенобиотиков с участием ГТазы:
R + ГSH ГSRH
RX + ГSH ГSR + НХ Например, 1-хлор-2,4-динитробензол обезвреживается следующим образом: 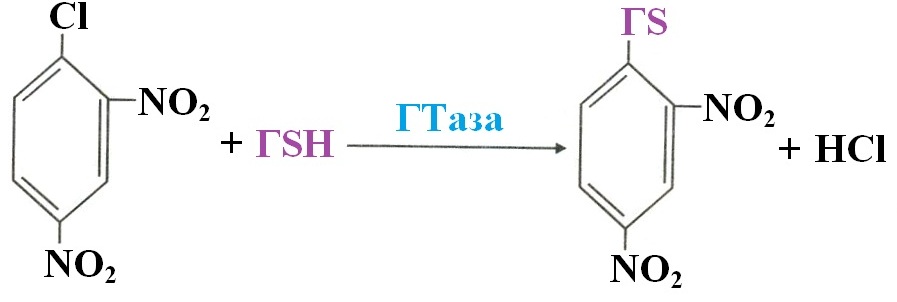
R–HC–O–OH + 2 ГSH R–HC–OH + ГSSГ + H2O. –ООН – гидроперекисная группа, ГSSГ – окисленный глутатион. Участие P-гликопротеина в обезвреживании ксенобиотиков. P-гликопротеин необходим для выведения из клетки гидрофобных ксенобиотиков. Также он участвует в выведении из клетки лекарственных в-в, использующихся в химиотерапии. P-гликопротеин - фосфогликопротеин, который присутствует в мембране многих клеток, особенно почек и кишечника. Содержит 12 трансмембранных доменов и 2 АТФ-связывающих центра. Гидрофобное в-во, проникая в клетку выводится из нее с участием АТФ: 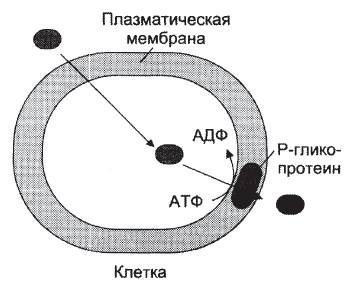 С этим механизмом связана 1 из причин множественной лекарственной устойчивости. Примеры обезвреживания токсических в-в в печени:
В толстой кишке происходит гниение белков – это образование токсичных продуктов из аминокислот под действием ферментов микроорганизмов кишечника. В основе гниения лежат реакции декарбоксилирования и дезаминирования аминокислот. В ходе гниения, из тирозина образуются фенол и крезол, из триптофана – скатол и индол. Эти вещества всасываются клетками кишечника, транспортируются кровью по воротной вене в печень, где они конъюгируют с серной или глюкуроновой кислотой. Если в организм попадает бензол, то его обезвреживание происходит в 2 этапа. Сначала он гидроксилируется с помощью СМО и превращается в фенол, а потом вступает в реакции конъюгации с ФАФС или УДФ-глюкуронатом. Реакции обезвреживания фенола, крезола и бензола: 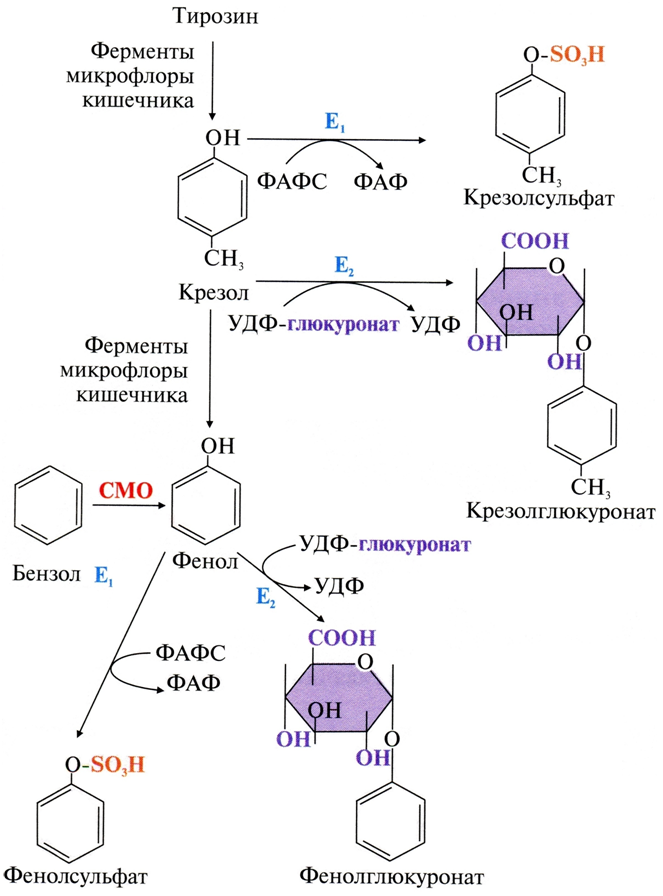 Реакции обезвреживания индола и скатола: 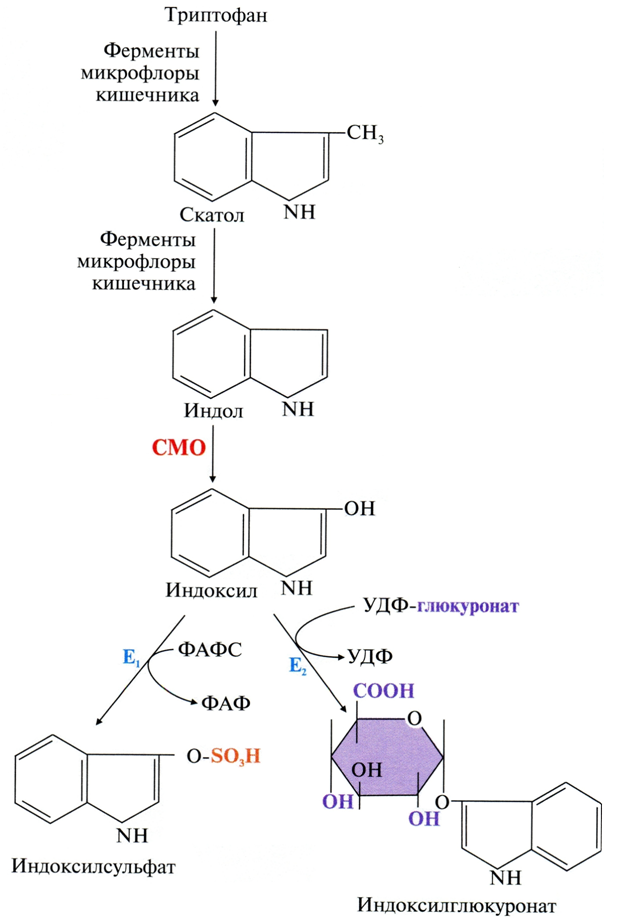 Биотрансформация лекарств в печени Лекарства либо выводятся из организма в неизмененном виде, либо подвергаются химической модификации. В результате биотрансформации лекарственных веществ может произойти:
(фенобарбитал, нитриты, эфедрин и др.)
(ловастатин, метилдофа, норморфин и др.)
(фенацетин, сульфаниламиды) Инактивация лекарственных в-в (как и ксенобиотиков) происходит в 1 или в 2 фазы. Примеры инактивации лекарственных в-в: Аспирин (ацетилсалициловая кислота) сначала гидролизуется и превращается в салициловую кислоту, которая конъюгирует с УДФ-глюкуронатом: Сульфаниламиды (альбуцид, сульгин, сульфаметоксазол) инактивируются в результате реакций ацетилирования: Реакции инактивации аспирина: 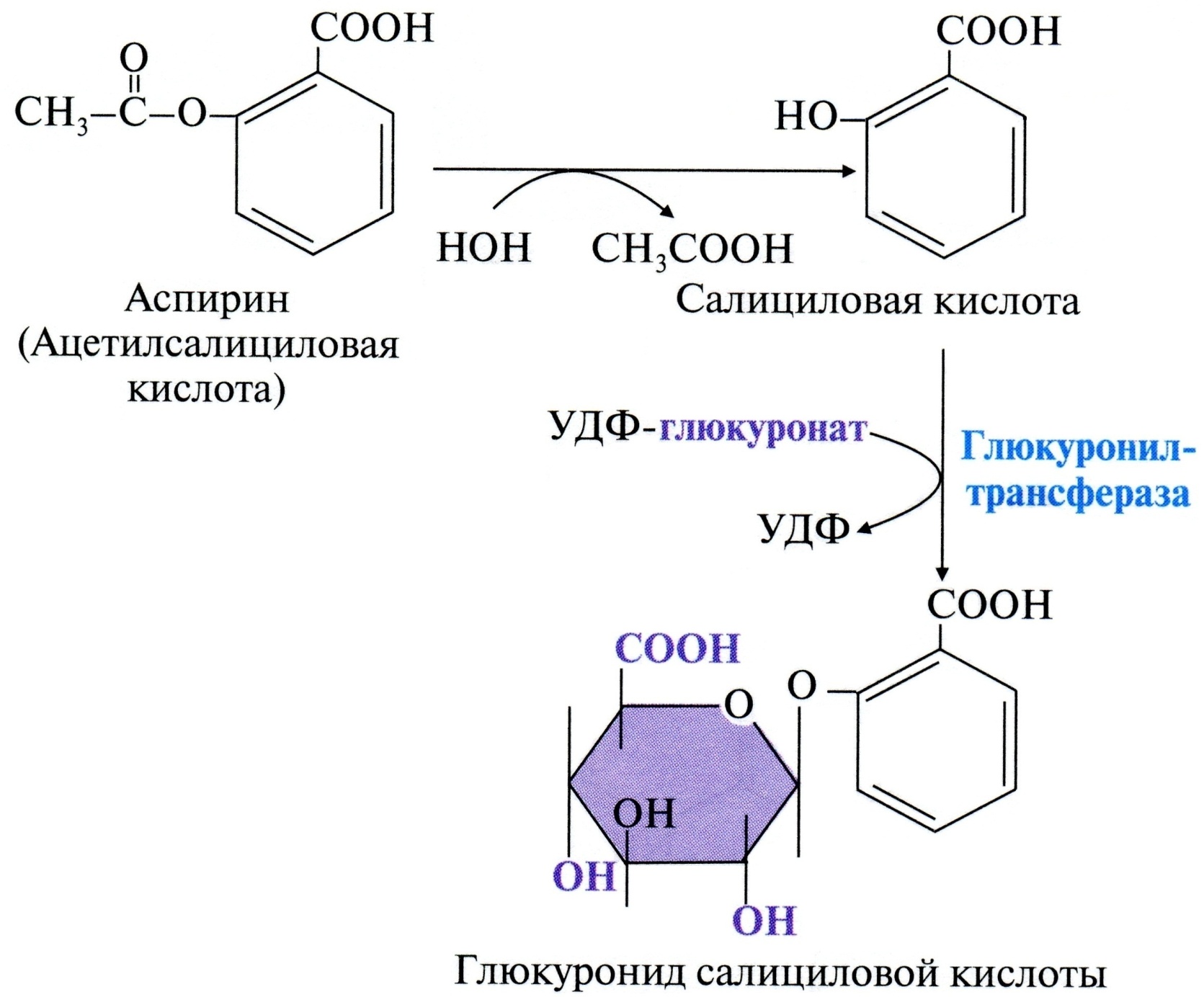 Инактивация сульфаниламидов: 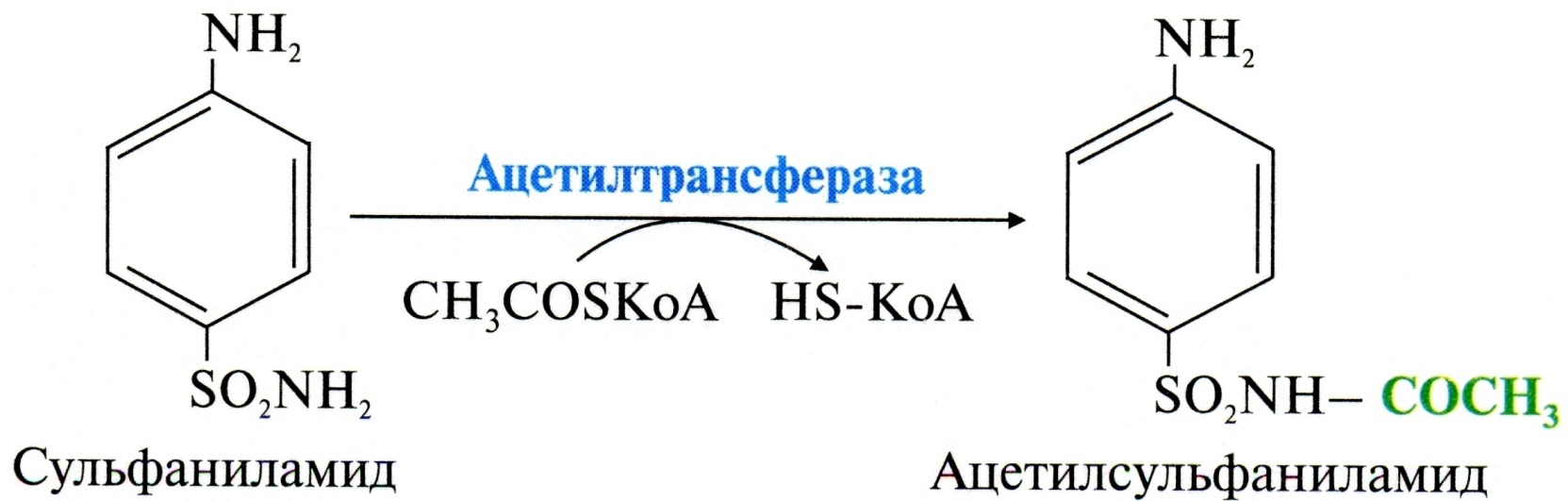 Пример повышения активности лекарственных в-в: Превращение имипрамина в более активное в-во – дезметилимипрамин: 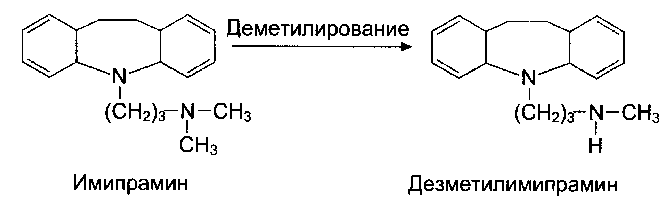 Дозы некоторых лекарств при частом приеме необходимо увеличивать, так как их действие на организм ослабляется. Это происходит потому, что эти лекарства, как и другие чужеродные соединения, индуцируют синтез ферментов СМО и реакций конъюгации. На этой особенности основано привыкание к лекарствам и некоторым ядам. ("Эффект Митридата") Аналогичное действие вызывает и этанол. Поэтому, в состоянии алкогольного опьянения существенно снижается эффективность многих лекарственных в-в. Химический канцерогенез В основе химического канцерогенеза – повреждения ДНК под действием химических канцерогенов. ! Химические канцерогены способствуют превращению протоонкогена в онкоген. Протоонкоген – ген, содержащий информацию о белке, регулирующем нормальную пролиферацию клеток, и способный в результате изменения структуры превращаться в онкоген. Известно несколько сотен протоонкогенов, мутации в которых могут привести к превращению нормальной клетки в опухолевую. Онкоген – ген, экспрессия которого приводит к неконтролируемой пролиферации клеток. Для превращения протоонгкогена в онкоген требуются определенные изменения в его регуляторной или структурной части. Многие в-ва, попадающие в организм, являются проканцерогенами. Они превращаются в канцерогены в ходе «обезвреживания» в печени. Некоторые химические проканцерогены:
Примеры канцерогенных в-в:
Используются в производстве анилиновых красителей и резиновой промышленности. 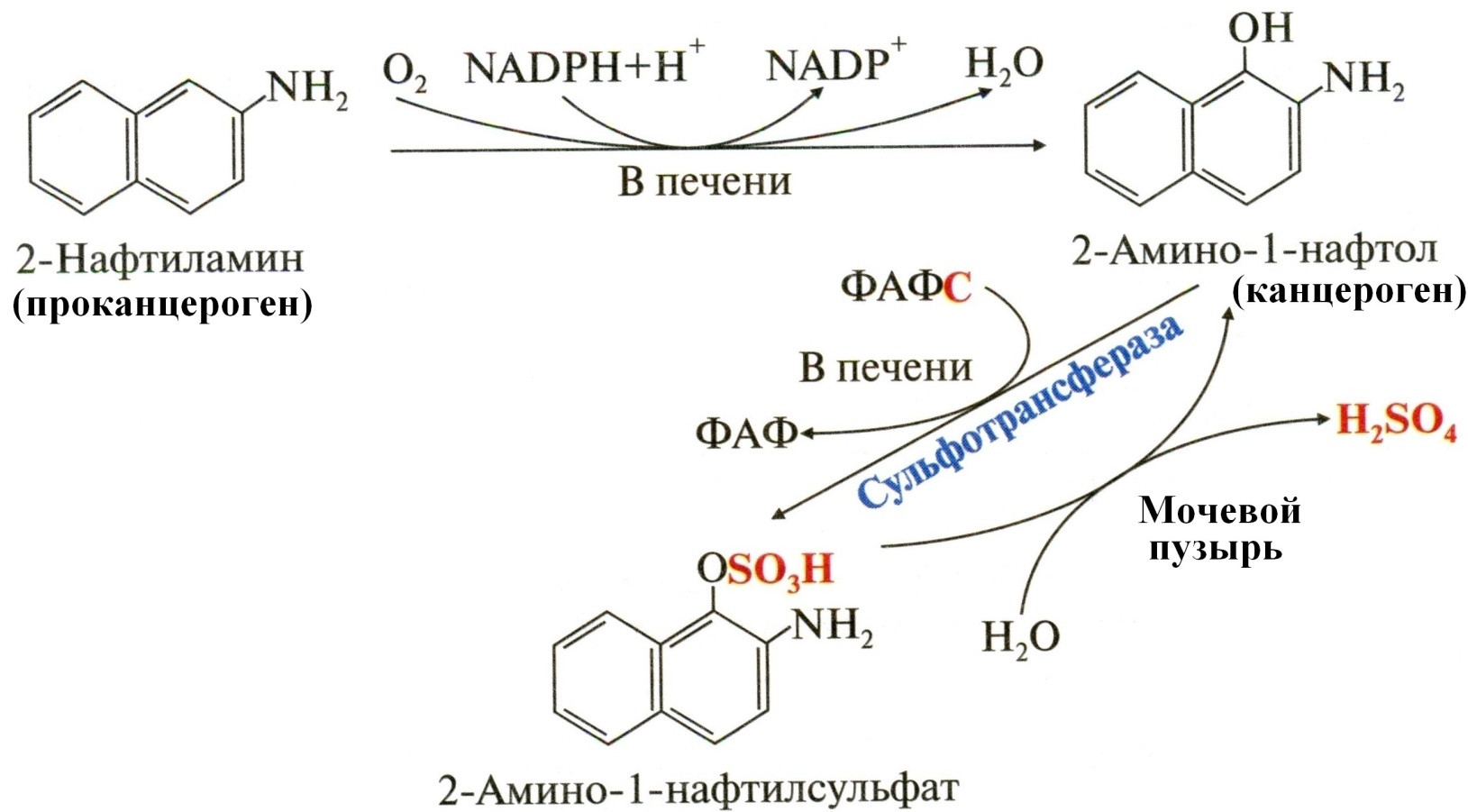 Активный канцероген 2-амино-1-нафтол вызывает рак мочевого пузыря.
Яркий представитель - бензантрацен. Содержится в выхлопных газах и сигаретном дыме. Активный канцероген: эпоксид бензантрацена. Может вызвать рак легких, печени и желудка. 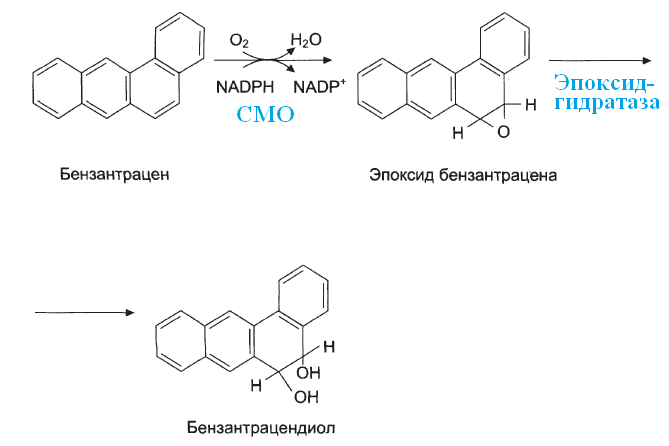 Эпоксиды обладают высокой химической активностью. Они могут участвовать в реакциях неферментативного алкилирования ДНК, РНК и белков, что может способствовать перерождению нормальной клетки в опухолевую.
Типичные представители: Афлатоксины – метаболиты некоторых видов плесени. Образуются при неправильном хранении зерна, круп, орехов. Яркий представитель – Афлатоксин B1: 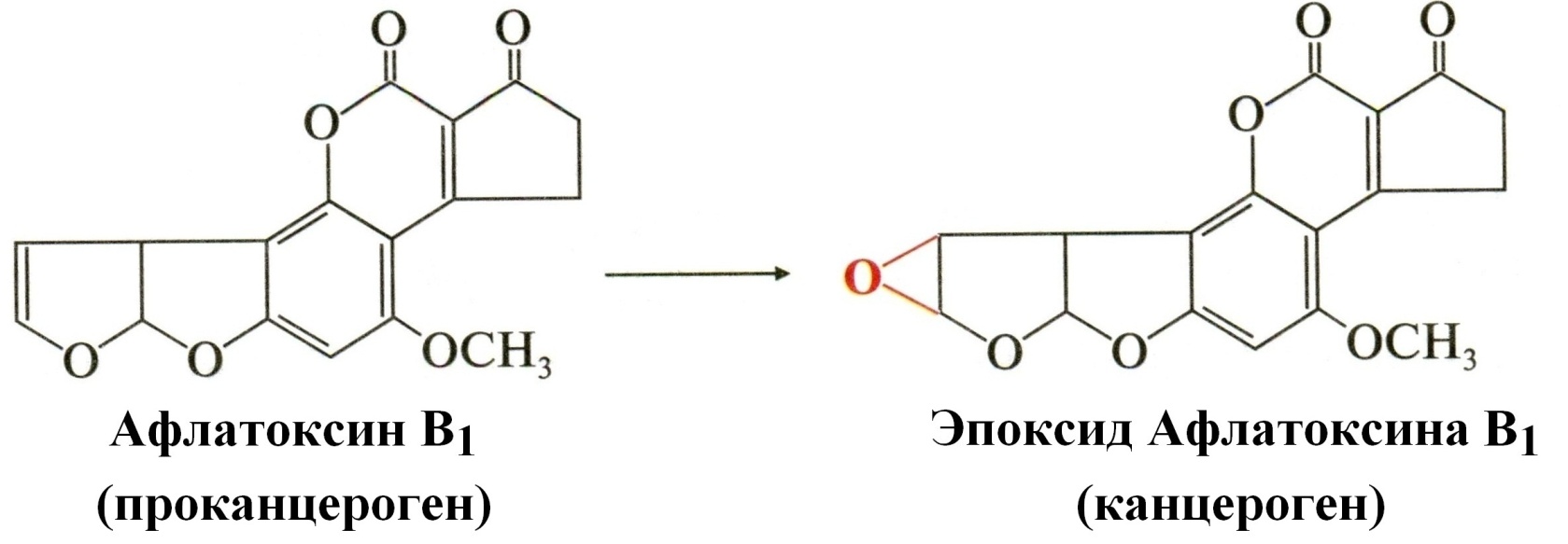 Активный канцероген Эпоксид Афлатоксина B1 вызывает рак печени.
Нитраты в высокой концентрации. Нитраты и особенно нитриты – сильные окислители: 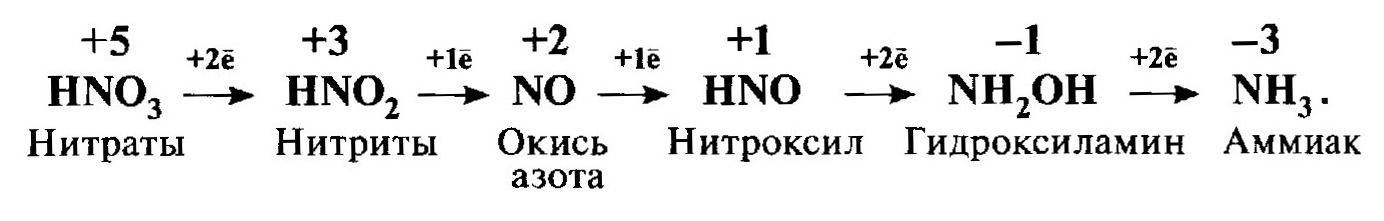 Они могут повреждать ДНК, окислять многие гемопротеины (Hb, цитохромы и т.п.). В организме из HNO2 и вторичных аминов образуются нитрозамины R2N–N=O, которые являются сильными мутагенами, вызывающими алкилирование азотистых оснований ДНК. |
