физическая химия рр3. пример к УЗ 4 РР 2_52993_1633876431. Чистый углекислый газ co
 Скачать 72 Kb. Скачать 72 Kb.
|
|
Пример Углекислый газ массой 200 г находится в состоянии 1 при температуре 600 К и давлении 2,5 атм. Его перевели в состояние 2, при котором температура равна 298 К, а давление 1 атм. Принимая свойства углекислого газа близкими к свойствам идеального газа, найти изменения мольных и полных объема; энтропии; энтальпии; внутренней энергии и энергии Гиббса системы при этом переходе. Дано: чистый углекислый газ CO2. Найти: Решение. Из справочных таблиц определяем форму уравнения и значения коэффициентов температурной зависимости мольной изобарной теплоемкости углекислого газа. Упростим обозначение, помня, что рассматриваем чистый углекислый газ, опустим в записи некоторые индексы.
Используя уравнение состояния идеального газа, находим изменение мольного объема следующим образом: 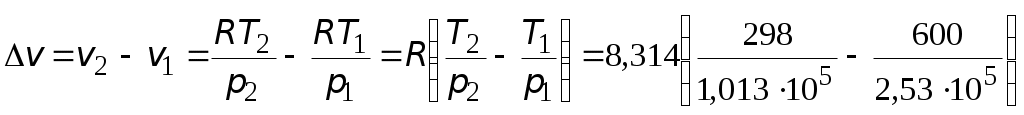 = == 4,74∙10−3 м3/моль. Полное изменение объёма углекислого газа при рассматриваемом переходе составит Число молей находим по формуле 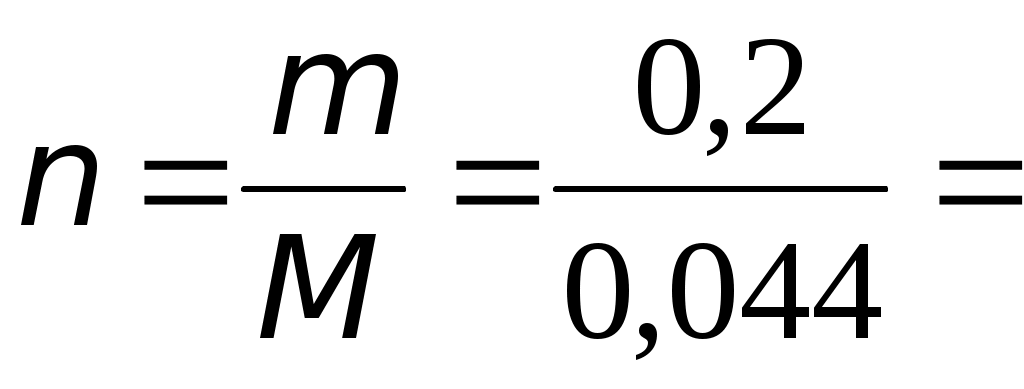 4,55 моль. 4,55 моль.Расчет мольного изменения энтропии углекислого газа при переходе из состояния 1 в состояние 2 производится по формуле 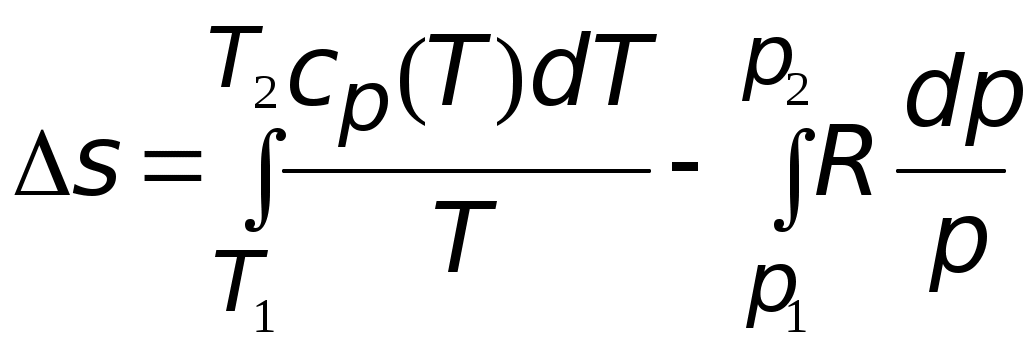 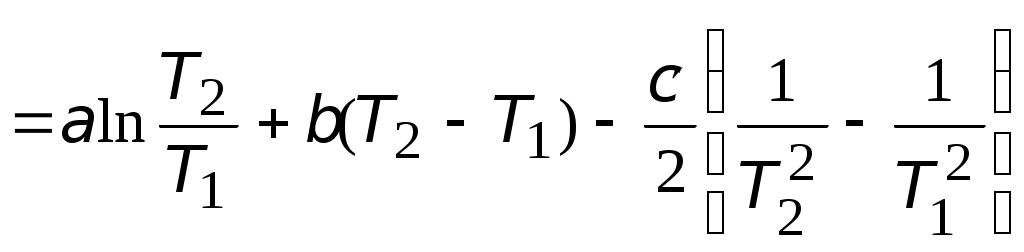 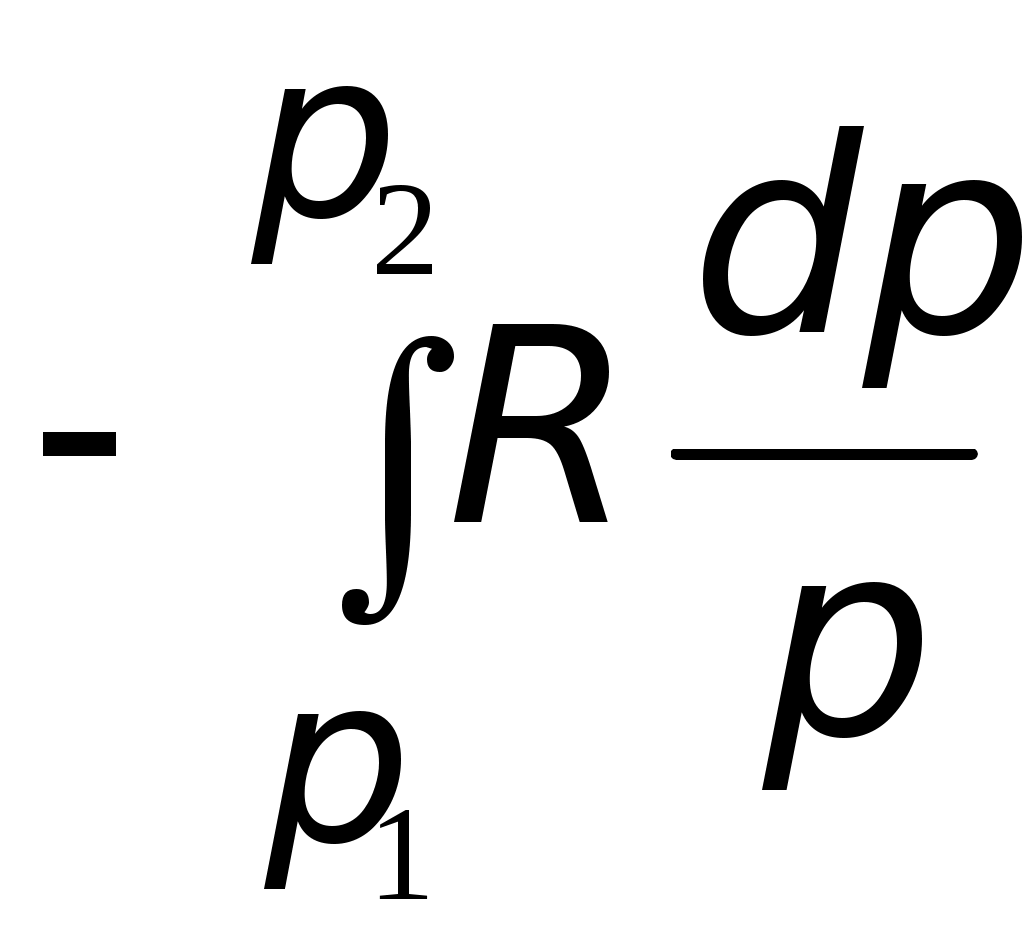 = =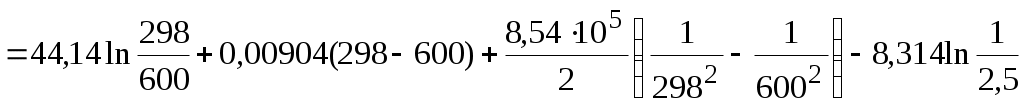 = == −46,89 Дж/(мольК). Полное изменение энтропии равно 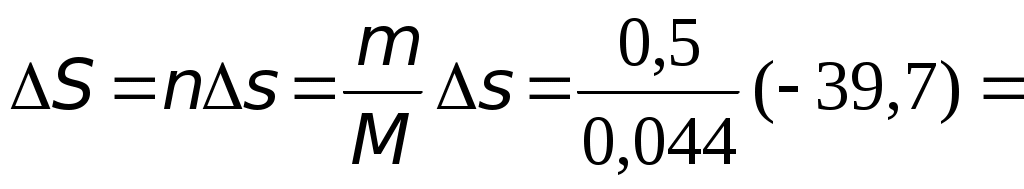 −213,32 Дж/К. −213,32 Дж/К.Для идеального газа изменение энтальпии не зависит от давления, поэтому формула для расчета мольного изменения энтальпии имеет вид: 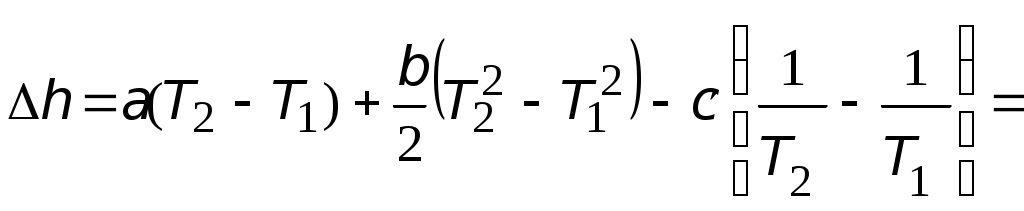 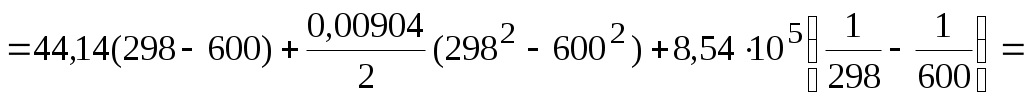 Полное изменение энтальпии равно Для идеального газа мольное изменение внутренней энергии связано с мольным изменением энтальпии Следовательно, Полное изменение внутренней энергии найдем как Мольное изменение энергии Гиббса при переходе углекислого газа из состояния 1 в состояние 2 определим как Но известно, что Тогда Мольные изменения энтальпии и энтропии определены ранее, значение мольной энтропии в состоянии 2 можно найти по справочнику, т.к. это состояние 298 К и 1 атм: | ||||||||||||||||||
