Фарм химия. Варіант14. Добування. Електрохімічне окиснення глюкози в присутності крейди та брому
 Скачать 7.93 Mb. Скачать 7.93 Mb.
|
|
Варіант14 182. Приведіть схему синтезу кальцію глюконату з вказівкою хімічних назв вихідних, проміжних і кінцевих продуктів; його фармакологічну дію. Запропонуйте можливі методи ідентифікації кальцію глюконату. Де це можливо, приведіть рівняння хімічних реакцій. Відповідь Добування. Електрохімічне окиснення глюкози в присутності крейди та брому 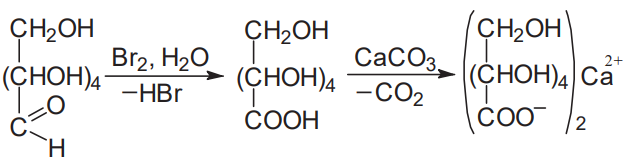 Глюкоза глюконова кислота кальцію глюконат Ідентифікація: 1. Методом тонкошарової хроматографії. 2. Субстанція дає реакції на іони кальцію. а ) При взаємодії іонів кальцію з розчином гліоксальгідроксіаніла в спирті в присутності розчину натрію гідроксиду розведеного і натрію карбонату , і струшування з хлороформом - хлороформний шар забарвлюється в червоний колір : 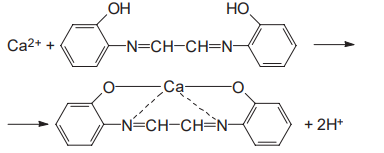 b ) До розчину субстанції розведеної оцтової кислоти додають розчин калію ферроцианида , білий осад утворюється після додавання амонію хлориду : Ca2+ + 2NH4+ + [Fe(CN)6]4- → (NH4)2Ca[Fe(CN)6]↓ c ) При взаємодії катіонів кальцію з розчином амонію оксалату утворюється білий осад , нерозчинний в кислоті оцтової розведеної і розчині аміаку , розчинний в розведених мінеральних кислотах : Ca2+ + C2O4 2- → CaC2O4↓ d ) Сіль кальцію , змочена кислотою хлористоводневою , внесена до безбарвного полум'я забарвлює його в помаранчево-червоний колір. 3. Нефармакопейна реакція – з розчином феруму (ІІІ) хлориду утворює ясно-зелене забарвлення (реакція на глюконат-іони):  276. Зазначте причини забруднення оксафенаміду домішкою n-амінофенолу. Напишіть рівняння реакції виявлення цієї домішки. Відповідь: n-амінофенол використовується у процесі добування оксафенаміду: реагують фенілсаліцилат та п-амінофенол, тому у якості домішки він є в оксафенаміді. Виявлення цієї домішки: в лужному середовищі з резорционом – з’являється червоно-фіолетове забарвлення: 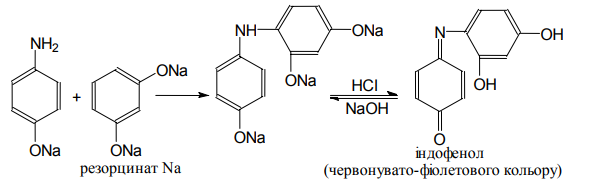 У процесі реакції утворюється натрію індофенолят синього кольору, який окиснюється киснем повітря до індофенолу червоного кольору. 156. Охарактеризуйте аргентометричний метод (по Фольгарду) кількісного визначення йодоформу. Наведіть рівняння реакцій, формулу розрахунку кількісного вмісту, зазначте молярну масу еквіваленту. Відповідь: Аргентометрія, зворотне титрування за методом Фольгарда. Спирто-водний розчин йодоформу нагрівають з титрованим розчином арґентуму нітрату в присутності кислоти нітратної. Надлишок арґентуму нітрату відтитровують розчином амонію тіоціанату, індикатор – феруму (ІІІ) амонію сульфат: 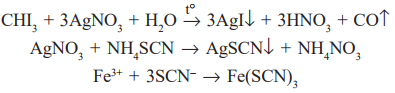 Паралельно проводять контрольний дослід. Мекв(CHI3)= 1/3 М.М. = 393,73/3 = 131,24 г / моль 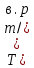 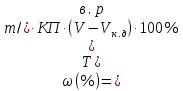 287. Охарактеризуйте лікарський засіб натрію бензоат згідно Державної Фармакопеї України. Наведіть повний фармакопейний аналіз: ідентифікація кількісне визначення, випробування на чистоту (в тому числі визначення специфічних домішок) та ін. Де це можливо, приведіть рівняння реакцій. Відповідь: Ідентифікація: 1. Субстанція дає реакції на бензоати Характерна реакція з феруму (ІІІ) хлоридом. При додаванні розчину феруму (ІІІ) хлориду випадає жовто-рожевий осад основного феруму (ІІІ) бензоату: 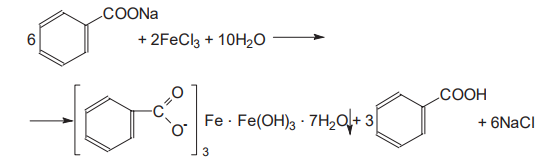 2. Субстанція дає реакцію на натрій Натрій ідентифікують за реакціями: а) з розчином калію піроантимонату (калію гексагідроксостибіату (V)) – утворюється білий осад: Na+ + [Sb(OH)6]- → Na[Sb(OH)6]↓ б) з розчином реактиву метоксифенілоцтової кислоти – утворюється об’ємний білий кристалічний осад: 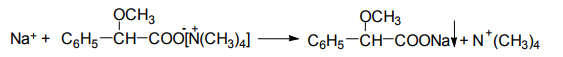 Осад розчиняється при додаванні розчину амоніаку розведеного і не випадає знову при наступному додаванні розчину амонію карбонату. в) сіль натрію, змочена кислотою хлористоводневою розведеною і внесена в безбарвне полум’я, забарвлює його у жовтий колір. Кількісне визначення: 1. Ацидиметрія в неводному середовищі, пряме титрування, індикатор – нафтолбензеїн: 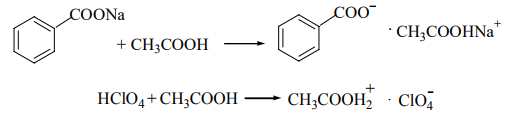 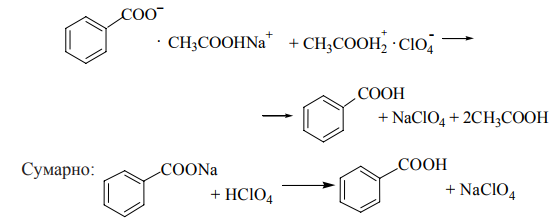 264. Охарактеризуйте можливі методи кількісного визначення ксикаїну. Приведіть рівняння реакцій, формули розрахунку кількісного вмісту, зазначте молярні маси еквівалентів. Відповідь: Кількісне визначення: 1. Ацидиметрія. Метод неводного титрування в середовищі протогенного розчинника - суміші мурашиної кислоти та оцтового ангідриду (1:20). Розчинник – мурашина кислота Середа – оцтовий ангідрид Титрант – хлорна кислота Індикатор - судан III Титрують до блакитно-зеленого фарбування розчину Метод заснований на властивості протогенного розчинника протонувати слабку органічну основу (по третинній аліфатичній аміногрупі), посилюючи його основні властивості, та на властивості протегенного розчинника віднімати протон від титранта. 1) При розчиненні препарату в мурашиній кислоті з додаванням оцтового ангідриду 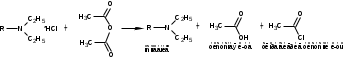 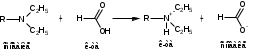 форміат-йон 2) в титранті HClO4 + CH3COOH → ClO4- + CH3COOH2+ кислота основа основа кислота 3) в процесі титрування реакція регенерації розчинника 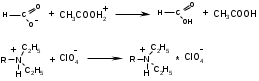 fекв. = 1 Е= М.м. = 288,8 г/моль 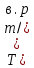 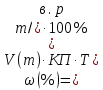 або ацидиметрія у присутності ртуті ацетату: 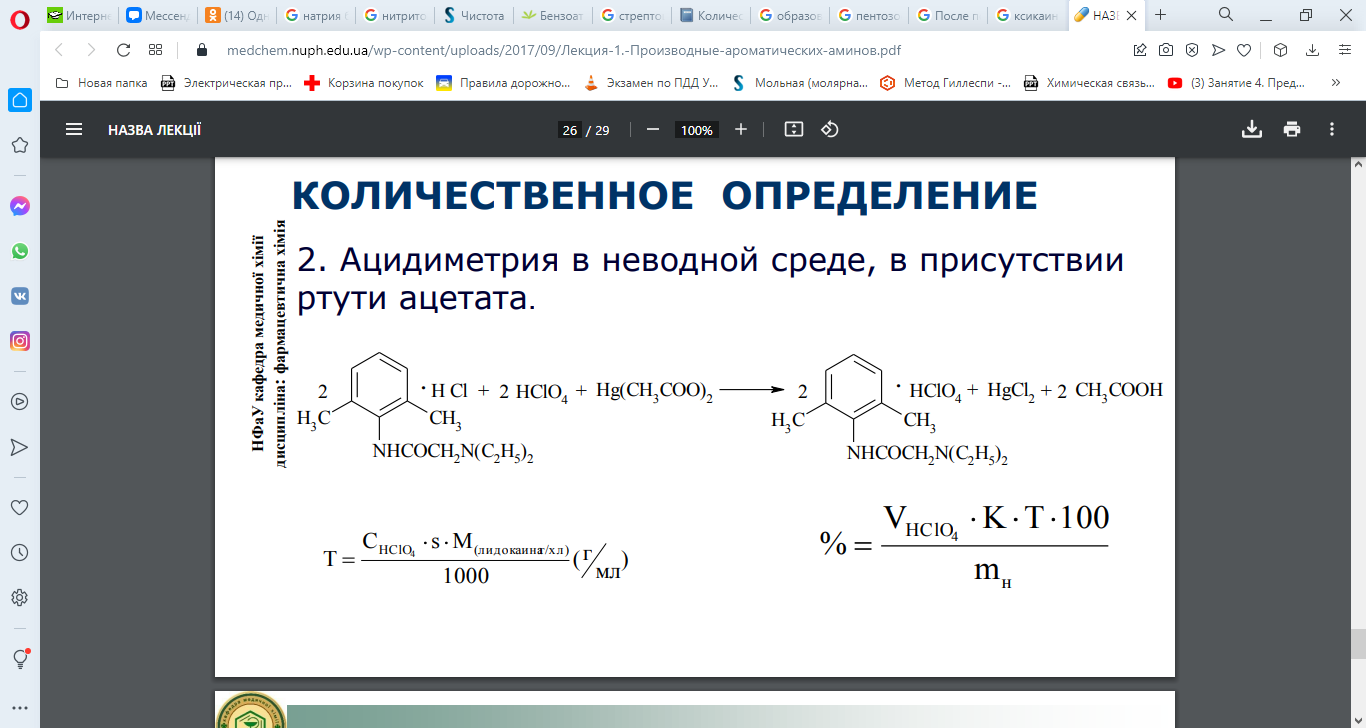 Е= М.м. 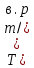 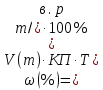 2. Алкаліметричний метод (варіант витіснення), за пов'язаною хлороводневою кислотою. Середовище – спирто-хлороформна суміш. Індикатор – фенолфталеїн. R•HCI + NaOH → R↓ + NaCl + Н2О заснування fекв. (речовин) = 1 Визначення ведуть у присутності органічного розчинника для вилучення основи, що виділяється. Е= М.м. 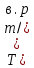 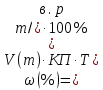 3. Аргентометричний метод, варіант Фаянсу, заснований на осадженні хлоридів нітратом срібла. Індикатор - бромфеноловий синій, середовище - оцтовокисле. R•HCI + АgNО3 → R•НNО3↓ + AgCI↓ fекв (речовин) = 1 4. Нітритометрія після кислотного гідролізу, з контролем  Е= М.м. 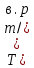 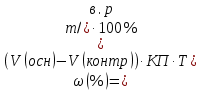 326. Охарактеризуйте нітритометричний метод кількісного визначення стрептоциду. Приведіть рівняння реакцій, формулу розрахунку кількісного вмісту, зазначте молярну масу еквіваленту. Відповідь: 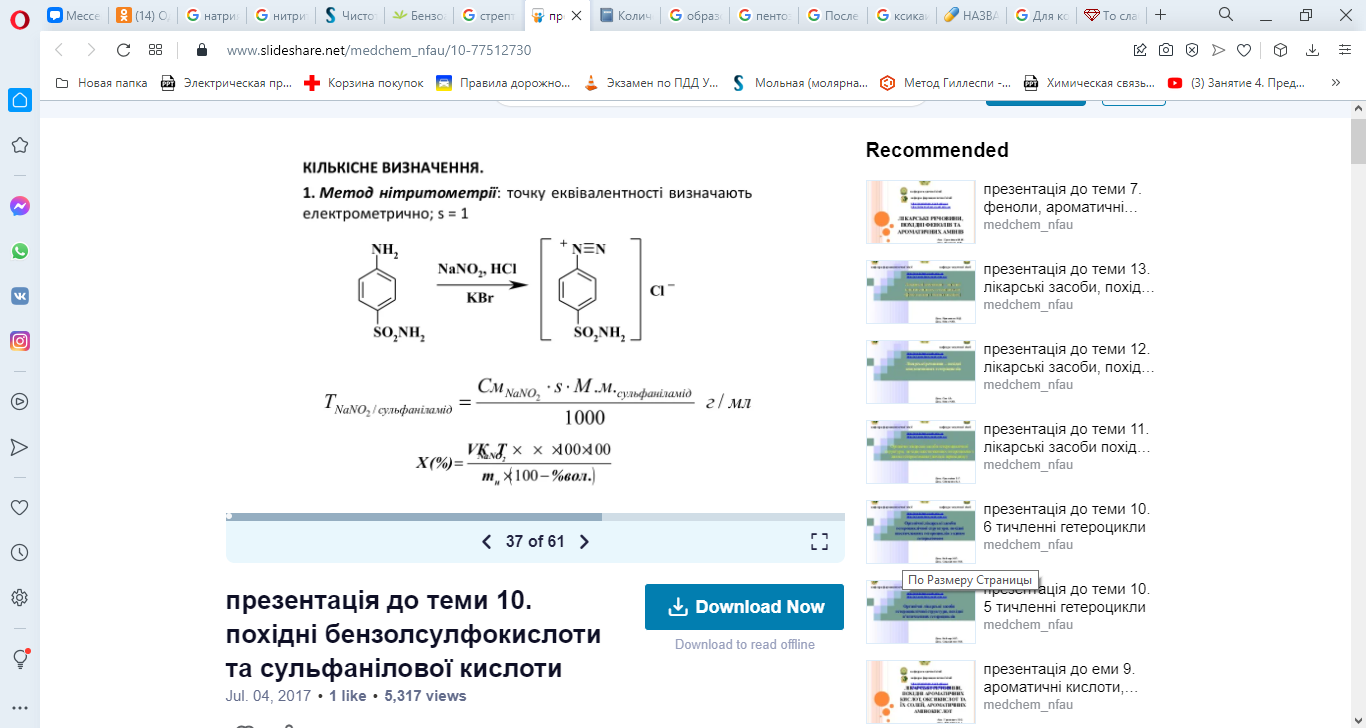 Е (стрептоцид)= Мм = 172,20 г/моль 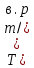 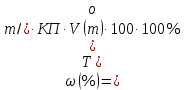 200. Охарактеризуйте лікарській засіб треонін згідно Державної Фармакопеї України. Наведіть повний фармакопейний аналіз: ідентифікація кількісне визначення, випробування на чистоту (в тому числі і визначення специфічних домішок). Де це можливо, напишіть рівняння реакцій. Відповідь:    Хлориди: Білий сирнистий Сульфати: білий Солі амонію: Лакмусовий папір синій Свинець: Жовтий Жовтий Залізо: Синій синій червоний Кількісне визначення: ацидиметрія. Метод неводного титрування в середовищі протогенного розчинника - суміші мурашиної кислоти та кислоти ацтової. Титрант - хлорна кислота; потенціометрично.   безв. НСООН безв. 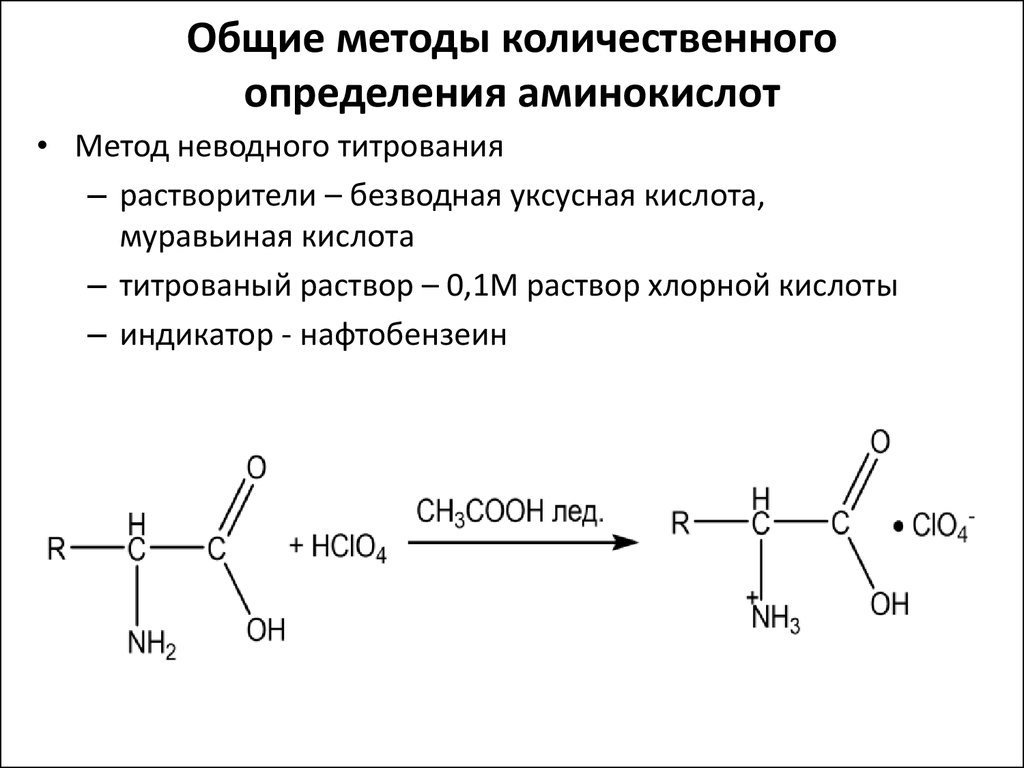 Е= М.м. = 119,1 г/моль 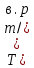 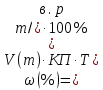 298. Приведіть рівняння можливих реакцій визначення якості анестезину. Де це можливо, приведіть рівняння хімічних реакцій. Відповідь: 1. Реакція на первинну ароматичну аміногрупу: 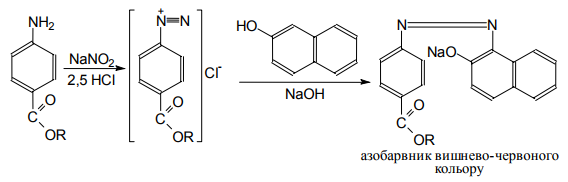 2. У результаті лужного гідролізу утворюється етанол, який можна виявити за йодоформною пробою: 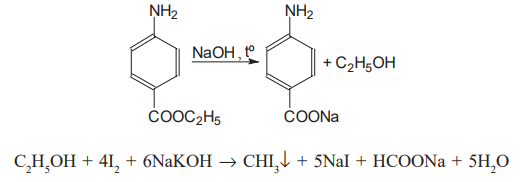 3. При окисненні лікарської речовини розчином хлораміну в присутності кислоти хлористоводневої та ефіру – ефірний шар забарвлюється в оранжевий колір. 4. Реакція з ароматичними альдегідами: 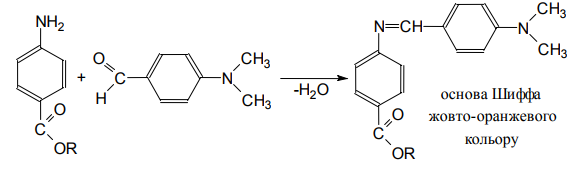 310. Приведіть схему синтезу стрептоциду із ацетаніліду з вказівкою хімічних назв вихідних, проміжних і кінцевого продуктів; вкажіть його фармакологічну дія. Приведіть рівняння можливих реакцій визначення якості. Відповідь:    п-ацетамінобензолсульфохлорид Хлорсульфонова кислота ацетанілід 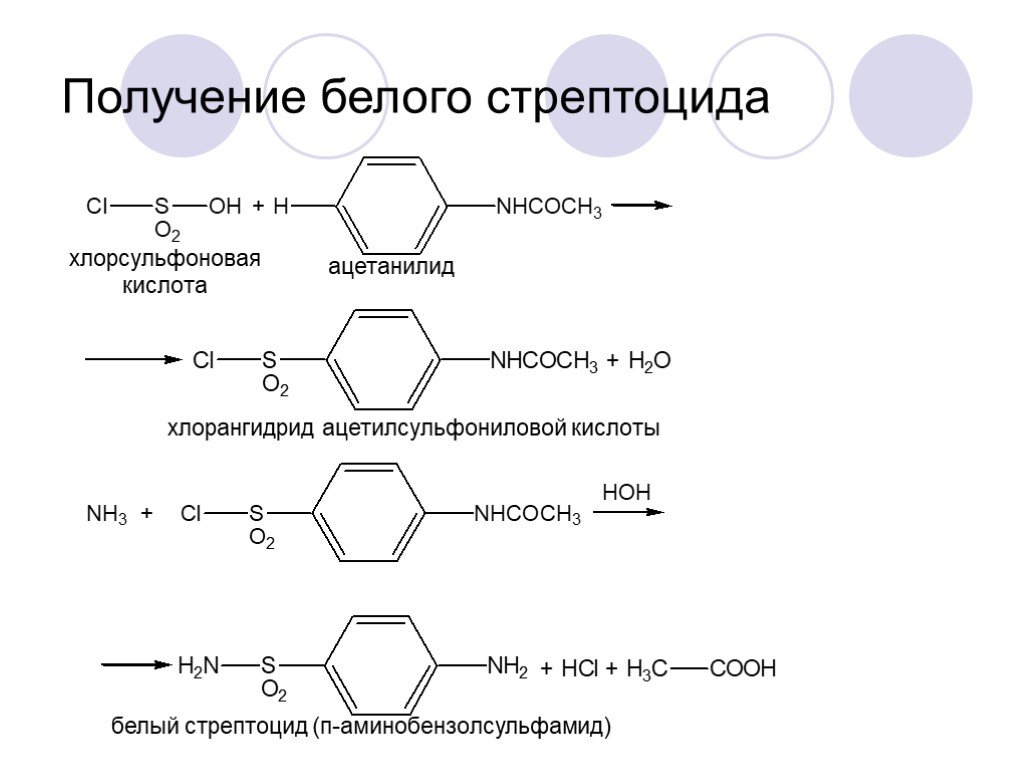 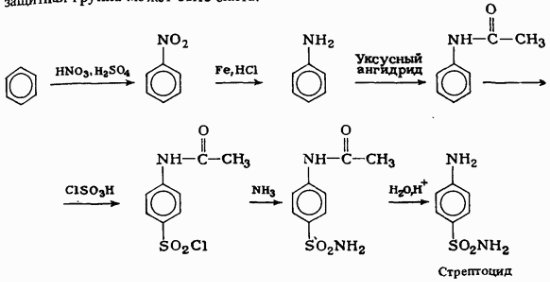 п-ацетамінобензолсульфамід Застосування. Для лікування ангіни, бешихи та інших кокових інфекцій. Ідентифікація: 1. При нагріванні з гідроксидом натрію відчувається запах амоніаку: 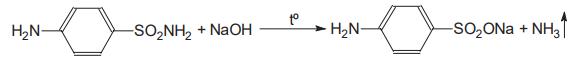 2. Лікарська речовина дає реакції на первинну ароматичну аміногрупу. 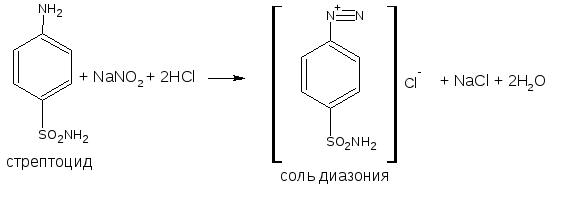    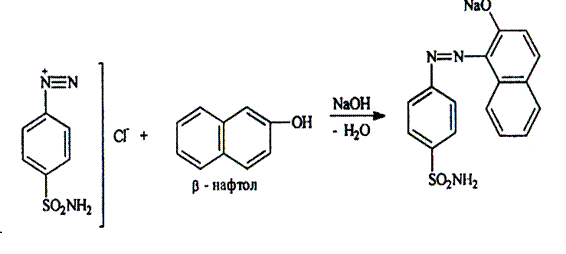 Азофарбник 3. Плав синьо-фіолетового кольору, відчувається запах аніліну і амоніаку. 4. При дії окисників (гідрогену пероксиду і феруму (ІІІ) хлориду) з’являється червоно-фіолетове забарвлення. 166. Запропонуйте можливі методи ідентифікації спирту етилового. Де це можливо, приведіть рівняння хімічних реакцій. Відповідь: Ідентифікація: За допомогою фізичних констант (температури кипіння, відносної густини), методом ІЧ-спектроскопії та за результатами хімічних реакцій: 1. При окисненні етанолу калію перманганатом у присутності кислоти сульфатної розведеної утворюється ацетальдегід, який має характерний запах. Якщо пробірку з реакційною сумішшю накрити фільтрувальним папером, змоченим розчином натрію нітропрусиду і піперазину гідрату, на папері з’являється інтенсивне блакитне забарвлення (реакція на ацетальдегід).  2. Йодоформна проба: Утворюється жовтий осад з характерним запахом. 3. Нефармакопейна реакція – утворення етилацетату (характерний запах): 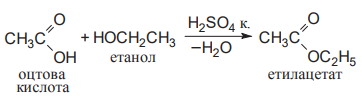 31. Розрахуйте, який об'єм 0,1 М розчину трилону Б (КП = 0,9998) буде витрачений на титрування 0,7422 г кальцію глюконату (М.м. 448,4), якщо його відсотковий вміст у субстанції - 99,7 %. Відповідь: Комплексонометрія -пряме титрування в присутності натрію гідроксиду, індикатор – кальконкарбонова кислота: 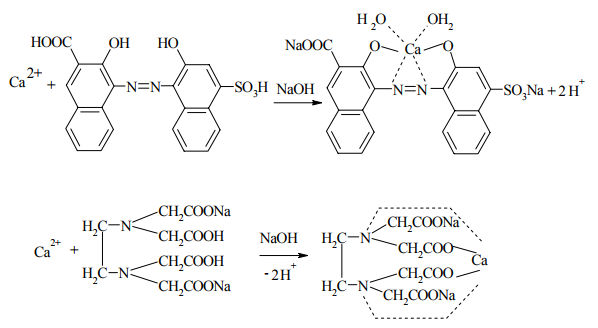 Титрують натрію едетатом до переходу фіолетового забарвлення в синє: 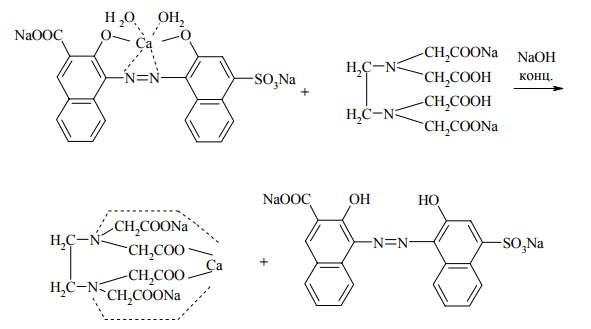 Е(в.р.) = М.м. = 448,4 г/моль  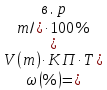 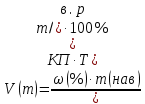 58. Розрахуйте відсотковий вміст аскорбінової кислоти (М.м. 176,13), якщо на титрування 0,2530 г препарату витрачено 14,00 мл 0,1 М розчину натрію гідроксиду (КП=1,0030). Відповідь: Алкаліметрія, пряме титрування, індикатор – фенолфталеїн: 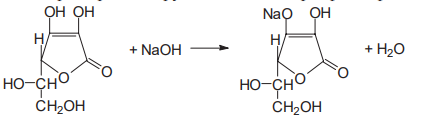 Е(в.р.) = М.м. = 176,13 г/моль 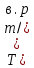 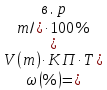 |
