электротехника и электроника лабораторная 1. Лабораторная работа №1. Федеральное государстенное бюджетное образовательное учреждение высшего образования
 Скачать 475.86 Kb. Скачать 475.86 Kb.
|
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСТЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ МОРДОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ИМ. Н.П. ОГАРЁВА» Институт физики и химии Кафедра органической химии ОТЧЕТ О ЛАБОРАТОРНОЙ РАБОТЕ № 1 по органической химии Химические свойства углеводородов Автор лабораторной работы _________ ________ М. А. Симакова (подпись) (дата) (ФИО) Обозначение лабораторной работы ЛР–02069964–19.03.01–01–21 Направление подготовки 19.03.01 Биотехнология Преподаватель _________ ________ А. Ш. Козлов (подпись) (дата) (ФИО) Саранск 2021 Лабораторная работа № 1 Химические свойства углеводородов 1. Цель и задачи лабораторной работы 1.1. Цель лабораторной работы Изучение химических свойств углеводородов. 1.2. Задачи лабораторной работы - На примере качественных химических реакций экспериментальным путем показать различие в химических свойствах основных классов углеводородов. - Дать теоретическое объяснение наблюдаемым экспериментальным результатам выполняемых реакций. 2. Список используемой литературы 1. Иванов В.Г. Органическая химия / В.Г. Иванов, В.А. Горленко, О.Н. Гева. – М.: Академия, 2012. – 624 с. 2 Грандберг И.И. Органическая химия / И.И. Грандберг, Н.Л. Нам. М.: Дрофа, 2015. 607 с. 3 Грандберг И.И. Практические работы и семинарские занятия по органической химии / И.И. Грандберг, Н.Л. Нам. М.: Издательство Юрайт, 2012. 350 с. 4 Болушева И.Ю. Лабораторный практикум по органической химии / И.Ю. Болушева, В.А. Васин. – Саранск: Мордов. гос. пед. ин-т, 2016. – 25 с. 3. Отчет о выполнении лабораторной работы 3.1. Бромирование и окисление ненасыщенных соединений 3.1.1 Описание выполнения эксперимента В одну пробирку поместила 1 каплю 2%-ного раствора перманганата калия, во вторую – 1 каплю бромной воды, добавила в каждую из них по 5 капель воды и 1 каплю скипидара и встряхнула. Наблюдала происходящие изменения. Результаты эксперимента занесла в таблицу 3.1.1. Таблица 3.1.1 – Результаты выполнения эксперимента по изучению бромирования и окисления ненасыщенных соединений
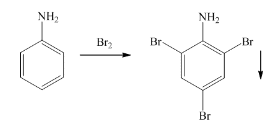
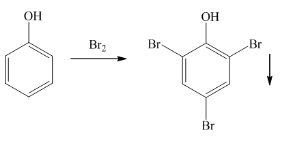
2.2. Бромирование анилина и фенола 2.2.1 Описание выполнения эксперимента В одну пробирку поместила 1 каплю анилина, во вторую – кристаллик фенола. Прилила в каждую по 1 мл воды, встряхнула содержимое и добавила по каплям бромную воду. Наблюдала происходящие изменения. Результаты занесла в таблицу 2.2.1. Таблица 2.2.1 – Результаты выполнения эксперимента по изучению бромирования анилина и фенола
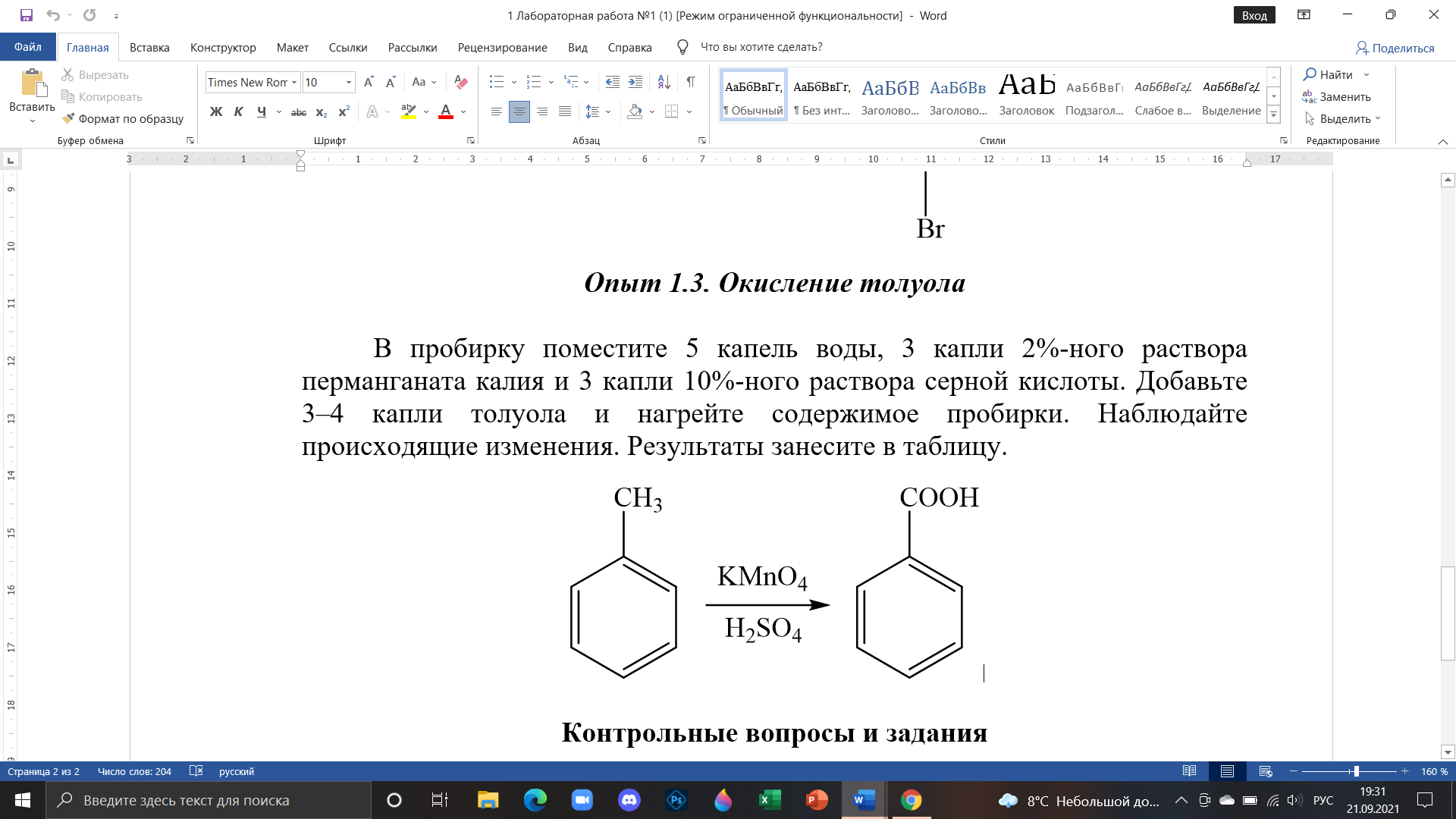
3.3. Окисление толуола 3.3.1. Описание выполнения эксперимента В пробирку поместила 5 капель воды, 3 капли 2%-ного раствора перманганата калия и 3 капли 10%-ного раствора серной кислоты. Добавила 3–4 капли толуола и нагрела содержимое пробирки. Наблюдала происходящие изменения. Результаты занесла в таблицу 3.3.1. Таблица 3.3.1. – Результаты выполнения эксперимента по изучению окисления толуола
4. Ответы на контрольные вопросы 1. Почему реакцию бромирования используют для обнаружения кратной связи в органических соединениях? 2. Приведите реакции окисления этилена перманганатом калия в нейтральной и кислой среде. 3. С помощью каких качественных реакций можно различить пропан, пропен и пропин? 4. Напишите уравнения реакций окисления п-диэтилбензола. 5. Сравните реакционную способность фенола, бензойной кислоты и бензола в реакциях электрофильного замещения. 6. Приведите уравнения реакций горения этана, этилена и ацетилена. |