ЛЕКЦИЯ Структурная организация дыхательной цепи. Главные функции окислительных процессов
 Скачать 2.29 Mb. Скачать 2.29 Mb.
|
|
Биологическое окисление – совокупность реакций окисления субстратов в живых клетках, основная функция которых – энергетическое обеспечение метаболизма. Главные функции окислительных процессов: 1) запас энергии в утилизируемой форме, 2) рассеяние энергии в виде теплоты, 3) образование полезных соединений, 4 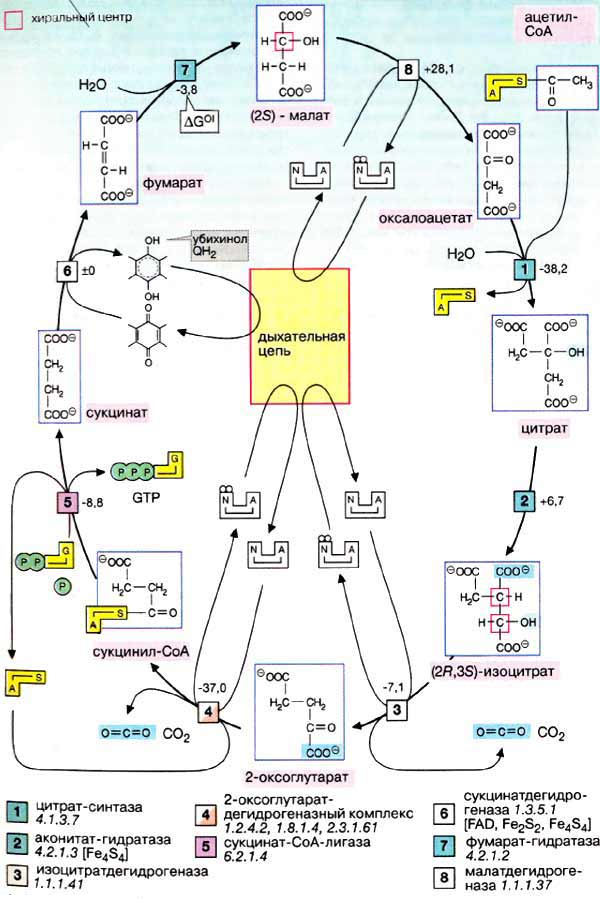 ) расщепление вредных веществ. ) расщепление вредных веществ.Различия между биологическим окислением и горением
История развития учения о биологическое окислении. Оксидазная теория А. Н. Баха
а) оксигеназа + О2 оксигеназа + перекись б) оксигеназа + субстрат оксигеназа + окисленный субстрат. Теория В. И. Палладина
Сущность окисления
акцепторы электрона или окислители.
Fe + ē Fe окислитель, восстановитель, акцептор донор Каждая редокс-пара характеризуется стандартным потенциалом ( в вольтах) Редокс-потенциал
Тканевое дыхание – вид биологического окисления, при котором акцептором электрона является кислород Субстраты тканевого дыхания:
Осуществляется тканевое дыхание с помощью ферментов дыхательной цепи. Схема превращения энергии в живых клетках: тканевое дыхание, образование АТФ и пути его использования. 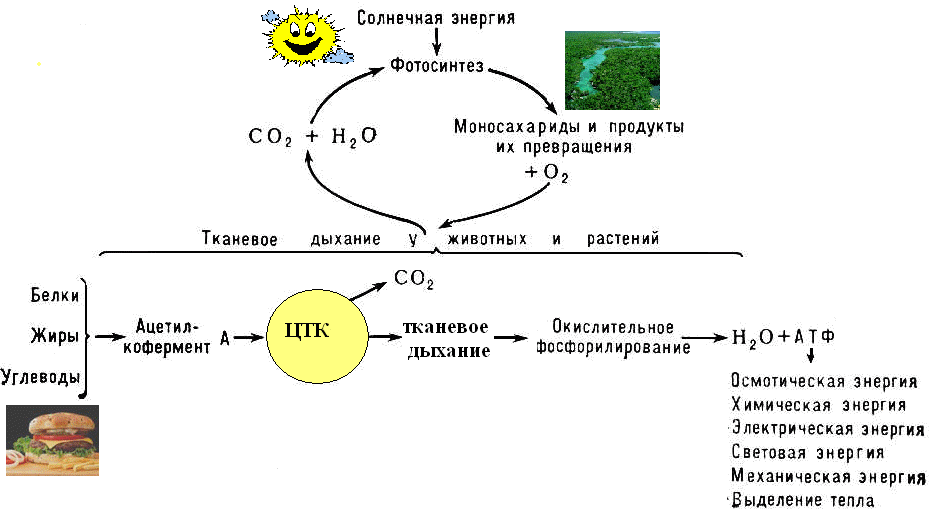 С 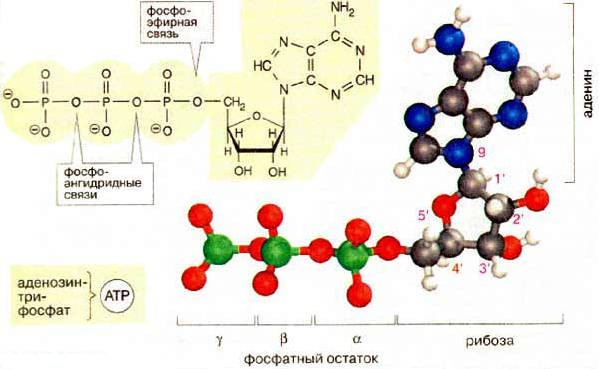 труктура АТФ труктура АТФСпособы синтеза АТФ 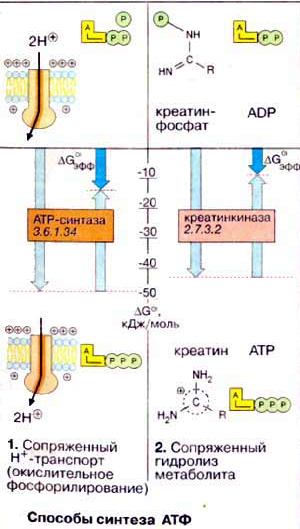 Дыхательная цепь – последовательность оксидоредуктаз во внутренней мембране митохондрий, осуществляющих перенос электронов и протонов от субстрата на молекулярный кислород. 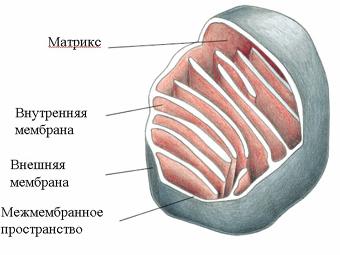 Митохондрия Перенос электронов и протонов с участием промежуточных переносчиков. 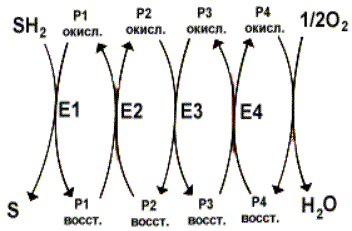 SH2 - исходный донор протонов и электронов; P1, Р2, Р3, Р4 - промежуточные переносчики; E1, E2, E3, E4 - ферменты окислительно-восстановительных реакций
Компоненты дыхательной цепи 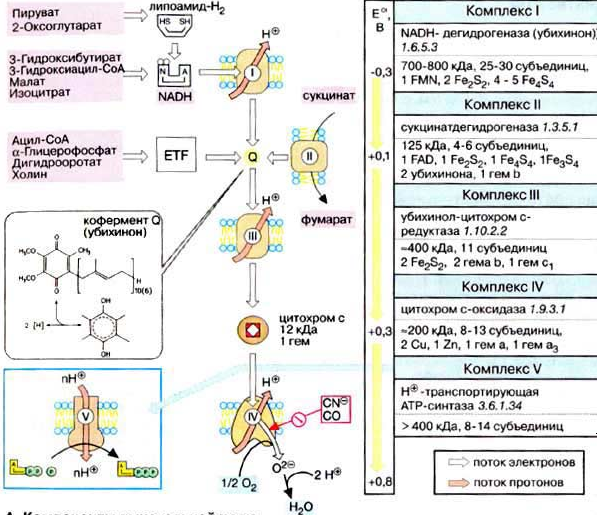 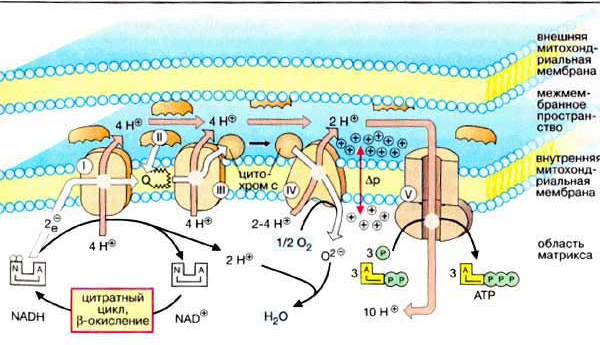 Водород в дыхательную цепь постыпает в виде в виде НАДН2, так как большинство дегидрогеназ внутри митохондрий НАД-зависимые, а также при действии на субстратфлавиновой дегидрогеназы (кофермент ФАД). НАД-зависимые дегидрогеназы
S -HH +НАД+ S +НАДН+Н+
Челночные механизмы переносят восстановленные нуклеотиды (НАДН+Н ) из цитоплазмы в митохондрии/
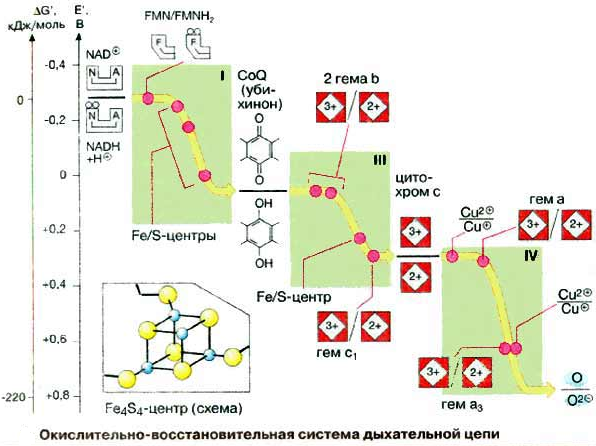 Окислительно-восстано-вительная система дыхательной цепи Д 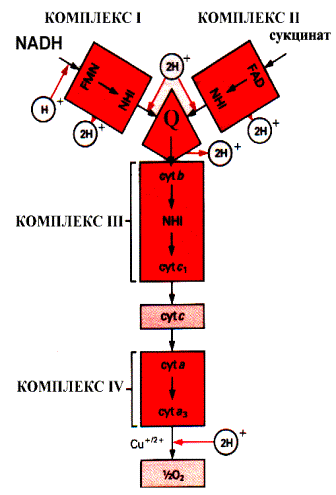 ыхательная цепь включает 4 ферментных комплекса, катализирующих окисление НАДН+Н кислородом. ыхательная цепь включает 4 ферментных комплекса, катализирующих окисление НАДН+Н кислородом.НАДН-KoQ-редуктаза катализирует перенос электронов от НАДН к KoQ. Этот комплекс включает в себя:
НАДН-дегидрогеназа
ФМН + НАДН+Н ФМНН2 +НАД В FeS – белках железо связано с остатком серы. Сукцинат-KoQ-редуктаза катализирует перенос электронов от сукцината к KoQ Этот комплекс включает в себя:
СДГ- флавопротеин, прочно связан с внутренней мембраной митохондрий. Коферментом является ФАД. KoQ (убихинон)
KoQ + ФМНН2 KoQН2 + ФМН Убихинон – коллектор, так как собирает восстановленные эквиваленты не только от НАДН-ДГ, но и от СДГ и других компонентов. KoQН2 – цитохром С–редуктаза катализирует перенос электронов от KoQН2 к цитохрому Комплекс включает в себя:
Цитохромы – сложные железосодержащие белки, окрашенные в красный цвет. Кофермент аналогичен гему, но железо в цитохромах меняет валентность. Впервые описаны Мак-Мунном, изучены Кейлиным. Цитохромы переносят электроны. Известны 25-30 различных цитохромов, которые отличаются:
П 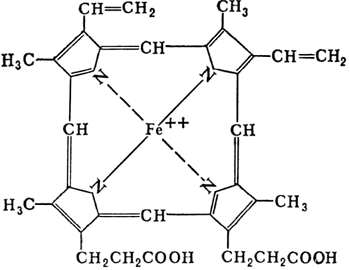 ростетическая группа гема в структуре цитохромов. ростетическая группа гема в структуре цитохромов.Связывание гема с белковой частью цитохрома С 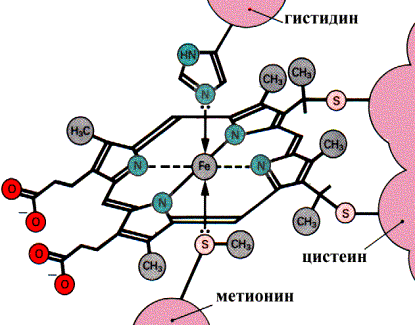 Цитохромоксидаза катализирует перенос электронов от цитохрома С к кислороду. Комплекс включает в себя:
Цитохромоксидаза отличается от других цитохромов:
В этом ферменте 4 редокс-центра: Цитохром С СuА гем А гем а3 СuВ О2 Сu + е Сu При транспорте одного электрона происходит перенос двух ионов водорода, один из которых используется при восстановлении кислорода до воды, а другой пересекает мембрану. Кислород, поступающий в митохондрии из крови, связывается с атомом железа в геме цитохрома а. Затем каждый из атомов молекулы кислорода присоединяет по 2 электрона и по 2 протона, превращаясь в молекулу воды. Протоны поступают из водной среды. 4ē + 4Н + О2 2Н20 200 – 400 мл воды синтезируется в сутки – эндогенная вода.
Нарушения в работе дыхательной цепи Состояние фатальной детской митохондриальной миопатии и дисфункции почек. Связано со снижением активности или полным отсутствием большинства оксидоредуктаз дыхательной цепи. Порядок распределения ферментов в дыхательной цепи определяется редокс-потенциалом.
Укороченные цепи
Ингибиторы дыхания
Каскадное выделение энергии в дыхательной цепи
Различают 2 типа дыхательных цепей:
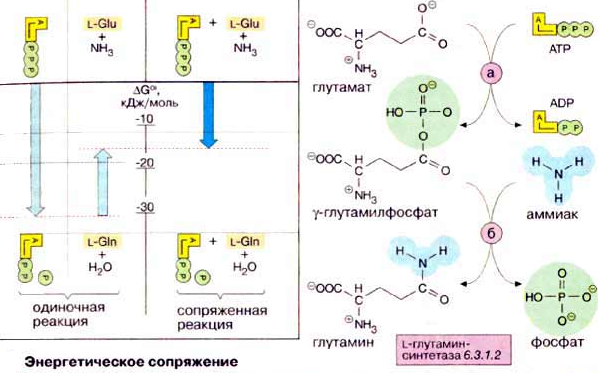 Тканевое дыхание включает:
Перенос электронов сопровождается уменьшением свободной энергии. Часть энергии рассеивается в виде тепла, а 40% используется на синтез АТФ. |
