ГУАП. Химия. 1 семестр. ответ на вопрос по экзамену. Химия. Химическая связь
 Скачать 17.89 Kb. Скачать 17.89 Kb.
|
|
Вопрос 1. Химическая связь — это взаимодействие атомов, обусловливающее устойчивость молекулы или кристалла как целого. Химическая связь определяется взаимодействием между заряженными частицами (ядрами и электронами). Современное описание химической связи проводится на основе квантовой механики. Основные характеристики химической связи — прочность, длина, полярность, устойчивость. Метод валентных связей (локализованных электронных пар) предполагает, что каждая пара атомов в молекуле удерживается вместе при помощи одной или нескольких общих электронных пар. Поэтому химическая связь представляется двухэлектронной и двухцентровой, т.е. локализована между двумя атомами. В структурных формулах соединений обозначается черточкой: H-Cl, H-H, H-O-H Валентность атома — определяется числом неспаренных (валентных) электронов, способных принять участие в образовании химической связи. Валентность выражается небольшими целыми числами и равна числу ковалентных связей. Валентность элементов, проявляющуюся в ковалентных соединениях, часто называют ковалентностью. Возбуждение атома до нового валентного состояния требует затраты энергии, которая компенсируется выделяемой при образовании связей энергией. Взаимное перекрывание облаков, т.е. образование связи может происходить разными способами, ввиду их различной формы. Различают σ-, π- и δ-связи. Сигма – связи образуются при перекрывании облаков вдоль линии, проходящей через ядра атомов. Пи – связи возникают при перекрывании облаков по обе стороны от линии, соединяющей ядра атомов. Дельта – связи осуществляются при перекрывании всех четырех лопастей d – электронных облаков, расположенных в параллельных плоскостях. Существует всего 6 видов связей: Металлическая связь Ковалентная связь Ионная связь Ван-дер-ваальсова связь Водородная связь Двухэлектронная трёхцентровая химическая связь Полярность химических связей — характеристика химической связи (как правило, ковалентной), показывающая изменение распределения электронной плотности в пространстве вокруг ядер в сравнении с распределением электронной плотности в образующих данную связь нейтральных атомах. Полярность молекул. Молекулы, которые образованы атомами одного и того же элемента, как правило, будут неполярными, как неполярны и сами связи в них. Молекулы, которые образованы атомами разных элементов, могут быть полярными и неполярными. Это зависит от геометрической формы. Если форма симметрична, то молекула неполярна, если асимметрична (из-за наличия неподелённых пар или неспаренных электронов), то молекула полярна. Вопрос 2. Тепловой эффект реакции — это энергия, которая выделяется или поглощается, когда химические вещества претерпевают превращения в процессе химической реакции. Этот параметр отражает изменение содержания энергии при превращении реактивов в продукты. Реакция может быть экзотермической (с выделением тепла) или эндотермической (с поглощением тепла); большинство реакций в химической и фармацевтической промышленности являются экзотермическими. Тепловой эффект реакции — одна из термодинамических характеристик, важных для разработки химических процессов, их безопасного масштабирования и переноса из лабораторных условий в производственные. Тепловой эффект реакции (или энтальпия) обычно выражается в единицах молярной энтальпии (кДж/моль) или удельной энтальпии (кДж/кг или кДж/л). Закон Гесса гласит - количество теплоты, выделяющееся или поглощающееся при каком-либо процессе (при p,T = const или V,T = const), всегда одно и то же, независимо от того, протекает ли данное химическое превращение в одну или в несколько стадий (при условии, что температура, давление и агрегатные состояния веществ одинаковы). Следствия из закона Гесса: Тепловой эффект прямой реакции равен по величине и противоположен по знаку тепловому эффекту обратной реакции (закон Лавуазье — Лапласа). Тепловой эффект химической реакции равен разности сумм теплот образования (ΔHf) продуктов реакции и исходных веществ, умноженных на стехиометрические коэффициенты (ν). Тепловой эффект химической реакции равен разности сумм теплот сгорания (ΔHc) исходных веществ и продуктов реакции, умноженных на стехиометрические коэффициенты (ν). Если начальное и конечное состояния химической реакции (реакций) совпадают, то их тепловой эффект равен нулю. Энтропия 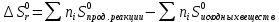 Тепловой эффект химической реакции 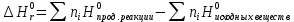 Энергия Гиббса 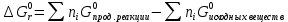 |
