расчетно графическая работа по физике механика. Юрлов Р.В. РГР2. Институт нефтепереработки и нефтехимии фгбоу во угнту в г. Салавате
 Скачать 40.06 Kb. Скачать 40.06 Kb.
|
|
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Федеральное государственное бюджетное образовательное учреждение высшего образования «Уфимский государственный нефтяной технический университет» (ФГБОУ ВО УГНТУ) Институт нефтепереработки и нефтехимии ФГБОУ ВО УГНТУ в г. Салавате Кафедра «Информационных технологий» Физика РАСЧЕТНО-ГРАФИЧЕСКАЯ РАБОТА Молекулярная физика. Термодинамика. ИнТех- 09.03.01 – 1.02.09 РГР Исполнитель: студент гр. БАБз - 22-21 Юрлов Р. В. Руководитель: ассистент Г.Ф. Шаяхметов Салават 2023 2.9. Определить относительную молекулярную массу  : : 1) воды, 2) углекислого газа, 3) поваренной соли. Дано:  Найти:  Решение. 1) Одна молекула  состоит из одного атома кислорода и двух атомов водорода. Молярная масса кислорода состоит из одного атома кислорода и двух атомов водорода. Молярная масса кислорода  , а водорода , а водорода  . Тогда молярная масса молекулы . Тогда молярная масса молекулы  Поэтому относительная молекулярная масса равна 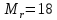 . .2) Одна молекула  состоит из одного атома углерода и двух атомов кислорода. Молярная масса углерода состоит из одного атома углерода и двух атомов кислорода. Молярная масса углерода  , а кислорода , а кислорода  . Тогда молярная масса молекулы . Тогда молярная масса молекулы  Поэтому относительная молекулярная масса равна  . .3) Одна молекула  состоит из одного атома натрия и одного атома хлора. Молярная масса натрия состоит из одного атома натрия и одного атома хлора. Молярная масса натрия  , а хлора , а хлора  . Тогда молярная масса молекулы . Тогда молярная масса молекулы  Поэтому относительная молекулярная масса равна  . .Ответ:  2.19. Определить плотность  водяного пара, находящегося под давлением водяного пара, находящегося под давлением 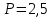 кПа и имеющего температуру кПа и имеющего температуру  = 250К. = 250К.Дано:_СИ'>Дано: 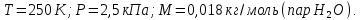 СИ:  Найти:  Решение. Воспользуемся уравнением Клапейрона – Менделеева, применив его к пару:  где 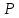 – давление пара, Па; – давление пара, Па; - объем, - объем, 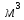 ; ; – температура газа, К; – температура газа, К; – молярная газовая постоянная (8,31Дж/(моль·К)). – молярная газовая постоянная (8,31Дж/(моль·К)).Откуда  . .Нам известно, что плотность 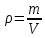 Поэтому  Проверим размерности расчетных формул  Подставляя числовые значения получим ответ  Ответ: 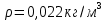 2.29. В азоте взвешены мельчайшие пылинки, которые движется так, как если бы они были очень крупными молекулами. Масса каждой пылинки равна 6  г. Газ находится при температуре г. Газ находится при температуре  = 400 К. Определить средние квадратичные скорости = 400 К. Определить средние квадратичные скорости 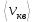 , а также средние кинетические энергии , а также средние кинетические энергии  поступательного движения молекулы азота. поступательного движения молекулы азота.Дано: 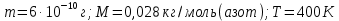 СИ:  Найти: 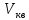 ; ;  . .Решение. По определению среднеквадратичная скорость  где  постоянная Больцмана (1,38 постоянная Больцмана (1,38 ; ; масса пылинки, кг. масса пылинки, кг.Поэтому скорость пылинки  С другой стороны среднеквадратичная скорость  где  ; ;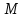 -молярная масса газа. -молярная масса газа.Поэтому скорость молекул азота  Средняя кинетическая энергия поступательного движения одной молекулы  Где  постоянная Больцмана (1,38 постоянная Больцмана (1,38 ; ;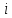  поступательные степени свободы молекулы (в нашем случае поступательные степени свободы молекулы (в нашем случае  , т.к. возможны три поступательных движения). , т.к. возможны три поступательных движения).Поэтому 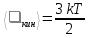 Средняя энергия поступательно движения пылинки равна  Видно, что средние кинетические энергии пылинки и молекул азота равны друг другу Проверим размерности расчетных формул  Подставляя числовые значения получим ответ  Дж ДжОтвет:_Дж1.39.'>Ответ: 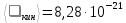 Дж Дж1.39. Одноатомный газ при нормальных условиях занимает объем  . Вычислить теплоемкость . Вычислить теплоемкость 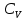 этого газа при постоянном объеме. этого газа при постоянном объеме.Дано:  СИ:  Найти: 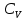 . .Решение. Изохорная теплоемкость равна  где   молекулярная масса газа, кг. молекулярная масса газа, кг.Воспользуемся уравнением Клапейрона – Менделеева:  где 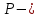 давление, Па; давление, Па; количество молей; количество молей; объем сосуда, объем сосуда, 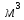  температура газа, К; температура газа, К;  . .Откуда  Поэтому  С другой стороны, молярная теплоемкость при постоянном объеме равна  где  число степеней свободы (в нашем случае число степеней свободы равно 3 (3 поступательные и ни одной вращательной, т.к. газ одноатомный)); число степеней свободы (в нашем случае число степеней свободы равно 3 (3 поступательные и ни одной вращательной, т.к. газ одноатомный)); . .тогда  Подставим 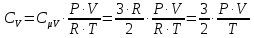 Проверим размерности расчетных формул  Подставляя числовые значения получим ответ  Дж/К Дж/КОтвет:  Дж/К Дж/К2.49. Определить количество теплоты  , которое надо сообщить кислороду объемом , которое надо сообщить кислороду объемом  л при его изохорном нагревании, чтобы давление газа повысилось на л при его изохорном нагревании, чтобы давление газа повысилось на  МПа. МПа.Дано:  л; л; 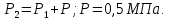 СИ: 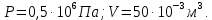 Найти:  Решение. Количество тепла  , необходимое для изохорного нагрева газа определяется: , необходимое для изохорного нагрева газа определяется: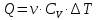 Где  количество молей газа; количество молей газа; молярная изохорная теплоемкость; молярная изохорная теплоемкость;Молярная изохорная теплоемкость вычисляется: 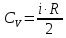 где  число степеней свободы газа (в нашем случае i=5, т.к. кислород – газ двухатомный (3 поступательные и 2 вращательные степени свободы) число степеней свободы газа (в нашем случае i=5, т.к. кислород – газ двухатомный (3 поступательные и 2 вращательные степени свободы)поэтому  Воспользуемся уравнением Клапейрона – Менделеева, применив его к газу:  где 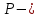 давление, Па; давление, Па; количество молей; количество молей; объем сосуда, объем сосуда,   температура газа, К; температура газа, К;  . .Тогда  , , . .Из второго вычитаем первое и получим:  Откуда 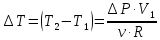 Подставим это в  Проверим размерности расчетных формул  Подставляя числовые значения получим ответ  Ответ:  2.59. Какая доля  количества теплоты количества теплоты  , подводимого к идеальному двухатомному газу при изобарном процессе, расходуется на увеличение внутренней энергии газа и какая доля , подводимого к идеальному двухатомному газу при изобарном процессе, расходуется на увеличение внутренней энергии газа и какая доля  - на работу - на работу  расширения? Рассмотреть три случая, если газ: расширения? Рассмотреть три случая, если газ: 1) одноатомный; 2) двухатомный; 3) трехатомный. Дано: 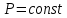 . .Найти: 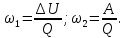 Решение. При изобарическом процессе количество затраченной энергии на нагрев азота:  где  масса газа, кг; масса газа, кг; молярная масса газа, (г/моль); молярная масса газа, (г/моль);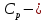 молярная изобарная теплоемкость газа; молярная изобарная теплоемкость газа;Молярная изобарная теплоемкость вычисляется по формуле 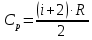 где   ; ; число степеней свободы молекулы: число степеней свободы молекулы:1) для одноатомного газа 3 поступательные  ; ;2) для двухатомного газа 3 поступательные и 2 вращательные 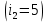 ; ;3) для трехатомного газа 3 поступательные и 3 вращательные  . .Поэтому 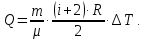 По определению изменение внутренней энергии газа равно  Где  Выражаем изменение внутренней энергии через 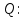  Молярная изохорная теплоемкость вычисляется по формуле 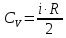 где  число степеней свободы молекулы. число степеней свободы молекулы.поэтому  Откуда искомое  Применим первый закон термодинамики, согласно которому количество теплоты  переданное системе, расходуется на увеличение внутренней энергии переданное системе, расходуется на увеличение внутренней энергии  и на внешнюю механическую работу и на внешнюю механическую работу  : : Откуда  Поэтому искомое  Подставляем числа 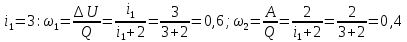 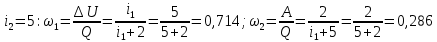 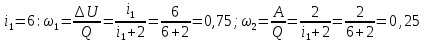 Ответ:  2.69. Газ, совершающий цикл Карно, получает теплоту 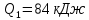 . Определить работу . Определить работу  газа, если температура газа, если температура  , теплоотдатчика в три раза выше температуры , теплоотдатчика в три раза выше температуры  теплоприемника. теплоприемника.Дано: 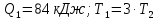 Найти:  Решение. Кпд тепловой машины равен отношению производимой силы  к количеству тепла к количеству тепла  полученному рабочим телом от нагревателя: полученному рабочим телом от нагревателя: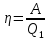 С другой стороны  где  температура нагревателя, температура нагревателя,  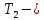 температура холодильника, температура холодильника,  Откуда  Поэтому работа равна  Проверим размерности расчетных формул  Подставляя числовые значения получим ответ  Ответ: 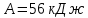 2.79. Воздушный пузырек диаметром  мкм находится в воде у самой ее поверхности. Определить плотность мкм находится в воде у самой ее поверхности. Определить плотность  воздуха в пузырьке, если воздух над поверхностью воды находится при нормальных условиях. воздуха в пузырьке, если воздух над поверхностью воды находится при нормальных условиях.Дано:  мкм; мкм; 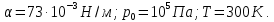 СИ:  Найти:  Решение. Так как поверхность жидкости в пузыре принимает выгнутую сферическую форму, то внутреннее давление 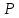 в пузыре будет больше, чем внешнее на величину избыточного давления под сферической поверхностью: в пузыре будет больше, чем внешнее на величину избыточного давления под сферической поверхностью: где  радиус кривизны пузыря; радиус кривизны пузыря;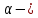 коэффициент поверхностного натяжения жидкости ( коэффициент поверхностного натяжения жидкости ( Так как  , то , то Тогда полное давление равно  где 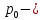 атмосферное давление, так как пузырек находится на поверхности воды. атмосферное давление, так как пузырек находится на поверхности воды.Воспользуемся уравнением Клапейрона – Менделеева, применив его к газу  где 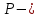 давление, Па; давление, Па; объем сосуда, объем сосуда, 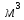  температура газа, К; температура газа, К;  . .Откуда  Известно, что плотность 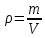 Поэтому  Проверим размерности расчетных формул 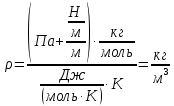 Подставляя числовые значения получим ответ 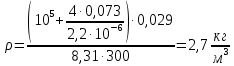 Ответ:  кг/ кг/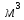 |
