Исследование термодинамических циклов
 Скачать 1.02 Mb. Скачать 1.02 Mb.
|
|
МИНОБРНАУКИ РОССИИ Санкт-Петербургский государственный электротехнический университет «ЛЭТИ» им. В.И. Ульянова (Ленина) Кафедра Физики отчет по лабораторной работе №10 по дисциплине «Физика» Тема: Исследование термодинамических циклов
Санкт-Петербург 2017 Цель работы. Исследование политропно-изохорно-изотермического (nVT) и адиабатно-изохорно-изотермического (SVT) циклов. Основные теоретические положения.         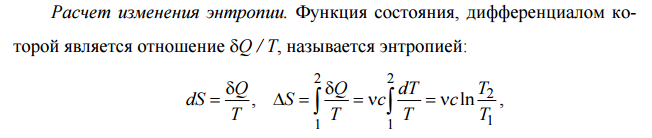   Обработка результатов эксперимента. а) Определение избыточных давлений Δp1 и Δp3 (прямые измерения): 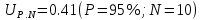 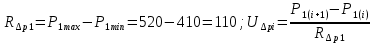 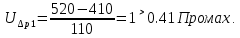 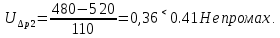 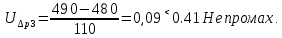 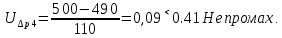 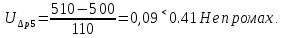 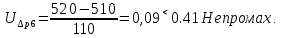 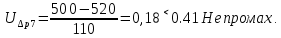 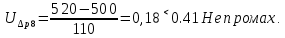 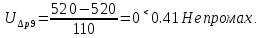 Есть промахи. N = 9; 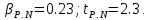 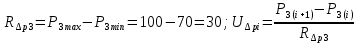 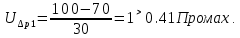 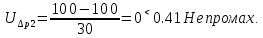 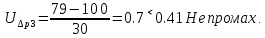 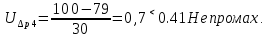 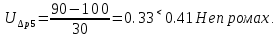 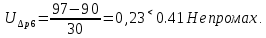 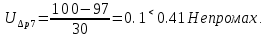 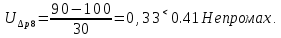 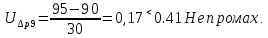 Есть промахи. N = 9; 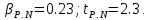 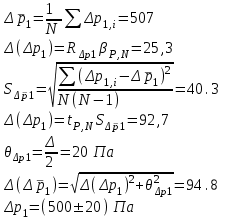 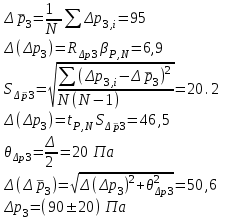 б) Определение показателя политропы n (перенос погрешностей.) 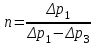 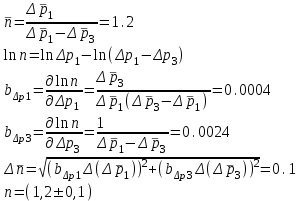 2. Определение параметров состояния (p, V, T) в точках 1, 2, 3, 1*, 2*, 3*. 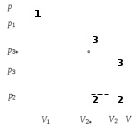 Cостояние 1 (совпадает с 1*): p1 = p2 + Δp1 = 102600 Па V1 = 22.4 л = 22.4∙10-3 м3 T1 = 297 K  Состояние 2*: p2* = p2 = 102100 Па Уравнение адиабаты: 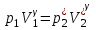 Газ двухатомный, i = 5. 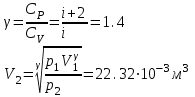 Уравнение состояния: 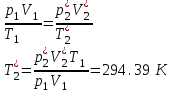 Cостояние 3*: T3* = T1 = 297 K Из уравнения изотермического процесса 1-3: 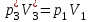 Процесс 2-3 изохорический, значит V3* = V2*. Тогда имеем 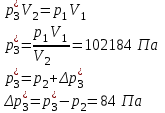 Уравнение состояния: 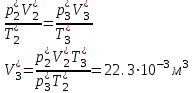 Состояние 2: p2 = 102100 Па Уравнение политропы: 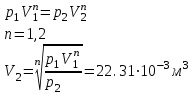 Уравнение состояния: 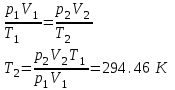 Cостояние 3: p3 = p2 + Δp3 = 102190 Па T3 = T1 = 297 K Уравнение состояния: 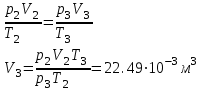 Графики циклов (начало координат сдвинуто): nVT (n = 1,2) 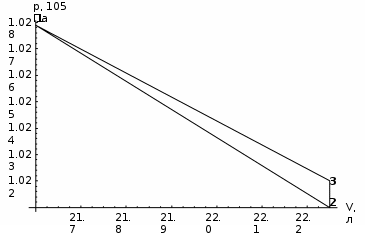 SVT (γ = 1,4) 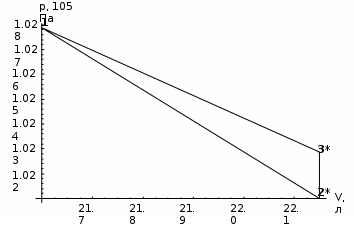 3. Расчет холодильных коэффициентов ε (вывод формул – стр. 3). Цикл nVT (1-2-3-1): 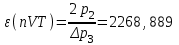 Цикл SVT (1-2*-3*-1): 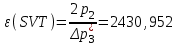 Так как Δp3* > Δp3, 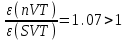 . .Обратный цикл Карно (идеальная холодильная машина): Для T1, T2: 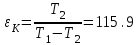 Для T1, T2*: 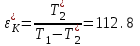 Так как T2* < T2, 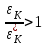 . .Холодильные коэффициенты циклов Карно меньше, чем холодильные коэффициенты рассматриваемых циклов в силу идеальности холодильной машины Карно. 4. Определение числа молей воздуха ν в сосуде (вывод формул – стр. 3). 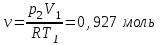 5. Изменение энтропии ΔS в циклах 1-2-3-1, 1-2*-3*-1 (вывод формул – стр. 4). Цикл nVT (1-2-3-1): Политропа 1-2 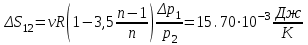 Изохора 2-3 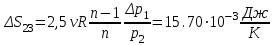 Изотерма 3-1 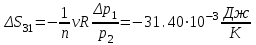 Изменение энтропии за цикл 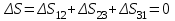 Цикл SVT (1-2*-3*-1): Адиабата 1-2* ΔS12 = 0 Изохора 2*-3* 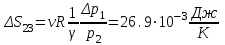 Изотерма 2*-3* 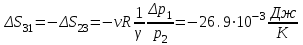 Изменение энтропии за цикл 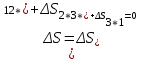 Итоговые результаты:
 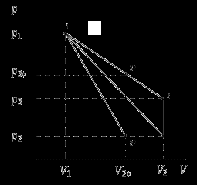
Выводы. Выполнив лабораторную работу, мы исследовали политропно-изохорно-изотермические (nVT) и адиабатно-изохорно-изотермические (SVT) циклы. По экспериментально измеренным величинам мы определили показатель политропного процесса n, нашли холодильные коэффициенты ε для nVT- и SVT-циклов. Были построены графики nVT- и SVT-циклов. Были вычислены параметры состояния (p,V,T). Итоговые результаты были вынесены в конец работы. Протокол по лабораторной работе №10 по дисциплине «Физика» Тема: Исследование термодинамических циклов Таблица 10.1
Таблица 10.2
Санкт-Петербург 2017 Дата: _______________ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

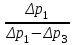 = (1.20.1)
= (1.20.1)