Теория горения и взрыва контрольная работа. ТГВ. Контрольная работа 1 по дисциплине Теория горения и взрыва Вариант 7 А. Т. Хузин Проверил Доцент, кандидат наук И. В. Озден
 Скачать 33.01 Kb. Скачать 33.01 Kb.
|
|
Министерство науки и высшего образования Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования «Уфимский государственный нефтяной технический университет» Кафедра «Пожарная и промышленная безопасность» Контрольная работа № 1 по дисциплине: «Теория горения и взрыва» Вариант № 7 Выполнил: А. Т. Хузин Проверил: Доцент, кандидат наук И. В. Озден УФА-2021 СОДЕРЖАНИЕ
Задание № 1 Рассчитать объем и массу окислительной среды, необходимые для горения i – го горючего вещества.
Решение. Запишем уравнение реакции горения дихлорбензола C6H4Cl2+6,5(О2+3,76N2)=6C О2+H2O+2HCl + 6,5  3,76N2 3,76N2Объем воздуха, необходимого для сгорания 1 кг дихлорбензола: 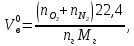 учитывая, что масса одного киломоля дихлорбензола составляет 58 кг, получим 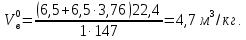 Действительный объем воздуха с учетом коэффициента избытка воздуха α=2 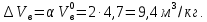 а избыток воздуха 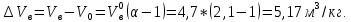 При сгорании 7 кг дихлорбензола объем воздуха при нормальных условиях составит: 9,4 м3/кг  7 кг =65,8 м3. 7 кг =65,8 м3.Масса воздуха: 65,8*1,292=85кг Задание № 2 Рассчитать объем образующихся продуктов (м3) при горении i – го горючего вещества.
Решение. Окислительная среда: 65/35=1,85 C6H5OH+7(О2+1,85N2)=6C О2+3H2O+ 7  1,85N2 1,85N2Условия отличаются от нормальных, следовательно 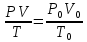 → →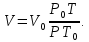 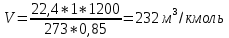 Объем воздуха, необходимого для сгорания 1 кг ацетона: 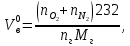 Учитывая, что масса одного киломоля фенола составляет 94 кг, получим 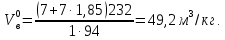 Действительный объем воздуха с учетом коэффициента избытка воздуха α=1,8 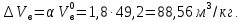 а избыток воздуха 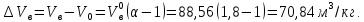 Объем продуктов горения 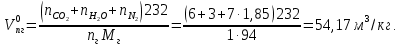 С учетом избытка воздуха полный объем продуктов горения 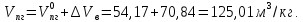 При сгорании 5 кг фенола объем воздуха при нормальных условиях составит: 88,56 м3/кг  5 кг =442,8 м3, а объем продуктов горения 125,01 м3/кг 5 кг =442,8 м3, а объем продуктов горения 125,01 м3/кг 5 кг =625,05 м3. 5 кг =625,05 м3.Задание №3 Задачи по расчету теплот сгорания веществ
Решение. Н-бутиловый спирт: С₄H₉OH Составляем уравнение реакции горения н-бутилового спирта в воздухе: С₄H₉OH + 6(О2+3,76N2)=4CО2+5H2O+ 6  3,76N2 3,76N2 Масса одного киломоля н-бутилового спирта составляет 74 кг, тогда доля С=64%, доля Н=13%, доля О=21% Низшую теплоту сгорания твердых и жидких горючих веществ можно определить по формуле Д. И. Менделеева: 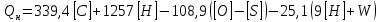 = =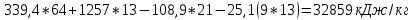 Низшая теплота сгорания н-бутилового спирта составляет 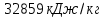 Задание №4 Рассчитать температуру горения i-го вещества
Решение. Для определения температуры горения необходимо знать низшую теплоту сгорания вещества Qн и объем продуктов горения. Для вещества сложного составa при определении Qн воспользуемся формулой Менделеева (23): 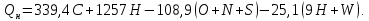 Подставляя численные значения C, H, N, S, получим: 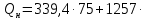 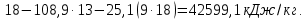 Найдем объем продуктов горения, воспользовавшись уравнениями (15)-(18): 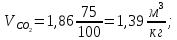 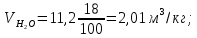 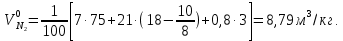 Так как горение происходит при избытке воздуха (α>1), то в продуктах горения будет еще и воздух, который не участвовал в горении: 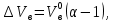 учитывая равенство (14), получим 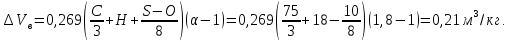 Температура горения из уравнения (28) 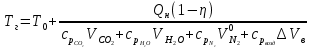 Так как в условии задачи не сказано о начальной температуре Т0, будем считать условия для горения нормальными. Так как размерность Qн кДж/кг, а Vпг в м3/кг, теплоемкость необходимо взять в кДж/(м3К) (см. табл. 4 приложения). Подставив численные значения, получим: 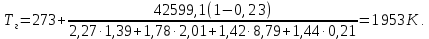 Температура горения вещества равна 1953 К. Список литературы 1. Корольченко, А.Я. Процессы горения и взрыва / А.Я. Корольченко. - М.: Изд-во «Пожнаука»,2007. 2. Корольченко, А.Я. Пожаровзрывобезопасность веществ и материалов и средства их тушения. В 2 ч./ А.Я. Корольченко, Д.А. Корольченко. - М.: Ассоциация «Пожнаука», 2004. 3. Демидов, П.Г. Горение и свойства горючих веществ/ П.Г.Демидов, В.А. Шандыбаж, П.П. Щеглов. - М.: Изд-во «Химия», 1981. 4. Тотай, А. В. Теория горения и взрыва: учебник и практикум для прикладного бакалавриата / А. В. Тотай, О. Г. Казаков. - М. :Изд-во Юрайт, 2016. 5. Карауш, С.А. Теория горения и взрыва: учебник / С.А. Карауш – М.: Изд-во «Академия», 2013. 6. Методические указания к выполнению контрольной работы. УГНТУ. |
