Контрольная работа 3 (20152016 уч гг.) Тест 1 (один вариант правильного ответа)
 Скачать 88 Kb. Скачать 88 Kb.
|
|
Контрольная работа № 3 (2015-2016 уч. гг.) Тест 1 (один вариант правильного ответа) Диеновые углеводороды 1. При взаимодействии 1 моль бутадиена-1,3 с 2 моль Вr2 образуется: а) 1,1,1,2-тетрабромбутан; б) 1,2,2,3-тетрабромбутан; в) 1,1,2,2-тетрабромбутан; г) 1,2,3,4-тетрабромбутан? 2. Бутадиен-1,3 можно получить при: а) крекинге бутана; б) термическом разложении метана (1500 °С); в) гидратации этина; г) высокотемпературном дегидрировании бутана в присутствии катализатора Сr2O3? 3. В молекуле бугадиена-1,3 каждый атом углерода образует: а) три σ- и одну π-связь; б) две σ- и две π-связи; в) одну σ-и две π-связи; г) одну σ- и три π-связи. 4. В бутадиене-1,3 атомные орбитали углерода находятся в состоянии: а) sp2-гибридизации; б) sp3-гибридизации; в) sp -гибридизации; г) sp3d-гибридизации? 5. При сгорании бугадиена-1,3 в избытке кислорода образуются вещества: а) С2Н3ОН + Н2О; б) С2Н5ОН + Н2О; в) СН3ОН + Н2О; г) СО2 + Н2О? 6. Валентный угол в молекуле бутадиена-1,3 равен: а) 120°; б) 109°28'; в) 90°; г) 180°? 7. В промышленности бутадиен-1,3 не используют для получения: а) бутадиен-стирольного каучука; б) дивинилового каучука; в) винилацетилена; г) резины? 8. Массовая доля (%) углерода в 1,3-бутадиене: а) 80; б) 96; в) 89; г) 48? 9. Назовите по систематической номенклатуре алкадиен строения: 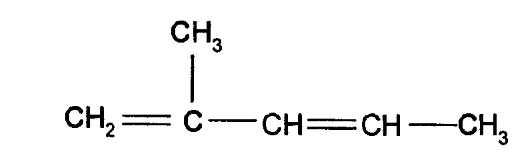 а) 4-метил-пентадиен-1,3; б) 2-метил-пентадиен-1,3; в) 4 метил-пентадиен-2,4; г) 2-метил-пентадиен? 10. В пропадиене-1,2 общее количество σ-связей равно: а) 5; б) 2; в) 9; г) 6?
Тест 2 (один вариант правильного ответа) Фенолы 1. При взаимодействии фенола с бромом образуется: а) 1,2,3-трибромфенол; б) 2,4,6-трибромфенол; в) 1,2,5-трибромфенол; г) 3-бромфенол? 2. Какая из реакций указывает на то, что фенол является слабой кислотой: а) фенол + NaOH ; б) фенол + Na ; в) калий-фенолят + СО2 + Н2О; г) натрий-фенолят + НС1? 3. Самыми сильными кислотными свойствами обладает: 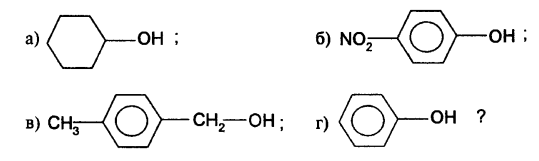 4. С каким веществом реагирует как фенол, так и этиловый спирт: а) хлороводород; б) калий; в) водный раствор КОН; г) калий-гидрокарбонат? 5. Для обнаружения фенола используется такой реагент, как: а) хлороводород; б) свежеосажденный медь(II)-гидроксид; в) железо(III)-хлорид; г) аммиачный раствор Ag2О? 6. Количество изомерных трехатомных фенолов состава C6H3(OH)3 равно: а) 3; 6) 4; в) 6; г) 7? 7. Какое из приведенных ниже веществ не относится к фенолам: 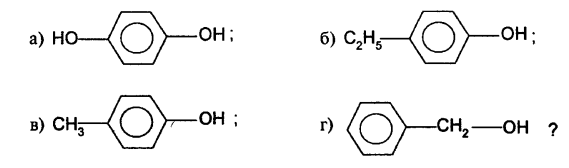 8. В какой паре первое вещество обладает более сильными кислотными свойствами, чем второе: а) этанол и вода; б) этанол и муравьиная кислота; в) вода и фенол; г) угольная кислота и фенол? 9. Какие вещества являются изомерами по отношению друг к другу: а) фенилметанол и метилфениловый эфир; б) пропанол-1 и изобутиловый спирт; в) калий-фенолят и калий-этилат; г) 2-метилпропанол-1 и 2-метилбутанол-2? 10. Укажите схему реакции, в которой не образуется фенол; а) калий-фенолят + НС1; б) хлорбензол + Н2О; в) натрий-фенолят + водный раствор СО2; г) натрий-фенолят + H2SО4 (paзб.)?
Задача 1 Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу кислоты. Задача 2 (задача повышенной сложности) Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании 4,4 г. его в кислороде образовалось 6,72 л. СО2 и 7,2 г. Н2О. Ждем Ваших решений! |
