годовая контрольная работа. ГКР химия 8. Контрольная работа за курс химии 8 класса 1 вариант Часть а к каждому из заданий даны 4 варианта ответа, из которых только
 Скачать 129.64 Kb. Скачать 129.64 Kb.
|
|
Годовая контрольная работа за курс химии 8 класса 1 вариант
А1. Электронная формула 1s22s22p63s1 соответствует атому : 1) кислорода 2) серы 3) натрия 4) калия 1. образование глюкозы в зеленом растении 2. лесной пожар 3. высыхание дождевых луж 4. процесс дыхания растений А3. Из приведенных понятий выберите только те, которые обозначают вещество. 1. железо, нож, сахар 2. стекло, дерево, железо 3. парта, дерево, стекло 4. стекло, окно, гвоздь А4. Формула сульфата калия 1) K2SO4 2) K2 SO3 3) K2S 4) CaSO4 А5. Какой элемент является окислителем в реакции, схема которой H2SO4 + Cu → CuSO4 + SO2 + H2O 1) медь 2) сера 3) водород 4) кислород А6. Как определяется число электронов атома химического элемента? 1. по порядковому номеру 2. по номеру периода 3. по номеру группы 4. по разнице между атомной массой и порядковым номером. А7. Какое из веществ имеет ковалентный неполярный вид связи? 1. O2 2. H2O 3. CaCl2 4. Ba А8. Из приведенного перечня выберите ряд, в котором указаны только двухвалентные элементы. 1. H, Na, K 2. O, Mg, Zn 3. Na, Mg, Ca 4. Al, P, Cl А9. Формулы оксида и кислоты MgO и KNO3 2) СаO и HNO3 3) NaOH и HCl 4) Al2O3 и КOH А10. Сумма коэффициентов в уравнении реакции, схема которой SO2+ O2 → SO3 1. 4 2. 5 3. 6 4. 7 А11.На какой диаграмме распределение массовых долей элементов соответствует количественному составу карбоната кальция? 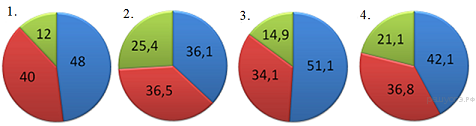 Ответ ___ А12. . Верны ли следующие суждения о правилах работы в лаборатории? А) При нагревании вещества пробирку нужно держать вертикально. Б) Чтобы погасить спиртовку, нужно накрыть её фитиль колпачком 1) верно только А 2) верно только Б 3) оба суждения верны 4) оба суждения неверны Часть В. В1. С раствором гидроксида натрия реагируют (выберите три правильных ответа из шести) 1) сульфат меди (II) 3) азотная кислота 5) оксид меди (II) 2) магний 4) гидроксид калия 6) оксид углерода (IV) Ответ __ В2. Установите соответствие между уравнением реакции и типом реакции 1. 2Al + 3S → 2Al2S3 А. реакция обмена 2. 2Fe(OH)3 → Fe2O3 + 3H2O Б. реакция замещения 3. Zn + 2HCl → ZnCl2 + H2 В. реакция разложения 4. ZnO + 2HNO3 → Zn (NO3) 2 + H2O Г. реакция соединения Часть С. С1. Осуществите цепочку превращения: Ca → CaO → Ca (OH)2 → CaCl2 С2. Объем углекислого газа, образовавшегося при сжигании 11,2 л (н.у.) метана СН4 равен СН4 + 2О2 → СО2 + Н2О Годовая контрольная работа за курс химии 8 класса 2 вариант Часть А К каждому из заданий даны 4 варианта ответа, из которых только один правильный. А1. Электронная формула 1s22s22p4 соответствует атому : 1) кислорода 2) серы 3) натрия 4) калия А2. Какое из перечисленных явлений не является химическим? 1) ржавление железа 3) плавление металла 2) горение угля 4) скисание молока А3. Из приведенных понятий выберите только те, которые обозначают физическое тело. 1. алюминий, парта, сахар 3. стекло, дерево, железо 2. ручка, тетрадь, парта 4. стекло, окно, гвоздь А4. Формула карбоната калия 1) CaСO3 2) K2СО3 3) Ca(NO2)2 4) СаSO3 А5. Какой элемент является восстановителем в реакции, схема которой KClO3 KCl + O2 1.калий 2. Хлор 3. кислород А6. Что определяется номером периода? 1. заряд ядра атома 2. число энергетических уровней 3. число валентных электронов 4. атомную массу А7. Какое из веществ имеет ионный вид связи? 1. O2 2. H2O 3. CaCl2 4. Ba А8. Из приведенного перечня выберите ряд, в котором указаны только двухвалентные элементы. 1. H, Ba, Al 3. O, Mg, Ca 2. H, Na, K 4. Al, P, Cl А9. Формулы основания и соли 1) SiO2 и NaCl 3) Mg(OН)2 и ZnSO4 2) Са(OH)2 и HCl 4) СaСО3 и Fe2O3 А10. Сумма коэффициентов в уравнении реакции, схема которой Mg + O2 → MgO 1. 4 2. 5 3. 6 4. 7 А11. На какой диаграмме распределение массовых долей элементов соответствует количественному составу нитрата калия? 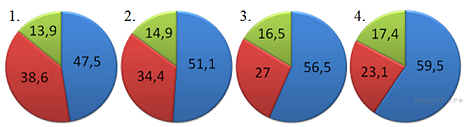 Ответ: А12. Верны ли следующие суждения о правилах работы в лаборатории? А) При нагревании вещества отверстие пробирки нужно направлять в сторону от себя и от товарища Б) Чтобы погасить спиртовку, нужно задуть пламя. 1) верно только А 2) верно только Б 3) оба суждения верны 4) оба суждения неверны Часть В. В1. В реакцию с раствором соляной кислоты вступают (выберите три правильных ответа из шести) 1) медь 4) карбонат натрия 2) гидроксид магния 5) хлорид бария 3) оксид натрия 6) оксид серы (VI) В2. Установите соответствие между уравнением реакции и типом реакции 1. Fe + S → FeS А. реакция обмена 2. 2Al(OH)3 → Al2O3 + 3H2O Б. реакция замещения 3. Fe + CuCl2 → FeCl2 + Cu В. реакция разложения 4. CaO + H2CO3 → CaCO3 + H2O Г. реакция соединения Часть С С1. Осуществите цепочку превращения: Ba → BaO → Ba(OH)2 → BaSO4 С2. Масса цинка, необходимого для получения 2 моль водорода по следующей схеме превращений составляет Zn + 2HCl → ZnCl2 + H2↑ |
