Лабораторная работа №6. Лабораторная работа 6. 3 Определение потенциала ионизации аргона выполнил студент ап102 Камышников Г. А
 Скачать 1.49 Mb. Скачать 1.49 Mb.
|
|
Министерство цифрового развития, связи и массовых коммуникаций Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования «Сибирский государственный университет телекоммуникаций и информатики» (СибГУТИ) Кафедра физики Лабораторная работа №6.3 ОПРЕДЕЛЕНИЕ ПОТЕНЦИАЛА ИОНИЗАЦИИ АРГОНА Выполнил студент: АП-102 Камышников Г.А.  (группа) (Фамилия Имя Отчество) Проверил преподаватель:  (должность) (Фамилия Имя Отчество)  Измерения сняты: Измерения сняты: (дата) (подпись) (расшифровка подписи)  Отчет принят: Отчет принят: (дата) (подпись) (расшифровка подписи) Работа зачтена:  (оценка) (дата) (подпись) (расшифровка подписи) Новосибирск, 2021 г. Лабораторная работа № 6.3 ОПРЕДЕЛЕНИЕ ПОТЕНЦИАЛА ИОНИЗАЦИИ АРГОНАЦЕЛЬ РАБОТЫ Определить потенциал ионизации атомов аргона. ОСНОВНЫЕ ТЕОРЕТИЧЕСКИЕ СВЕДЕНИЯ Согласно современным теоретическим представлениям атомные системы мо- гут находиться только в некоторых определенных состояниях, называемых ста-ционарными. Каждому стационарному состоянию соответствует свое фиксиро- ванное значение энергии. Спектр допустимых значений энергий атомов является дискретным. Состояние с наименьшим допустимым значением энергии атоманазываетсяосновнымсостоянием. Часто при взаимодействиях атома с внешними системами изменяется состояние только валентного (внешнего) электрона. По- этому в данной работе мы будем считать, что энергия атома эквивалентна энергии валентного электрона, а состояние атома и состояние валентного электрона будем считать синонимами. Значения энергии разрешенного состояния называют энер-гетическими уровнями. На энергетических диаграммах энергетические уровни обозначают черточками. Если атом находится в основном состоянии, то все энер- гетические уровни, расположенные ниже энергетического уровня валентного электрона, заняты электронами, а все вышележащие уровни – свободны, смотри рисунок 3.1(а). Согласно современным теоретическим представлениям атомные системы мо- гут находиться только в некоторых определенных состояниях, называемых ста-ционарными. Каждому стационарному состоянию соответствует свое фиксиро- ванное значение энергии. Спектр допустимых значений энергий атомов является дискретным. Состояние с наименьшим допустимым значением энергии атоманазываетсяосновнымсостоянием. Часто при взаимодействиях атома с внешними системами изменяется состояние только валентного (внешнего) электрона. По- этому в данной работе мы будем считать, что энергия атома эквивалентна энергии валентного электрона, а состояние атома и состояние валентного электрона будем считать синонимами. Значения энергии разрешенного состояния называют энер-гетическими уровнями. На энергетических диаграммах энергетические уровни обозначают черточками. Если атом находится в основном состоянии, то все энер- гетические уровни, расположенные ниже энергетического уровня валентного электрона, заняты электронами, а все вышележащие уровни – свободны, смотри рисунок 3.1(а).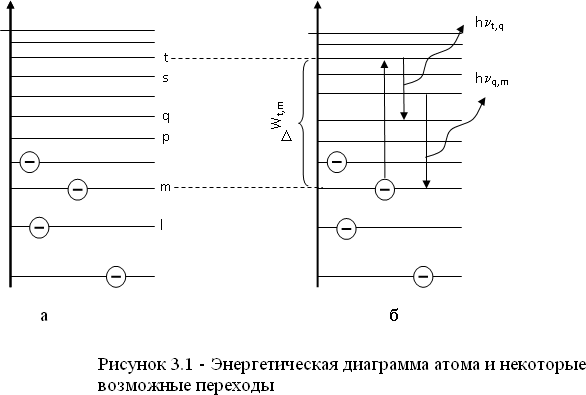 В случае внешних воздействий атом, т.е., как правило, один из его валентных электронов может получить дополнительную энергию Wи перейти в какое- либо из разрешенных состояний с большей энергией, рис. 3.1(б). Такоесостояниеатома называется возбужденным.В возбужденном состоянии атом долго нахо- диться не может. Очень быстро он спонтанно (самопроизвольно) возвращается непосредственно в основное состояние или переходит в одно из возбужденных состояний с меньшей энергией, например с уровня t на уровень m на рисунке 3.1(б). Переход атомной системы из состояния с большей энергией Wk в состояние с меньшей энергией Wn сопровождается выделением энергии W WkWn, (1) которая излучается в виде кванта электромагнитного излучения h , так что: h WkWn (2). (2) н возб  Соотношениеа азываетсяправиломчастот. Соотношениеа азываетсяправиломчастот. Энергию уждения часто характеризуют потенциалом возбуждения. При этом под потенциалом возбуждения понимают ту разность потенциалов, которую должен пройти электрон, чтобы приобрести энергию, равную данной энергии воз- буждения. Если подведенная извне энергия превысит модуль энергии основного состо- яния валентного электрона, то валентный электрон, получив эту энергию, выйдет за пределы атома и станет свободным. Такой процесс называется ионизациейатома. В результате ионизации, нейтральный атом превращается в положительно заряженный ион и, кроме того, появляется свободный электрон. Минимальная энергия, при которой возникает ионизация атомов, называется энергией ионизации Wi . Энергия ионизации атомов зависит от структуры атомов и характеризуется потенциалом ионизации. Потенциал ионизации равен той раз-ностипотенциалов,которуюдолженпройтиэлектрон,чтобыприобрестиэнер-гию,равнуюэнергииионизацииатома. ОПИСАНИЕ УСТАНОВКИ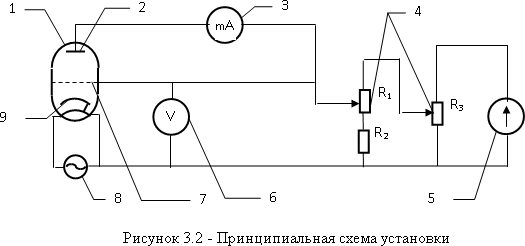 Установка, рис. 3.2, состоит из тиратрона (1), гальванометра (3), включенного в анодную цепь тиратрона, источника напряжения анодной цепи (5), вольтметра (6), измеряющего ускоряющее напряжение, источника питания (8) накала катода тиратрона. Потенциометры (4) служат для регулировки ускоряющего напряжения анодной цепи тиратрона. Тиратрон представляет собой стеклянный баллон (1), заполненный аргоном с малым давлением. В баллон помещены три электрода: катод (9) подогревного типа, сетка (7) и анод (2). Под действием напряжения накала нить накала и катод разогреваются. Воз- никает явление термоэлектронной эмиссии. Вследствие термоэлектронной эмис- сии, вокруг разогретого катода образуется электронное облако. К катоду и сетке подведено ускоряющее напряжение. Под действием ускоряющего поля элек- троны, эмитируемые катодом, ускоряются, проходят сквозь ячейки сетки, далее попадают на анод (2) и регистрируются гальванометром (3) в виде анодного тока, рис.3.3. 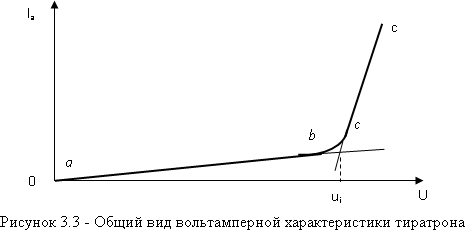 Увеличение ускоряющего напряжения сопровождается возрастанием анод- ного тока, участок a b на рис.3.3. На участке a bявления ионизации не проис- ходит, поэтому рост силы тока достаточно слаб. При прохождении участка катод-сетка, электроны приобретают: W eU Если окажется, что энергия электронов больше, чем энергия ионизации: (3) W Wi, (4) то катодные электроны, сталкиваясь с атомами аргона в области за сеткой, иони- зируют атомы аргона. Ионизация атомов аргона сопровождается увеличением концентрации свободных электронов, создающих анодный ток, и, кроме того, об- разующиеся из атомов аргона положительные ионы, двигаясь к катоду, вносят до- полнительный вклад в рост силы анодного тока. Вследствие этого, крутизна воз- растания анодного тока резко увеличивается, участок b c на рис. 3.3. Напряже- ние излома вольтамперной характеристики тиратрона, рис. 3.3, позволяет нам определить потенциал ионизации атомов аргона. ВЫПОЛНЕНИЕ РАБОТЫ  Ui=15,8 В Ui=15,8 ВВывод: в ходе данной работы я построил график ВАХ тиратрона и определил потенциал ионизации атома аргона (15,8В). КОНТРОЛЬНЫЕ ВОПРОСЫОбъясните в общих чертах строение атомов. Атомы состоят из ядра и электронов (точнее, электронного «облака»). Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным Какие состояния называются стационарными? Стационарным состоянием в термодинамике называют состояние вещества, когда основные его характеристики не изменяются со временем. Стационарным состоянием в квантовой физике атома называют состояние, при котором оно имеет постоянную энергию. Что называют возбуждением атомов и ионизацией атомов? Возбуждение атома- квантовый переход атома или молекулы с более низкого (напр., основного) уровня энергии на более высокий при поглощении ими фотонов (фотовозбуждение) или при столкновениях с электронами и др. частицами (возбуждение ударом). Ионизация атома- эндотермический процесс образования ионов из нейтральных атомов или молекул. Положительно заряженный ион образуется, если электрон в молекуле получает достаточную энергию для преодоления потенциального барьера, равную ионизационному потенциалу Что называют потенциалом ионизации атомов? Потенциал ионизации атома или иона определяется как работа, которая требуется для отрыва электрона от атома или иона и удаления его на бесконечно большое расстояние. По абсолютной величине он равен, очевидно, потенциальной энергии отрываемого электрона, но имеет обратный знак Что понимают под энергетическими уровнями атомов. Главные энергетические уровни атома — это совокупности атомных орбиталей, имеющих одинаковые значения главного квантового числа. Число таких энергетических уровней в атоме равно номеру периода, в котором расположен соответствующий химический элемент. Поясните схему и принцип действия лабораторной установки. Установка, рис. 3.2, состоит из тиратрона (1), гальванометра (3), включенного в анодную цепь тиратрона, источника напряжения анодной цепи (5), вольтметра (6), измеряющего ускоряющее напряжение, источника питания (8) накала катода тиратрона. Потенциометры (4) служат для регулировки ускоряющего напряжения анодной цепи тиратрона. Тиратрон представляет собой стеклянный баллон (1), заполненный аргоном с малым давлением. В баллон помещены три электрода: катод (9) подогревного типа, сетка (7) и анод (2). Под действием напряжения накала нить накала и катод разогреваются. Возникает явление термоэлектронной эмиссии. Вследствие термоэлектронной эмиссии, вокруг разогретого катода образуется электронное облако. К катоду и сетке подведено ускоряющее напряжение. Под действием ускоряющего поля электроны, эмитируемые катодом, ускоряются, проходят сквозь ячейки сетки, далее попадают на анод (2) и регистрируются гальванометром (3) в виде анодного тока, рис.3.3. Почему крутизна вольтамперной характеристики резко увеличивается, когда ускоряющее напряжение превышает потенциал ионизации атомов? Ионизация атомов аргона сопровождается увеличением концентрации свободных электронов, создающих анодный ток, и, кроме того, образующиеся из атомов аргона положительные ионы, двигаясь к катоду, вносят дополнительный вклад в рост силы анодного тока. Вследствие этого, крутизна воз- растания анодного тока резко увеличивается, участок b c на рис. 3.3 ЗАДАЧИ К ЛАБОРАТОРНОЙ РАБОТЕКакой наименьшей скоростью должен обладать электрон, чтобы ионизи- ровать атом гелия? Энергия ионизации атома гелия равна 24,5 эВ.  Дано: Р-е:  W=24,5эВ W= 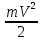 V-? V= 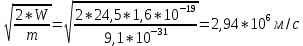 Ответ: 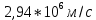 Электрон, ускоренный электрическим полем, приобрел скорость, при ко- торой его масса стала равной удвоенной массе покоя. Чему равна разность потен- циалов, пройденная электроном? 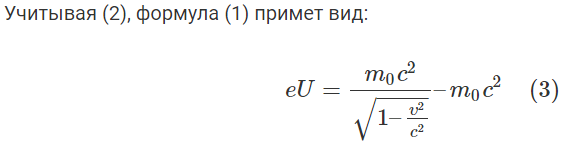 |
