Лекция_Обмен углеводов. Лекция_09_Обемн_углеводов. Лекция 9 Обмен углеводов
 Скачать 0.5 Mb. Скачать 0.5 Mb.
|
|
Лекция 9 Обмен углеводов Углеводный обмен занимает одно из ведущих мест в обмене веществ. При распаде (окислении) углеводов в клетках высвобождается свободная энергия, которая запасается в макроэргических связях АТФ, поставляющей свою энергию для осуществления биохимических процессов. Глюкоза играет главную роль в метаболизме углеводов, так как именно она является основным источником энергии. Глюкоза может превращаться практически во все моносахариды, в то же время возможно и обратное превращение. 9.1. Катаболизм глюкозы Гликолиз и цикл трикарбоновых кислот (ЦТК) приводят к полному окислению глюкозы до оксида углерода (IV) CO2 и Н2О и выделению больших количеств энергии в форме АТФ. 9.1.1. Основные источники глюкозы Основными источниками глюкозы в растительных и животных клетках являются полисахариды и свободные дисахариды: - полисахариды: крахмал (растения) и гликоген (животные); - дисахариды: сахароза, лактоза и мальтоза. При катаболизме углеводов в клетках происходит ферментативный гидролиз гликозидных связей и образование моносахаридов, главным из которых является глюкоза. Гидролиз крахмала катализирует фермент амилаза, которая расщепляет внутренние α-1,4-гликозидные связи. В результате из крахмала образуются дисахаридные остатки мальтозы и изомальтозы. Гидролиз всех дисахаридов катализируется специфическими ферментами: сахаразой, лактазой, мальтазой и изомальтазой. В результате действия этих ферментов происходит ферментативный гидролиз гликозидных связей с образованием соответствующих моносахаридов. Гидролиз гликогена катализирует фермент фосфорилаза, которая гидролизует α-1,4-гликозидные связи с одновременным присоединением фосфорной кислоты по месту разрыва гликозидной связи между остатками моносахаридов. В результате из гликогена образуется глюкозо-1-фосфат (Рис. 9.1): 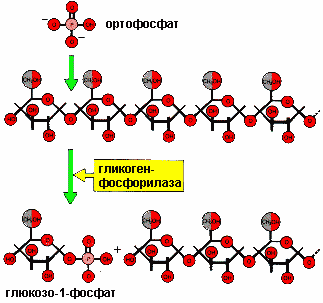 Рис. 9.1. Схема гидролиза гликогена Таким образом: 1) При распаде олиго- и полисахаридов возникают свободные моносахариды или их фосфорные эфиры. 2) В дальнейшем в обмене моносахаридов участвуют только их фосфорные эфиры. Свободные монозы подвергаются фосфорилированию с образованием соответствующих фосфорных эфиров. Фосфорные эфиры представляют собой более реакционнспособные соединения по сравнению со свободными моносахаридами. 3) Фосфорилирование моносахаридов осуществляется при их взаимодействии с АТФ и катализируется ферментами фосфотрансферазами, которые называются – киназами: Глюкоза + АТФ = Глюкозо-6-фосфат + АДФ 4) В результате реакции фосфорилирования фосфорные эфиры становятся макроэргическими соединениями. 9.2. Гликолиз Гликолиз - это последовательность реакций, в результате которых глюкоза распадается на две молекулы пировиноградной кислоты (пирувата) (аэробный гликолиз) или две молекулы молочной кислоты(лактата) (анаэробный гликолиз). Все реакции гликолиза протекают в цитозоле и характерны для всех органов и тканей. Ниже приведены стехиометрические уравнения анаэробного (а) и аэробного (б) гликолиза: C6H12O6 + 2АДФ + 2H3PO4 → → 2CH3CHOHCOOH + 2АТФ + H2O (а); C6H12O6 + 2АДФ + 2H3PO4 + НАД+ → → 2CH3CHOCOOH + 2АТФ + H2O + НАДН∙Н+ (б). Общие характеристики для аэробного и анаэробного гликолиза: - большинство реакций обратимо, за исключением трех (реакций 1, 3, 10); - все метаболиты находятся в фосфорилированной форме; - источником фосфатной группы в реакциях фосфорилирования являются АТФ (реакции 1, 3) или неорганический фосфат (реакция 6). 9.2.1. Анаэробный гликолиз !!! Анаэробный гликолиз это расщепление глюкозы в отсутствии или при недостаточном количестве кислорода. Анаэробный гликолиз включает теже реакции, что и аэробный гликолиз до пирувата, но с последующим превращением пирувата в лактат. Последовательность реакций анаэробного гликолиза представлена на рисунке 9.2: 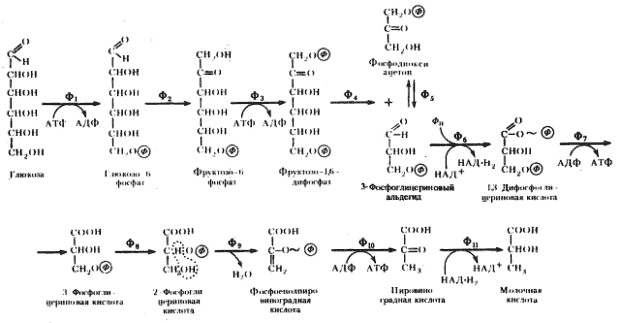 Рис. 9.2. Схема гликолиза в анаэробных условиях: Ф1 — гексокиназа; Ф2 — глюкозофосфатизомераза; Ф3 — фофсофруктокиназа; Ф4 — фруктозо-1,6-дифосфатальдолаза; Ф5 — триозофосфатизомераза; Ф6 — 3-ФГА-дегидрогеназа; Ф7 — фофсоглицерокиназа; Ф8 — фосфоглицеромутаза; Ф9 — енолаза; Ф10 — пируваткиназа; Ф11 — лактатдегидрогеназа Условно гликолиз можно разделить на две стадии: - первая стадия гликолиза – стадия активации глюкозы, которая включает пять реакций и завершается расщеплением углеродного скелета глюкозы на две молекулы трёхуглеродного скелета – глицероальдегидфосфата; - вторая стадия – синтез молекул АТФ, в которой энергия окислительных реакций трансформируется в химическую энергию АТФ по механизму субстратного фосфорилирования. I. Стадия активации глюкозы: 1) Необратимая реакция фосфорилирования глюкозы и образования глюкозо-6-фосфата, катализируемая ферментом гексокиназой. 2) Обратимая реакция кето-альдольной изомеризации глюкозо-6-фосфата во фруктозо-6-фосфат, катализируемая ферментом глюкозо-6-фосфатизомеразой. 3) Необратимая реакция фосфорилирования фруктозо-6-фосфата молекулой АТФ до фруктозо-1,6-дифосфата, катализируемая ферментом фосфофруктокиназой. 4) Обратимая реакция расщепления связи С-С во фруктозо-1,6- дифосфате на две триозы дигидрооксиацетон-3-фосфат и глицеральдегид-3-фосфат, катализируемые ферментом альдолазой. 5) Обратимая реакция кето-альдольной изомеризации дигидроксиацетон-3-фосфата в глицеральдегид-3-фосфат, катализируемая ферментом триозофосфатизомеразой. II. Стадия синтеза АТФ: 6) Обратимая реакция окисления глицероальдегид-3-фосфата до 1,3-фосфоглицерата, которая катализируется ферментом глицеральдегид-3-фосфатдегидрогеназой. !!! Эта реакция позволяет высокую энергию окисления альдегидной группы аккумулировать в виде макроэргической связи АТФ. 7) Обратимая реакция субстратного фосфорилирования АДФ и образования АТФ, при которой происходит перенос богатого энергией фосфорильного остатка с 1,3-дифосфоглицерата на АДФ. Реакция катализируется фосфоглицераткиназой. 8) Обратимая реакция изомериизации 3-фосфоглицерата в 2-фосфоглицерат, катализируемая ферментом фосфоглицератмутазой. 9) Обратимая реакция енолизации, в процессе которой отщепление молекулы воды от 2-фосфоглицерата приводит к образованию макроэргической связи в фосфоеноилпирувате. Реакция катализируется ферментом енолазой. 10) Необратимая реакция субстратного фосфорилирования АДФ и образования АТФ, при которой происходит разрыв макроэргитечской связи и перенос фосфорильного остатка от фосфоэнолпирувата на АДФ. Катализируется эта реакция ферментом пируваткиназой. 11) Обратимая реакция восстановления пирувата до лактката происходит в анаэробных условиях при участии фермента лактатдегидрогеназы, коферментом которой является восстановленная форма НАДН∙Н+ Специфические характеристики анаэробного гликолиза (отличие от аэробного гликолиза): Во-первых, при анаэробном гликолизе окисление НАДН∙Н+ осуществляется независимо от дыхательной цепи. В этом случае акцептором водорода от НАДН∙Н+ является пируват, который восстанавливается в лактат. Во-вторых, образование АТФ при анаэробном гликолизе идёт за счет субстратного фосфорилирования, когда для фосфорилирования АДФ используется энергия макроэргической связи субстрата (реакции 7, 10). 9.2.1.1. Энергетический эффект и биологическое значение анаэробного гликолиза Энергетический эффект анаэробного гликолиза по сравнению с аэробным – небольшой: образование двух моль лактата из глюкозы сопровождается синтезом всего двух моль АТФ. Это объясняется тем, что восстановленная форма НАДН∙Н+, полученная при окислении глицероальдегидфосфата, не используется дыхательной цепью, а акцептируется пируватом. Анаэробный гликолиз является основным источником энергии для скелетных мышц в начальном периоде интенсивной работы, то есть в условиях, когда снабжение кислородом ограничено. Кроме того, зрелые эритроциты извлекают энергию за счет анаэробного окисления глюкозы, потому что не имеют митохондрий. 9.3. Брожение Брожение - процесс анаэробного расщепления углеводов (глюкозы), происходящий под влиянием микроорганизмов или выделенных из них ферментов. Брожение, идентично по химизму реакциям гликолиза в аэробных условиях вплоть до образования пирувата. Далее в зависимости от вида микроорганизмов пировиноградная кислота подвергается различным превращениям с образованием различных конечных продуктов (Рис. 9.3): 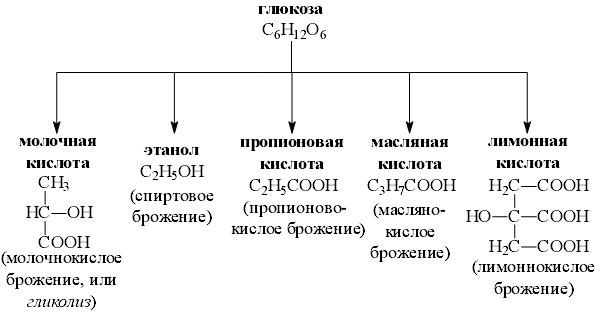 Рис. 9.3. Виды брожения глюкозы и их конечные продукты В зависимости от характера конечных продуктов различают спиртовое, молочнокислое, маслянокислое, пропионовокислое, ацетоно-бутиловое, ацетоно-этиловое и др. виды брожения. 9.3.1. Биологическое значение брожения В ходе брожения в результате сопряженных окислительно-восстановительных реакций: - аккумулируется энергия в виде молекул АТФ, необходимая для жизнедеятельности микроорганизмов; - образуются химические соединения, которые микроорганизмы используют для биосинтеза собственных белков, нуклеиновых кислот, полисахаридов и др. 9.3.2. Спиртовое брожение Для дрожжей характерен процесс спиртового брожения. Суммарно уравнение спиртового брожения может быть представлено в следующем виде: C6H12O6 + 2H3PO4 + 2АДФ → 2CH3CH2OH + 2CO2 + 2АТФ. !!! В процессе спиртового брожения вплоть до образования пирувата реакции идут по механизму аэробного гликолиза. Превращение пирувата в продукты спиртового брожения включает две реакции (Рис. 9.4): 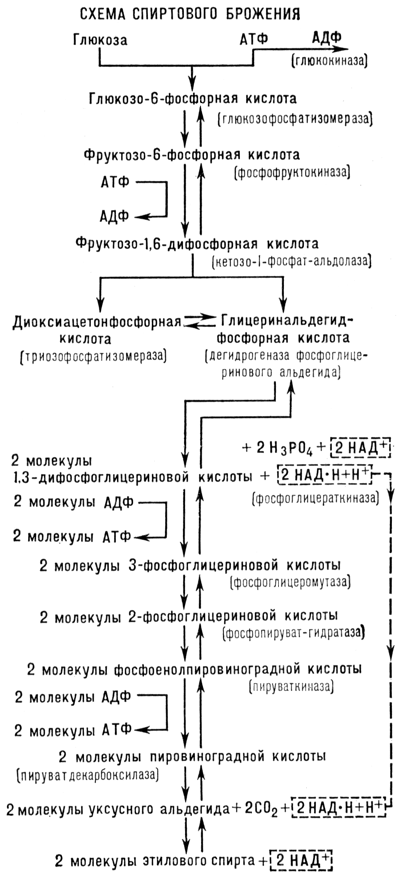 Рис. 9.4. Схема спиртового брожения глюкозы: реакции 1-10 – расщепление глюкозы до пировиноградной кислоты (совпадает с аэробным гликолизом); реакции 11-12 – образование этилового спирта из пировиноградной кислоты. 11) Необратимая реакция декарбоксилирования пирувата при участии имеющегося в дрожжах фермента пируватдекарбоксилазы с образованием уксусного альдегида и двуокиси углерода. 12) Реакция восстановления альдегида до этанола при действии фермента алкогольдегидрогеназы, содержащего в качестве кофермента НАД в восстановленной форме (НАДН∙Н+), образовавшийся при окислении 1,3-глицеринфосфорной кислоты (реакция 6). Энергетический эффект спиртового брожения: при сбраживании 1 моля глюкозы образуются: - 2 моля этилового спирта; - 2 моля CO2; - в результате фосфорилирования 2 молей АДФ образуются 2 моля АТФ. Сбраживание углеводов (глюкозы, ферментативных гидролизатов крахмала, кислотных гидролизатов древесины) используется во многих отраслях промышленности: для получения этилового спирта, глицерина и др. технических и пищевых продуктов. На спиртовом брожении глюкозы основаны приготовление теста в хлебопекарной промышленности, виноделие и пивоварение. 9.4. Аэробный гликолиз Аэробный гликолиз протекает в присутствии кислорода, включает те же стадии, что и анаэробный гликолиз, за исключением последней стадии: восстановления пирувата до лактата, которая протекает в анаэробных условиях (Рис. 9.5): 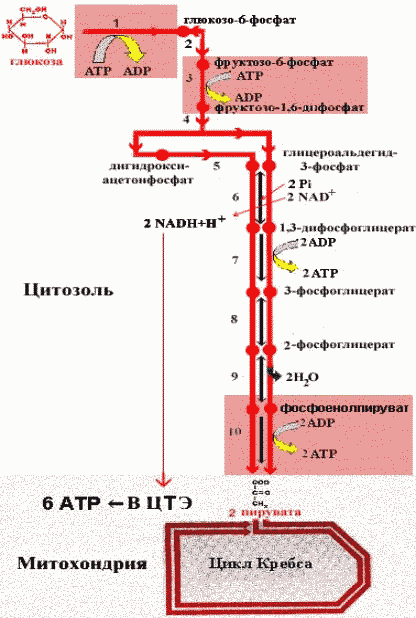 Рис. 9.5. Схема аэробного гликолиза Специфические характеристики аэробного гликолиза (отличие от анаэробного гликолиза): Во-первых, окисление восстановленной формы НАДН∙Н+, являющееся необходимым условием протекания гликолиза, происходит при аэробном гликолизе посредством дыхательной цепи. Во-вторых, образование АТФ при аэробном гликолизе может идти двумя путями: - путём субстратного фосфорилирования, когда для фосфорилирования АДФ используется энергия макроэргической связи субстрата (реакции 7, 10); - путем окислительного фосфорилирования АДФ, сопряженного с дыхательной цепью (реакция 6). 9.4.1 Энергетическое значение аэробного распада глюкозы В аэробном гликолизе образуется 10 моль АТР на 1 моль глюкозы. Так, в реакциях 7, 10 образуется 4 моль АТФ путем субстратного фосфорилирования, а в реакции 6 синтезируется 6 моль АТФ (на 2 моль глицероальдегидфосфата) путем окислительного фосфорилирования. Суммарный эффект аэробного гликолиза составляет 8 моль АТР, так как в реакциях 1 и 3 используется 2 моль АТР. 9.5. Цикл трикарбоновых кислот Цикл трикарбоновых кислот (ЦТК) или цикл лимонной кислоты или цикл Кребса – путь окислительных превращений ди- и трикарбоновых кислот, образующихся в качестве промежуточных продуктов при распаде и синтезе белков, жиров и углеводов. Цикл трикарбоновых кислот представлен в клетках всех организмов: растений, животных и микроорганизмов. Этот цикл является основой метаболизма и выполняет две важных функции: - снабжения организма энергией; - интеграции всех главных метаболических потоков, как катаболических (биорасщепление), так и анаболических (биосинтез). Напомню, что реакции аэробного гликолиза локализованы в цитоплазме клетки и приводят к образованию пирувата (ПВК). !!! Последующие превращения пирувата протекают в матриксе митохондрий. В матриксе пируват превращается в ацетил-КоА – макроэргическое соединение. Реакция катализируется ферментом НАД-зависимой пируватдекарбоксилазой: 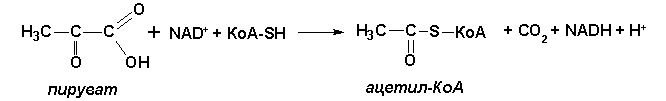 Восстановленная форма НАДН∙Н+, образовавшаяся в результате этой реакции, поступает в дыхательную цепь и генерирует 6 молекул АТФ (в пересчете на 1 молекулу глюкозы). !!! ЦТК представляет собой последовательность из восьми реакций, протекающих в матриксе митохондрий (Рис. 9.6): 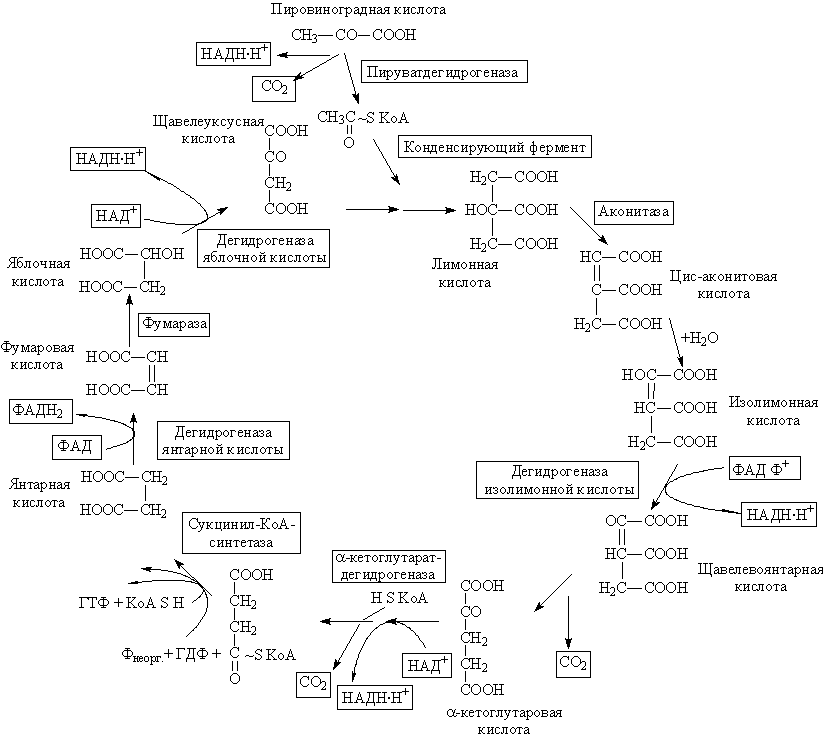 Рис. 9.6. Схема цикла трикарбоновых кислот 1) Необратимая реакция конденсации ацетил-КоА со щавелевоуксусной кислотой (оксалоацетатом), катализируемая ферментом цитратсинтетазой, с образованием лимонной кислоты (цитрата). 2) Обратимая реакция изомеризация лимонной кислоты (цитрата) в изолимонную кислоту (изоцитрат), в процессе которой происходит перенос гидроксигруппы к другому атому углерода, катализируется ферментом аконитазой. Реакция идёт через образование промежуточного продукта цис-аканитовой кислоты (цис-аконитата). 3) Необратимая реакция окислительного декарбоксилирования изолимонной кислоты (изоцитрата): гидроксигруппа изолимонной кислоты окисляется до карбонильной группы с помощью окисленной формы НАД+ и одновременно отщепляется карбоксильная группа в β-положении с образованием α-кетоглутаровой кислоты (α-кетоглутарата). Промежуточный продукт этой реакции щавелевоянтарная кислота (оксалосукцинат). !!! Это первая реакция цикла, в которой происходит восстановление окисленной формы НАД+-кофермента до НАДН∙Н+, фермента изоцитратдегидрогеназы. Восстановленная форма НАДН∙Н поступает в дыхательную цепь, там окисляется до НАД+, что приводит к образованию 2 молекул АТФ. 4) Обратимая реакция окислительного декарбоксилирования α-кетоглутаровой кислоты до макроэргического соединения сукцинил-КоА. Реакцию катализирует фермент 2-оксоглутаратдегидрогеназный комплекс. 5) Реакция является единственной в цикле реакцией субстратного фосфорилирования; катализируется ферментом сукцинил-КоА-синтетазой. В этой реакции сукцинил-КоА при участии гуанодиндифосфата (ГДФ) и неорганического фосфата (H3PO4) превращается в янтарную кислоту (сукцинат). !!! Одновременно происходит синтез макроэргического соединения ГТФ за счёт макроэргической связи тиоэфирной связи сукцинил-КоА. 6) Реакция дегидрирования янтарной кислоты (сукцината) с образованием фумаровой кислоты (фумарата). Реакция катализируется сложным ферментом сукцинатдегидрогеназой, в молекуле которой кофермент ФАД+ ковалентно связан, а белковой частью фермента. Окисленная форма ФАД+ в результате реакции восстанавливается до ФАД∙Н2. Восстановленная форма ФАД∙Н2 поступает в дыхательную цепь, там регенерирует до окисленной формы ФАД+, что приводит к образованию двух молекул АТФ. 7) Реакция гидратации фумаровой кислоты (фумарата) до яблочной кислоты (малата). Реакция катализируется ферментом фумаразой. 8) Реакция дегидрирования яблочной кислоты до щавелеуксусной кислоты (оксалоацетата). Реакция катализируется ферментом НАД+-зависимой-малатдегидрогеназой. В результате реакции окисленная форма НАД восстанавливается до восстановленной формы НАДН∙Н+. Восстановленная форма НАДН∙Н поступает в дыхательную цепь, там окисляется до НАД+, что приводит к образованию 2 молекул АТФ. Суммарное уравнение ЦТК можно записать следующим образом: Ацетил-КоА + 3НАД+ + ФАД+ + ГДФ + H3PO4 = 2CO2 + H2O + HS-КоА + 3НАДН∙Н + ФАД∙Н2 + ГТФ Как видно из схемы суммарного уравнения ЦТК в этом процессе восстанавливаются: - три молекулы НАДН∙Н (реакции 3, 4, 8); - одна молекула ФАД∙Н2 (реакция 6). При аэробном окислении из этих молекул в электрон-транспортной цепи в процессе окислительного фосфорилирования образуется при окислении: - одной молекулы НАДН∙Н – 3 молекулы АТФ; - одной молекулы ФАД∙Н2 – 2 молекулы АТФ. - одна молекула ГТФ образуется в реакции субстратного фосфорилирования (реакция 5). Всё это составит : 9 (3х3) АТФ + 2 АТФ + 1 АТФ (ГТФ) = 12 АТФ. Следовательно, энергетический баланс окисления ацетил-КоА (2 молекулы пирувата из аэробного гликолиза) в ЦТК составляет 24 молекулы АТФ. !!! Полное окисление глюкозы: 8 молекул АТФ гликолиза + 6 молекул АТФ окислительного декарбоксилирование пирувата в цетил-КоА + 24 молекулы АТФ ЦТК = 38 молекул АТФ на молекулу глюкозы. 9.6. Биосинтез углеводов Биосинтез (анаболизм) углеводов можно условно разделить на три процесса: биосинтез глюкозы, олигосахаридов и полисахаридов. У растений огромные количества глюкозы образуются путём восстановления диоксида углерода (CO2) в процессе фотосинтеза. 9.6.1. Биосинтез глюкозы – глюконеогенез !!! В организме животных глюкоза синтезируется из простых предшественников: пирувата, лактата или любого другого компонента, который в процессе катаболизма может быть превращён в пируват или один из метаболитов ЦТК. Обратное превращение пирувата в глюкозу называется глюконеогенезом (Рис. 9.7): 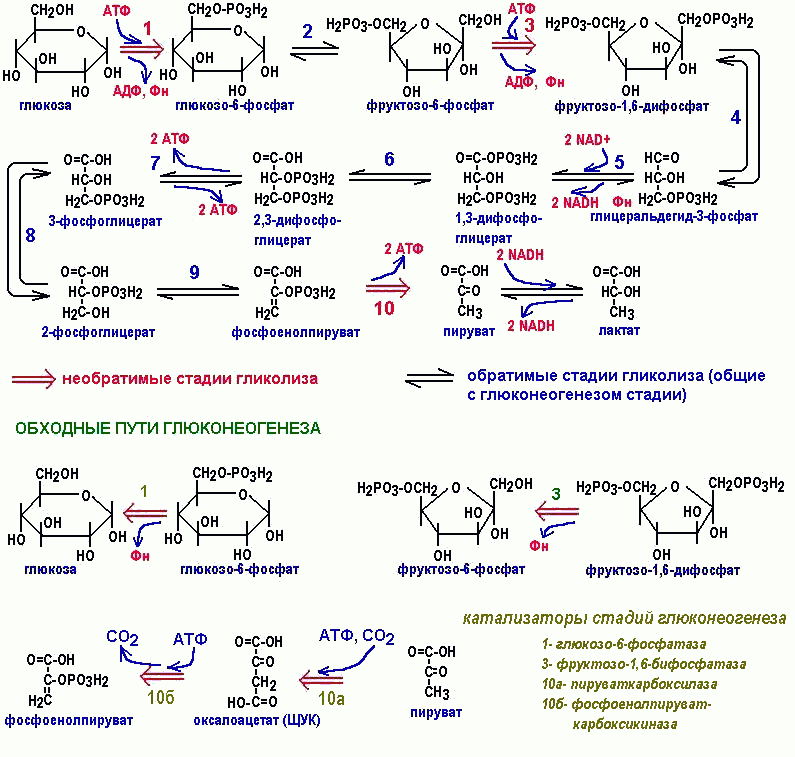 Рис. 9.7. Схема биосинтеза глюкозы в организме животных !!! Глюконеогенез протекает в основном по тому же пути, что и аэробный гликолиз, но в обратном направлении. !!! Однако, три реакции гликолиза (1, 3 и 10) необратимы, и в обход этих реакций в глюконеогенезе протекают другие реакции, катализируемые соответствующими ферментами. 10) Реакция - фосфорилирования пирувата – превращение пирувата в фосфоенолпируват идёт при участии двух ферментов пируваткарбоксилазы и фосфоеноилпируваткарбоксилазы. Реакция протекает в две стадии с образованием промежуточного продукта щавелевоуксусной кислоты и с потреблением энергии за счет молекул АТФ и ГТФ: Пируват +АТФ + ГТФ + → Фосфоеноилпируват + АДФ + ГДФ + H3PO4 2) Реакция – дефосфорилирования фруктозо-1,6-дифосфата – катализируется ферментом фруктозо-1,6-дифосфатазой, с образованием фркутозо-6-фосфата. 1) Реакция – дефосфорилирования фруктозо-6-фосфата – катализируется ферментом глюкозо-6-фосфотазой, с образованием глюкозы. Общую реакцию синтеза одной молекулы глюкозы можно представать следующим уравнением: Пируват +4АТФ + 4ГТФ + 2 НАДН∙Н + 4H2O → → Глюкоза + 2НАД+ + 4АДФ + 4ГДФ + 6H3PO4 Таким образом, синтез глюкозы из пирувата требует значительных затрат энергии: 4 молекулы АТФ и 2 молекулы ГТФ. 9.6.2. Биосинтез олигосахаридов и полисахаридов !!! Биосинтез олигосахаридов осуществляется путём переноса фосфорного эфира моносахарида к другим моносахаридам или их фосфорным эфирам (реакция трансгликозидирования). Реакции катализируются специфическими ферментами гликозилтрансферазами - фосфорилазами. В качестве субстратов гликозильных остатков в реакциях трансгликозидирования выступают уридиндифосфат глюкоза (УДФ-глюкоза) или другие нуклеозидфосфатсахара, например, гуанозиндифосфатглюкоза и др. Например, синтез сахарозы осуществляется путём переноса остатка глюкозы от УДФ-глюкозы к молекуле фруктоз-6-фосфата при каталитическом воздействии фермента неспецифической сахарзофосфорилазы. !!! Синтез полисахаридов также осуществляется путём реакции трансгликозидирования (переноса) гликозильных остатков в виде фосфорных эфиров моносахаридов или уридиндифосфосахаров на невосстанавливающийся конец растущего полисахарида. Реакции переноса остатков моносахаридов в процессе синтеза полисахаридов ускоряются соответствующими ферментами гликозилтрансферазами. Биосинтез гликогена – гликогенез - показан на рисунке 9.8: 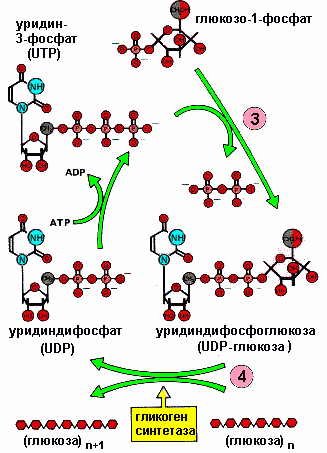 Рис. 9.8. Схема биосинтеза гликогена – гликогенеза - в клетках животных В начальных реакциях образуется УДФ-глюкоза (реакция 3), которая является активированной формой глюкозы, непосредственно включающейся в реакцию полимеризации (реакция 4). Реакция, приводящая к образованию гликогена, происходит при переносе остатка глюкозы, входящего в состав УДФ-глюкозы, на гликозидную «затравочную цепь» гликогена. При этом образуется α(1→4)-гликозидная связь между первым атомом углерода добавляемого остатка глюкозы и 4-гидргксильной группой остатка глюкозы в цепи гликогена. Эта реакция катализируется ферментом гликосинтетазой. Для подготовки и включения в растущую полисахаридную цепь 1 моль глюкозы требуется энергия 1 моль АТФ и 1 моль УТФ. Ветвление полисахаридной цепи происходит при участии фермента амил-α-1,4-α-1,6-гликозил-трансферазы путем разрыва одной α-1,4-гликозидной связи и переноса олигосахаридного остатка от конца растущей цепи к ее середине с образованием в этом месте α-1,6-гликозидной связи Молекула гликогена содержит до 1 млн. остатков глюкозы, следовательно, на синтез расходуется значительное количество энергии. |
