Расчет шеелитового концентрата. 15 вариант. Металлургия легких металлов
 Скачать 1.55 Mb. Скачать 1.55 Mb.
|
|
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования ИРКУТСКИЙ НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ Заочно-вечерний факультет Кафедра металлургии цветных металлов Допускаю к защите Руководитель ___________ ФИО Процессы и аппараты технологии рафинирования легких металлов Вариант 15 Курсовая работа по дисциплине «Металлургия легких металлов» Выполнил студент группы МЦз-10-1 __________________ А.А. Иванов Курсовая работа защищена с оценкой ___________________________ Иркутск 2018 г. Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования ИРКУТСКИЙ НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ ЗАДАНИЕ НА КУРСОВУЮ РАБОТУ По курсу ____________«Металлургия легких металлов»_______________________________ Студенту __гр. МЦз-10-1 ______ ФИО. ________________________________________ (фамилия, инициалы) Тема работы Процессы и аппараты технологии рафинирования легких металлов Исходные данные Составить материальный баланс процесса электролиза для электролизера с предварительно обожженными анодами на силу тока 315 кА, принимая показатель выхода по току равным - 91 %. Рекомендуемая литература: 1. Манвелян М.Г., Ханамирова А.А. Обескремнивание щелочных алюминатных растворов. Изд-во АН АрмССР, 2003. — 300 с. 2. Производство глинозема. Учеб. пособие для вузов по спец. "Металлургия цв. металлов" / А.И. Лайнер, Н. И. Еремин, Ю.А. Лайнер, перераб. и доп. - М: Металлургия. 2005 - 344 с. 3. Беляев А. И. Металлургия легких металлов. Изд-во «Металлургия», 2002. – 368с. 4.Лайнер А.И., Еремин Н.И., Лайнер Ю.А., Певзнер И.З. Производство глинозема. 2-е изд. — М.: Металлургия, 2001. — 344 с. Графическая часть на ___________листах. Дата выдачи задания «___» ___________20___ г. Задание получил __________ ________________ подпись И.О. Фамилия Дата представления работы руководителю «____» ___________20___ г. Руководитель курсовой работы ______________ФИО СодержаниеСодержание 3 Введение 4 1 Рафинирование алюминия 6 1.1 Адсорбционное рафинирование 6 1.1.1 Рафинирование инертными газами 7 1.1.2 Рафинирование хлором 7 1.1.3 Рафинирование хлористыми солями 7 1.2 Неадсорбционное рафинирование 8 1.2.1 Ультразвуковое рафинирование 8 1.2.2 Действие на расплав постоянного электрического тока 10 1.2.3 Рафинирование в вакууме 12 1.2.4 Фильтрация 13 2 Рафинирование магния 14 2.1 Рафинирование флюсами 14 2.2 Рафинирование отстаиванием 16 2.3 Рафинирование титановой губкой 16 2.4 Рафинирование возгонкой и зонной плавкой 17 2.5 Электролитическое рафинирование 17 3 Рафинирование лития, бериллия, кальция, натрия, калия 19 4 Расчет материального баланса электролиза 20 4.1 Составление материального баланса 20 Заключение 23 Список использованных источников 24 ВведениеРафинирование металлов - очистка первичных (черновых) металлов от примесей. Черновые металлы, получаемые из сырья, содержат 96 – 99% основного металла, остальное приходится на примеси. Такие металлы не могут использоваться промышленностью из-за низких физико-химических и механических свойств. Примеси, содержащиеся в черновых металлах, могут представлять самостоятельную ценность. Различают 3 основных метода рафинирования: пирометаллургический, электролитический и химический. В основе всех методов лежит различие свойств разделяемых элементов: температур плавления, плотности, электроотрицательности и т.д. Для получения чистых металлов нередко используют последовательно несколько методов рафинирования. Пирометаллургическое рафинирование, осуществляемое при высокой температуре в расплавах, имеет ряд разновидностей. Окислительное рафинирование основано на способности некоторых примесей образовывать с О, S, Cl, F более прочные соединения, чем соединения основного металла с теми же элементами. Способ применяется, например, для очистки Cu, Pb, Zn, Sn. Ликвационное разделение основано на различии температур плавления и плотностей компонентов, составляющих сплав, и на малой их взаимной растворимости. Способ применяется для очистки чернового свинца от Cu, Ag, Au, Bi, очистки чернового цинка от Fe, Cu, Pb, при рафинировании Sn и др. металлов. При фракционной перекристаллизации используется различие в растворимости примесей металла в твёрдой и жидкой фазах с учётом медленной диффузии примесей в твёрдой фазе. Способ применяется в производстве полупроводниковых материалов и для получения металлов высокой чистоты (например, зонная плавка, плазменная металлургия, вытягивание монокристаллов из расплава, направленная кристаллизация). В основе ректификации, или дистилляции, лежит различие в температурах кипения основного металла и примеси. Очистка осуществляется в форме непрерывного противоточного процесса, в котором операции возгонки и конденсации удаляемых фракций многократно повторяются. Использование вакуума позволяет заметно ускорить прцесс. Способ применяется при очистке Zn от Cd, Pb от Zn, при разделении Al и Mg, в металлургии Ti и др. процессах. Вакуумная фильтрация жидкого металла через керамические фильтры (например, в металлургии Sn) позволяет удалить взвешенные в нём твёрдые примеси. При очистке стали в ковше жидкими синтетическими шлаками поверхность контакта между металлом и шлаком в результате их перемешивания значительно больше, чем при проведении рафинировочных процессов в плавильном агрегате; благодаря этому резко повышается интенсивность протекания десульфурации, дефосфорации,раскисления металлов, очищения его от неметаллических включений. Рафинирование стали продувкой расплава инертными газами используется для удаления из металла взвешенных частиц шлака или твёрдых окислов, прилипающих к пузырькам газа и флотируемых на поверхность расплава. Электролитическое рафинирование, представляющее собой электролиз водных растворов или солевых расплавов, позволяет получать металлы высокой чистоты. Применяется для глубокой очистки большинства цветных металлов. Электролитическое рафинирование с растворимыми анодами состоит в анодном растворении очищаемых металлов и осаждении на катоде чистых металлов в результате приобретения ионами основного металла электронов внешней цепи. Разделение металлов под действием электролиза возможно вследствие различия электрохимических потенциалов примесей и основного металла. Например, нормальный электродный потенциал Cu относительно водородного электрода сравнения, принятого за нуль, + 0,346, у Au и Ag эта величина имеет большее положительное значение, a y Ni, Fe, Zn, Mn, Pb, Sn, Co нормальный электродный потенциал отрицателен. При электролизе медь осаждается на катоде, благородные металлы, не растворяясь, оседают на дно электролитной ванны в виде шлама, а металлы, обладающие отрицательным электродным потенциалом, накапливаются в электролите, который периодически очищают. Иногда (например, в гидрометаллургии Zn) используют электролитическое рафинирование с нерастворимыми анодами. Основной металл находится в растворе, предварительно тщательно очищенном от примесей, и в результате электролиза осаждается в компактном виде на катоде. Химическое рафинирование основано на различной растворимости металла и примесей в растворах кислот или щелочей. Примеси, постепенно накапливающиеся в растворе, выделяются из него химическим путём (гидролиз, цементация, образование труднорастворимых соединений, очистка с помощью экстракции или ионного обмена). Примером химического рафинирования может служить аффинаж благородных металлов. Очистку Au производят в кипящей серной или азотной кислоте. Примеси Cu, Ag и др. металлов растворяются, а очищенное золото остаётся в нерастворимом осадке. Методы рафинирования легких металлов делят на адсорбционные и неадсорбционные. Первые нарушают равновесие металл-комплекс только в тех зонах расплава, через которые проходит адсорбент, вторые – во всем объеме. Поэтому они эффективнее. 1 Рафинирование алюминия1.1 Адсорбционное рафинированиеК адсорбционным методам относится обработка расплава газами и солями. Применяются инертные и химически активные газы. К числу первых относится азот. Он чаще других инертных газов применяется для рафинирования алюминиевых сплавов. Его действие основано на адсорбции и диффузии растворенных в расплаве других газов, в частности водорода. Если газонасыщенный сплав находится в контакте с атмосферой, не содержащей растворенного в металле газа, то газ будет выделяться из расплава. Вместе с водородом будут также адсорбироваться твердые неметаллические частицы, которые выплывают на поверхность ванны. Твердые частицы, которые при этом отрываются от водорода, оседают на дно. Однако продувка азотом не обеспечивает полной дегазации расплава: азот, пропускаемый через расплав под атмосферным давлением, способен адсорбировать объем водорода, равный 10 % собственного объема. Поэтому если не пропускать через расплав очень большой объем азота, то после дегазации остается определенное количество неудаленного водорода. В этом отношении значительно эффективнее действует аргон. В качестве химически активного вещества применяют газообразный хлор. В литературе встречаются указания на применение ряда хлорсодержащих соединений: четыреххлористых кремния, углерода, титана; широко применяют хлористые цинк, алюминий, марганец; исследован треххлористый бор. Наибольшее применение нашли хлор и хлористые соли цинка, марганца, алюминия. Сущность действия хлора состоит в образовании хлористого соединения алюминия и хлористого водорода, которые, находясь в расплаве в парообразном состоянии, выделяются на поверхность. На границе соприкосновения пузырька образовавшегося газа и расплава имеется разность парциальных давлений водорода внутри пузырька образовавшегося газа и в расплаве. Парциальное давление водорода стремится выровняться по всему объему пузырька образовавшегося газа, поэтому газ, растворенный в поверхностном по отношению к пузырьку слое расплава, начинает переходить в него. Этот процесс может продолжаться до выравнивания концентрации водорода в центре пузырька и в пограничном с ним слое расплава. Однако поскольку при продувании хлором пузырьки хлорида металла и соляной кислоты быстро выделяются в атмосферу, полного их насыщения водородом не происходит, что снижает эффективность рафинирования. По практическим данным исследования очистки алюминиевых расплавов следует, что рафинирование хлористым алюминием дает практически такой же эффект, что и рафинирование хлористым цинком, и обе соли по активности действия уступают хлору. Помимо химического состава рафинирующего вещества, на эффект очистки от примесей большое влияние оказывают такие факторы, как температура расплава, вязкость, размеры и скорость выделения рафинирующих газовых пузырьков. [1] 1.1.1 Рафинирование инертными газамиВ этих целях обычно применяют азот или аргон. Установка состоит из баллона с инертным газом, устройства для поглощения воды, манометра и кварцевой трубки. Все элементы соединены между собой резиновыми трубками. Процесс рафинирования ведут непосредственно в печах или в раздаточных тиглях. При этом газ с помощью кварцевой трубки вводят в расплав и перемещением трубки вдоль стенок печи стремятся обработать наибольший объем металла. Продолжительность рафинирования 7 – 10 минут, после чего с поверхности расплава снимают шлак и производят разливку. 1.1.2 Рафинирование хлоромУстановка для хлорирования состоит из баллона с хлором, осушительных склянок Тищенко с серной кислотой, ртутного манометра и кварцевой трубки. Все эти элементы установки соединены между собой стационарной стальной трубкой, а в местах, требующих подвижного соединения, - резиновой трубкой. Баллон с хлором и склянками обязательно устанавливают в изолированном помещении. Процесс хлорирования ведется в тигле с крышкой, имеющей отвод отходящих газов в боров. Над тиглем необходимо устанавливать вентиляционный кожух. Кварцевую трубку вводят в расплавленный металл таким образом, чтобы конец ее находился на расстоянии 100 – 150 мм от дна тигля. При достижении требуемой температуры металла вентиль баллона поворачивают примерно на ¼ оборота и наблюдают за прохождением хлора в склянках и изменением давления в манометре. По достижении давления в манометре 50 – 60 мм рт. ст. вентиль поворачивают с таким расчетом, чтобы давление повысилось до 100 мм рт. ст. Обработку хлором проводят при давлении около 100 мм рт. ст. Продолжительность рафинирования устанавливают в зависимости от качества шихтовых материалов. При сильно загрязненной шихте длительность рафинирования увеличивают, но не выше 10 – 12 минут, во избежание роста зерен. 1.1.3 Рафинирование хлористыми солямиДля этих целей обычно применяют хлористый цинк, хлористый марганец, реже хлористый алюминий и др. Перед применением хлористый цинк необходимо переплавить, т.к. он очень гигроскопичен и содержит много воды. Во избежание поглощения водяных паров хлористый цинк необходимо вводить в расплав еще горячим с помощью железного колокольчика, которым одновременно перемешивают сплав. Операцию рафинирования считают законченной после прекращения выделения из металла пузырьков газа. После рафинирования с поверхности расплава снимают шлак, сплав выдерживают не менее 5 – 10 минут и разливают по формам. Обычно в расплав вводят хлористого цинка не более 0,1 – 0,2 % от массы шихты, чтобы им не загрязнять сплавы. Взамен хлористого цинка можно применять хлористый марганец. Последний вводят в количестве 0,05 – 0,1 % к массе расплава. Работать с хлористым марганцем удобнее вследствие его меньшей гигроскопичности. Хлористый марганец перед употреблением достаточно просушить в сушильном шкафу при температуре 110 – 115 ºC, а затем хранить в герметически закрытой посуде. Дегазацию также можно осуществлять также хлористым алюминием. При разработке режимов рафинирования хлором и хлористыми солями необходимо учитывать большое влияние, которое оказывают на эффект их действия температура и вязкость сплавов. 1.2 Неадсорбционное рафинированиеК неадсорбционным методам относится обработка ультразвуком, постоянным электрическим током и в вакууме. Проблема удаления из расплава неметаллических включений становится все острее по мере увеличения емкости печей, перехода на газовый и мазутный обогрев отражательных печей при одновременном возрастании габаритов и требований, предъявляемых к отливкам. Все это вынуждает работать над созданием новых методов рафинирования, более эффективных, чем методы, основанные на адсорбции. Оптимальные результаты могут быть достигнуты при нарушении равновесия системы металл – газ – окись во всем объеме расплава, а не в отдельных участках. Это достигается с помощью ультразвука, постоянного электрического тока и вакуума, т.е. неадсорбционных методов рафинирования. [1] 1.2.1 Ультразвуковое рафинированиеПри прохождении упругих колебаний через жидкую среду (расплав) наблюдается явление кавитации, приводящее к разрыву сплошности в жидкой фазе и образование пустот, в которые устремляется растворенный в жидкости (расплаве) газ. Вследствие этого упругие колебания звуковой и особенно ультразвуковой частоты способствуют формированию зародышей газовых пузырьков и стимулируют их дальнейший рост в жидкой фазе и коагуляцию до размеров, обеспечивающих активное выделение газа из жидкости (расплава). Упругие колебания, получаемые при помощи магнитострикционного излучателя частотой 8 – 10 кГц, были использованы для дегазации оптического стекла. Ультразвуком обрабатываются расплавы металла, при этом применяется способ дегазации расплавов путем наложения постоянного магнитного поля на высокочастотное поле индукционной печи, в которой расплавляют металл. При таком способе обработки в расплаве в результате электродинамических сил возникают интенсивные колебания, что обеспечивает полную дегазацию расплава за 30 – 60 минут без интенсивного перемешивания. Для получения упругих колебаний ультразвуковой частоты используется магнитострикционный способ. В качестве источника высокой частоты применяют генератор самовозбуждения типа УЗГ мощностью 8 кВт и частотой 20 кГц, а для преобразования электромагнитных колебаний в механические – магнитострикционный преобразователь типа ПМС-7, набранный из штампованных отожженных пластин пермендюра толщиной 0,2 мм. При пропускании через обмотку магнитного преобразователя переменного тока от генератора ВЧ и постоянного подмагничивающего тока от выпрямителя вибратор изменяет свои линейные размеры в такт высокочастотным колебаниям тока. В конструкцию преобразователя было введено усовершенствование с целью повышения коэффициента полезного выхода энергии упругих колебаний. Веденный в конструкцию сильфон прижимает резиновую прокладку к неработающему торцу вибратора и создает условия демпфирования колебаний нерабочего торца вибратора, который через резиновую прокладку граничит с воздухом. Таким образом, большая часть упругой энергии, вырабатываемой в вибраторе, полезно используется для обработки расплава упругими колебаниями (см. рисунок 1). 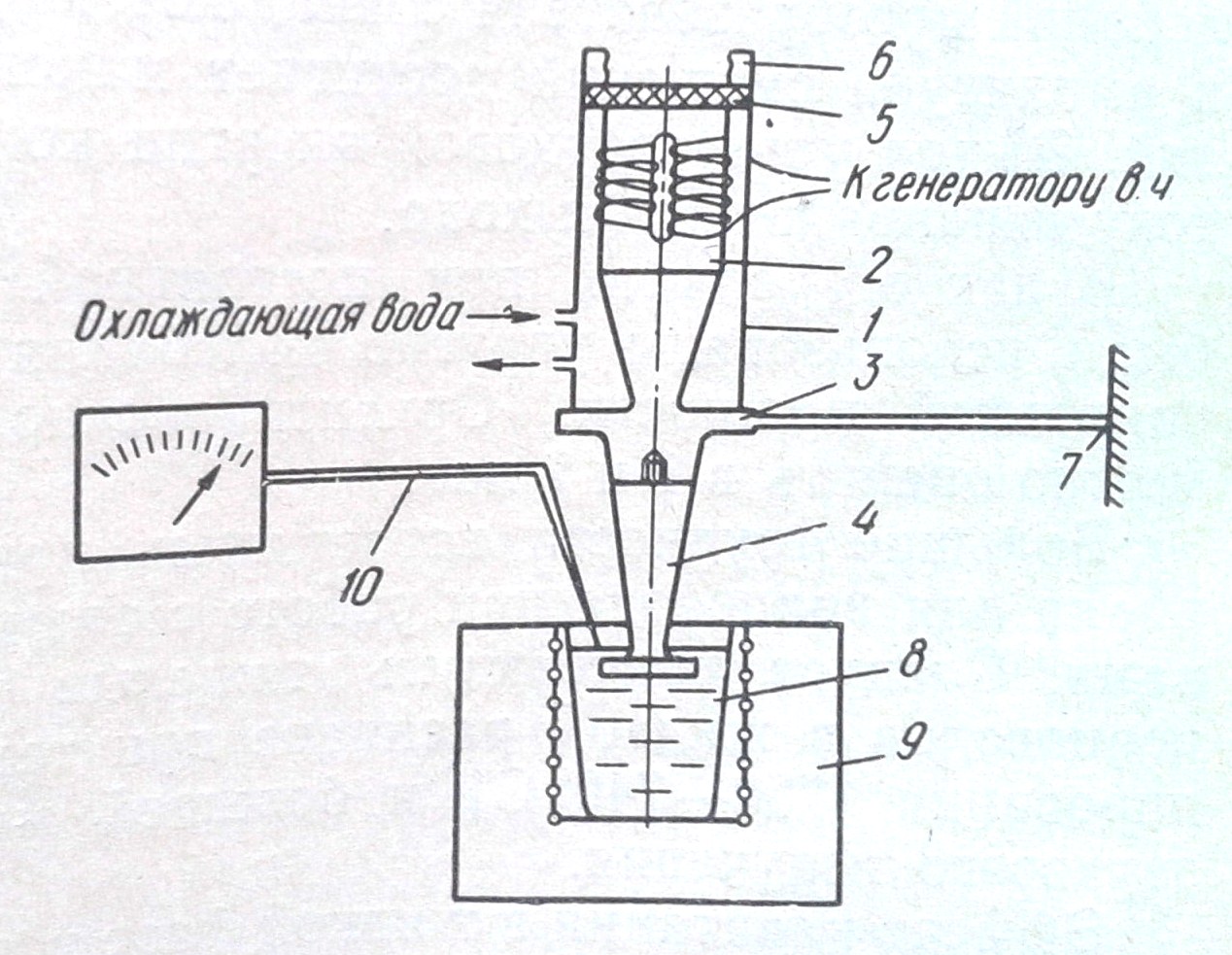 1 – кожух; 2 – магнитный преобразователь; 3 – концентратор; 4 – вибратор; 5 – резиновый амортизатор; 6 – сильфон; 7 – крепление узла колебаний; 8 – тигель; 9 – печь; 10 – термопара Рисунок 1 – Схема введения упругих колебаний в расплав Этот способ перспективен, т.к. обеспечивает высокий уровень дегазации и удаление из расплава твердых включений. Для рафинирования алюминия применяется промышленный агрегат УЗД-200 (см. рисунок 2). При рафинировании рабочую головку агрегата подводят к печи, с поверхности расплава снимают окисную пленку, и рабочую головку опускают до касания торцами волноводов поверхности расплава. Волноводы предварительно прогревают, включают напряжение и проводят рафинирование. После этого расплав выдерживают 10 – 15 минут, снимают шлак и проводят разливку. 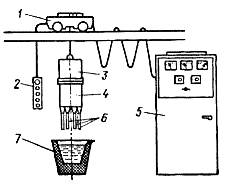 1 – тельфер; 2 – пульт; 3 – блок переключения преобразователей; 4 – головка с преобразователями; 5 – генератор; 6 – излучатели; 7 – тигель с расплавом. Рисунок 2 – Принципиальная схема промышленного ультразвукового дегазатора УЗД-200 1.2.2 Действие на расплав постоянного электрического токаСчитается, что газы при переходе в расплав находятся в атомарном состоянии, но также они могут быть ионизированы. Исходя из этого, проводились испытания по очистке расплава от газов постоянным электрическим током (см. рисунок 3). Дегазация расплава постоянным электрическим током служит подтверждением ионизации водорода в расплаве. Поэтому отсутствие дегазации считается результатом низкой степени ионизации водорода. При этом наблюдается неравномерное распределение водорода в расплаве: у катода газосодержание возрастает, а у анода падает. В целом применение постоянного электрического тока положительно влияет на очистку расплавов. При этом на рафинирование оказывают влияние температура расплава и плотность тока. 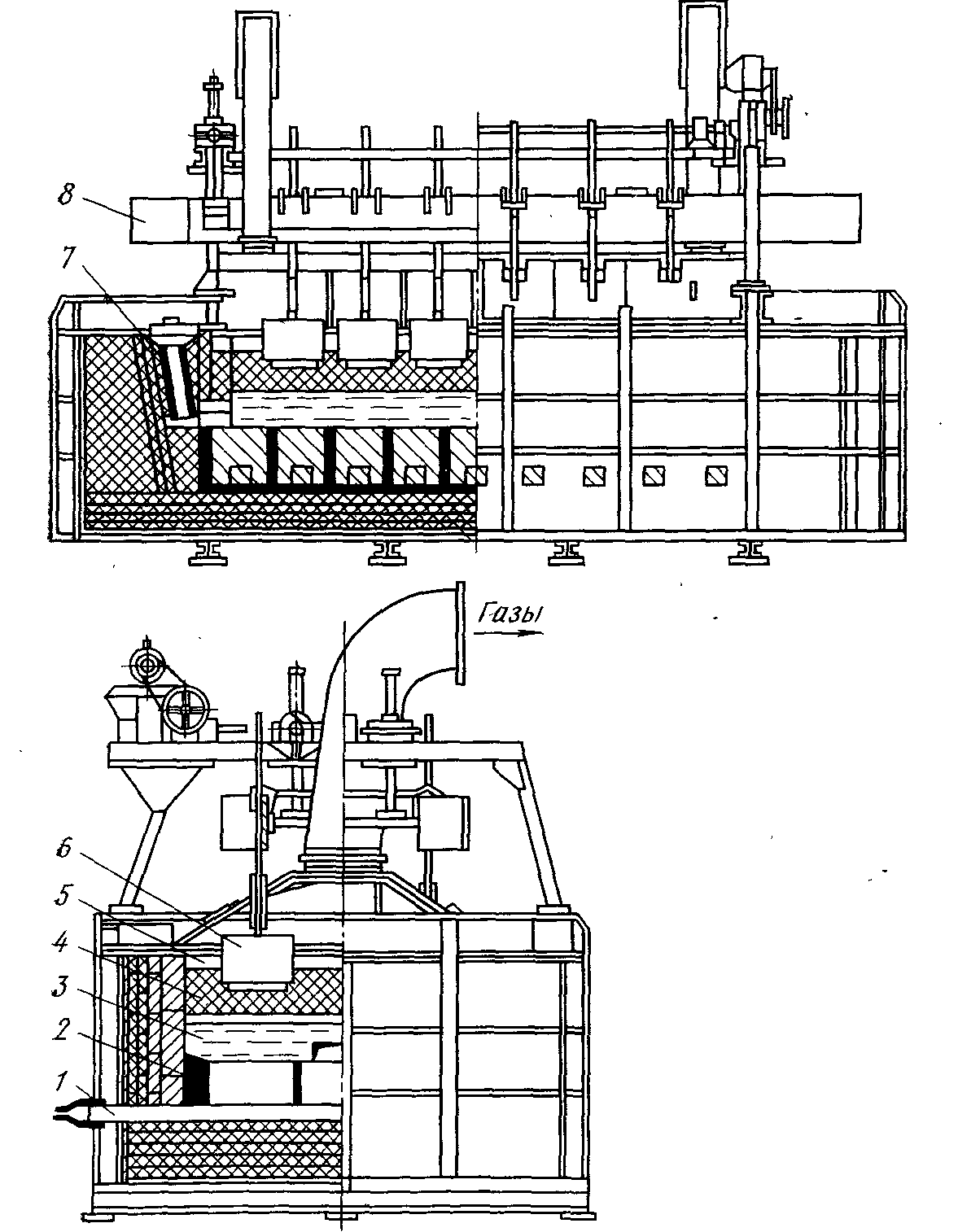 1 – токоподвод к аноду; 2 – угольная футеровка; 3 – анодный сплав; 4 – электролит; 5 – рафинированный алюминий; 6 – графитированный электрод; 7 – загрузочный карман; 8 – шинопровод. Рисунок 3 – Электролизер для рафинирования алюминия 1.2.3 Рафинирование в вакуумеОбработка в вакууме позволяет удалять из расплава алюминия водород и окисные включения более эффективно, чем методы, основанные на адсорбции. Применение же вакуумирования с использованием флюса позволяет резко уменьшить два фактора, препятствующих удалению водорода: давление внешней газовой фазы и поверхностное натяжение окисной пленки. Благодаря этому величина парциального давления примесного газа, необходимая для его удаления из расплава, значительно уменьшается, уменьшается и необходимый размер радиуса пузырька. Для вакуумирования могут быть применены вакуумные камеры, куда помещают тигли с расплавом или вакуумные раздаточные печи (см. рисунок 4, 5). Продолжительность вакуумирования может составлять 2 – 6 минут. 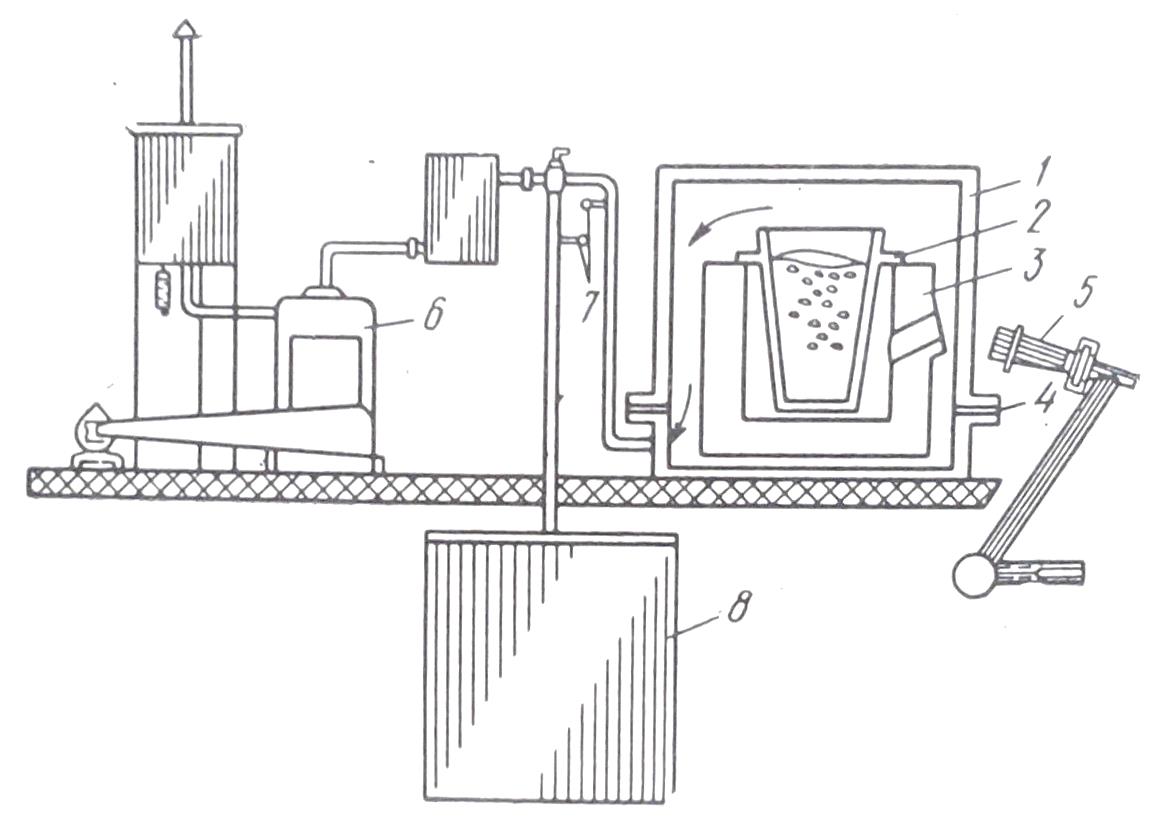 1 – вакуумная камера; 2 – тигель с расплавом; 3 – печь; 4 – прокладка; 5 – газовая горелка; 6 – вакуумный насос; 7 – вакуумметры; 8 – рессивер Рисунок 4 – Схема установки для вакуумирования (ВДК-1)  1 – вакуумная раздаточная печь ВРП-1; 2 – вакуумметр; 3 – вентиль; 4 – фильтр вакуумной системы; 5 – вакуумный насос; 6 – крышка; 7 – экран Рисунок 5 – Схема установки для вакуумирования: При вакуумировании сплава происходит активное удаление газовых и твердых включений. Увеличение времени вакуумирования приводит к снижению пористости и повышению плотности, а малые добавки флюса, засыпаемые на поверхность расплава, способствуют лучшей очистки. Рафинирование проводится следующим образом: расплав из плавильной печи заливают в раздаточный тигель, который помещают в вакуумную камеру или в тигель печи. На поверхность расплава рекомендуется насыпать слой сухого рафинирующего флюса. Затем расплав выдерживают под давлением 10 – 15 минут, и после отстаивания разливают. 1.2.4 ФильтрацияФильтрация состоит в том, что расплав перед заливкой из печи в раздаточные тигли или в формы пропускают через специальные фильтры. Фильтры в зависимости от характера их действия делят на две группы: инертные (сетчатые) и активные. В сетчатых фильтрах твердые неметаллические включения, размеры которых больше размера ячеек фильтра, задерживаются механически. Эффективность очистки тем выше, чем меньше размеры ячеек фильтра. Активные фильтры, в которых задержка неметаллических включений является результатом в основном адсорбции, изготавливают из огнеупорной крошки, пропитанной рафинирующим флюсом. В то время, как инертные делают из стеклоткани. 2 Рафинирование магнияИзвлекаемый из электролизеров магний содержит более 25 различных примесей (Fe, Si, Ni Mn и др.), концентрация их колеблется в пределах 0,04 до 10 %. Существует несколько способов рафинирования, наиболее распространены следующие: рафинирование флюсами, отстаивание, металлотермические методы, электролитическое рафинирование, зонная плавка, вакуумная возгонка, фильтрация. 2.1 Рафинирование флюсамиДля рафинирования применяют флюсы с различным химическим составом, который определяет его назначение. В основном флюсы разделяют на рафинирующие (бариевые; ВИ-2) и покровные (ВИ-3; бесхлоридные), хотя последние одновременно обеспечивают процессы очистки металла от некоторых металлических примесей. Покровные флюсы, расплавляясь на поверхности металла, образуют плотный слой, хорошо защищающий металл от взаимодействия с воздухом и парами воды. Оксиды, нитриды магния и другие твердые включения поглощаются флюсом из-за лучшего смачивания, чем металлом. Для улучшения смачиваемости металла во флюсы вводят CaF2. Механизм рафинирования состоит в том, что флюс поглощает твердые включения, взаимодействует с некоторыми металлическими примесями и погружается на дно емкости, в которой производится рафинирование. Для реализации описанных механизмов флюсы должны обладать следующими свойствами: температура плавления ниже, чем температура плавления металла; не должны взаимодействовать с магнием, его сплавами, футеровкой; не разлагаться; не испаряться; не отравлять окружающую среду; хорошо смачивать твердые включения. Для очистки применяют тигельные электропечи сопротивления. Можно использовать также тигельные индукционные печи промышленной частоты (см. рисунок 6).  1 – кожух печи; 2 – фасонный шамот; 3 – асбест; 4 – шамотная футеровка; 5 – нихромовые нагреватели; 6 – тигель; 7 – крышка; 8 – механизм подъема и поворота крышки; 9 – выводы нагревателей; 10 – токовыводящие клеммы; 11 – защитная коробка; 12 – заземление; 13 – желоб для стока металла Рисунок 6 – Стационарная магниевая электропечь СМТ-1: В тигель загружают рафинирующий флюс, при температуре 690 ºC заливают магний вакуум-ковшом. Металл перемешивают вместе с флюсом, нагревают (до 720 ºC) и отстаивают в течение 1 – 2 часов. Разливают на чушку. 2.2 Рафинирование отстаиваниемНа заводах наибольшее распространение получили печи непрерывного рафинирования (см. рисунок 7). Очистка осуществляется в результате отстаивания. Окисление исключено, т.к. металл не соприкасается с воздухом. Температура металла в печи – 700 – 720 ºC. Заливку металла в печь производят вакуумным ковшом, извлечение – электромагнитным насосом.  1 – разливочный конвейер; 2 – электромагнитный насос; 3 – печь; 4 – теплоизолирующие трубки; 5 – футеровка; 6 – загрузочный патрубок; 7 – нагревательные элементы; 8 – заборный патрубок для магния; ВУ и НУ – соответственно верхний и нижний уровни расплава Рисунок 7 – Литейный комплекс для непрерывного рафинирования и разливки магния Греющим сопротивлением служит расплавленный флюс. Электрический ток подводится к расплаву через электроды, вмонтированные в кладку печи. Печь состоит из двух камер, разделенных керамической перегородкой, в нижней части которой имеется переточное отверстие. Донные части камер заполнены солевым расплавом. Нагрев осуществляется трубчатыми солевыми нагревателями, опущенными в металл. Заливка металла в камеру производится через стальную трубку, извлечение металла – из другой камеры. Зеркало металла распылением укрывают покровным флюсом. Устройством грейферного типа, установленным на мостовом кране, периодически извлекают накопившийся на поду печи шлам. Рафинированный металл подают на разливочные машины. 2.3 Рафинирование титановой губкойВ тигель при температуре 700 – 720 ºC загружают калиево-натриевый флюс, в солевой расплав постепенно вводят титановую губку. Эта операция предотвращает окисление титановой губки. Затем заливают магний и интенсивно перемешивают. После отстаивания металл разливают. Механизм рафинирования основан на нерастворимости титана в магнии и образовании с примесями нитридов, оксидов титана, интерметаллидов или твердых растворов. Не менее эффективна очистка магния низшими хлоридами титана, которые вводят в расплав в смеси с хлоридами щелочных металлов. 2.4 Рафинирование возгонкой и зонной плавкойЭти методы используют для очистки магния от металлических и солевых примесей. Очистка возгонкой основана на различии давления паров магния и примесей. Процесс ведут в стальных ретортах. Нижняя часть ее обогревается, верхняя – охлаждается. Пары магния и более летучих, чем он, примесей осаждаются в конденсаторе в виде крупных кристаллов. Примеси, имеющие низкое давление паров при рабочей температуре, остаются в донной части реторты. После окончания процесса отгонки основной металл из конденсатора извлекают, переплавляют и разливают. 2.5 Электролитическое рафинированиеЭлектролитическое рафинирование магния проводят в электролизере (см. рисунок 8). Стальной кожух электролизера футерован магнезитовым кирпичом, под ванны выполнен из графитовых блоков. К поду подключен положительный полюс внешнего источника тока. На поду располагается рафинируемый магний, утяжеленный медью или цинком – анодный сплав. Выделяющийся на катоде металл образует третий слой. При электролизе (температура 700 – 720 ºC, напряжение на ванне 4,0 – 4,5 В) магний анодно растворяется на катоде, примеси более электроположительные – не растворяются и накапливаются в анодном сплаве, а примеси более электроотрицательные также растворяются, но на катоде не разряжаются. Электролитическое рафинирование обеспечивает почти такую же чистоту металла, как и возгонка, но процесс – непрерывный и более дешевый. [2]  1 – поворотный кронштейн; 2 – анодный сплав; 3 – графитовый анод; 4 – карман для загрузки анодного металла; 5 – стальной передвижной катод Рисунок 8 – Схема электролизера для рафинирования магния 3 Рафинирование лития, бериллия, кальция, натрия, калияЧерновой литий содержит такие примеси, как Na, K, Mg, Ca, Al, Si, Fe, а также оксиды и нитриды лития. Рафинирование металла проводят несколькими методами. Нитриды и оксиды лития при повышенных температурах растворяются в металле, а при охлаждении примерно до 250 ºC почти полностью выпадают из раствора. Это свойство используют для очистки металла от оксидов и нитридов фильтрацией при указанной температуре. Дальнейшую очистку производят погружением в расплав титана, циркония или иттрия, которые имеют большее сродство к кислороду, чем литий, и выдержкой металла-восстановителя в нем при 816 ºC в течение 50 – 100 часов. Металлические примеси удаляют вакуумной дистилляцией, ректификацией или зонной плавкой. При производстве бериллия электролизом примеси хлорируются одновременно с хлорированием брикетированного оксида бериллия с восстановителем при температуре 700 – 800 ºC в электрических шахтных печах. При получении металла металлотермическим способом бериллий очищают дополнительной переплавкой в индукционных печах от шлаковых включений и снижают содержание примеси магния. [2] Главное применение металлического кальция – это использование его как восстановителя при получении металлов, чистый металлический кальций широко применяется в металлотермии при получении редких металлов. Металлический калий – материал для электродов в химических источниках тока. Сплав калия с натрием находит применение в качестве теплоносителя в ядерных реакторах. В больших масштабах, чем металлические кальций и калий, находят применение их соединения. Калий и кальций в настоящее время получают путем электролиза, в результате этого металлы получаются достаточной чистотой в области их применения и, чаще всего, дополнительного рафинирования не требуют. Полученный в результате электролиза натрий-сырец содержит сравнительно большое количество неметаллических и металлических примесей. Наиболее эффективный способ очистки – фильтрация, основанная на малой растворимости примесей при температуре на 10 – 50 ºC выше температуры плавления натрия. Фильтрацией при этих температурах удается удержать на сетчатых или пористых фильтрах большую часть примесей. [2] 4 Расчет материального баланса электролизаВ материальном балансе определяется расход сырья для производства алюминий-сырца. Глинозем. Для электролизеров с обожженными анодами удельный расход глинозема на 1т алюминий-сырца принимаем 1920 кг (Al2O3). Фтористые соли. Удельный расход свежего криолита принимаем равным 44,91 кг на 1т алюминий-сырца. Такая величина учитывает расход криолита на пропитку футеровки электролизера. Помимо свежего криолита в электролиз подают регенерированный криолит. Обожженные аноды. По практическим данным общий удельный расход анодов 560 – 580 кг (вместе с огарками). Без огарков удельный расход 415 – 453 кг. По данным ИркАЗа удельный расход анодов 550 кг на 1т алюминий-сырца, а выход огарков – 140 кг. 4.1 Составление материального балансаРасчет ведется на 1 час работы электролизера при условии нормального ведения технологического процесса. Сначала рассчитаем суточную производительность электролизера, исходя, что заданная сила тока I = 315 кА, а выход по току = 91 %. P = I qm m 24 10-3, где qm – электрохимический эквивалент Al, г/Ачас. P = 315000 0,3354 0,91 24 10-3 = 2018 кг/сут. Тогда в час количество алюминий сырца составит: 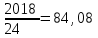 кг – часовая производительность электролизера. кг – часовая производительность электролизера.Приход сырья. Глинозем: 1,92 84,08 = 161,43 кг/час. Фтор. соли: (0,0091 + 0,00572) 84,08 = 1,24 кг/час. Аноды: 0,55 84,08 = 46,24 кг/час. Огарки: 0,14 84,08 = 11,77 кг/час. Расход сырья. Теоретически рассчитанный расход глинозема на производство 1 кг Al равен 1,89, тогда потери глинозема составят: (1,92 – 1,89) 84,08 = 2,52 кг/час. Расход анодов связан с окислительными процессами с выделением угарного и углекислого газов. Для расчета количества углерода, который окисляется в процессе электрохимического разложения глинозема примем состав анодных газов следующим: CO2 – 70 %, CO – 30 %. При получении 1 кг алюминий-сырца выделяется: 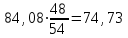 кг/час кислорода, кг/час кислорода,где 48 и 54 – количество O2 и Al соответственно в глиноземе. Из этого кислорода перейдет в состав CO2 и CO: 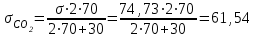 кг/час; кг/час;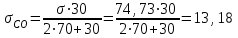 кг/час; кг/час;где (2 70 + 30) – содержание кислорода в CO2 и CO. Тогда количество углерода, связанного в CO2 и CO: 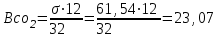 кг/час; кг/час;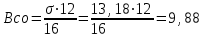 кг/час. кг/час.Таким образом, при получении 61,17 кг/час алюминий-сырца выделяется: CO2 = 61,54 + 23,07 = 84,61 кг/час; CO = 13,18 + 9,88 = 23,06 кг/час. Потери обожженных анодов связаны и с отходящими газами коксования, и с механическими потерями, и составляют (по практическим данным): ОА-потери = 0,55 84,08– (11,77 + 23,08 + 9,88) = 1,51 кг/час. Потери фтористых солей принимаем равными приходу фтористых солей, т.к. в процессе электролиза они теоретически не расходуются. Таблица 1 - Материальный баланс процесса электролиза
ЗаключениеТаким образом, можно отметить, что методы рафинирования в металлургии легких металлов схожи между собой, и можно выделить несколько применяющихся чаще и действующих эффективнее. [3] Окислительное рафинирование Окислительное рафинирование - самый распространенный способ очистки металлов от примесей. Основная идея метода - окисление вредных и излишних примесей и перевод их в виде оксидов в оксидную или газовую фазу, не растворяющуюся в металле. Специфика процессов окислительного рафинирования состоит в том, что продукты реакции (реагенты) находятся в различных фазах, либо разделены промежуточными фазами. Ликвационное рафинирование. Ликвация - нарушение однородности расплава, протекающее в жидком или затвердевающем металле. При этом происходит обеднение компонентами одних участков объема расплава и обогащение других. Причем чем больше интервал кристаллизации, тем больше степень ликвации компонентов расплава. Кристаллизационное рафинирование Для получения особо чистых материалов широко используются так называемые кристаллизационные методы рафинирования. Как правило, они применяются на конечной стадии рафинирования с целью удаления из расплава очень малых количеств примесей. Оценка эффективности очистки рафинируемого металла от примесей кристаллизацией осуществляется на основе представлений о равновесном и эффективном коэффициенте распределения. Электролитическое рафинирование. Теория электролитического осаждения и рафинирования основывается на явлениях совместного разряда ионов. Для общего суждения о порядке разряда катионов на катоде или их образования на аноде служит ряд напряжений: чем больше величина его равновесного электродного потенциала, тем вероятнее его разряд на катоде и, следовательно, менее вероятно анодное растворение соответствующего металла. При электролитическом рафинировании металлов важна глубокая очистка электролита от примесей способом предварительного электролиза. Список использованных источниковАльтман М.Б. Металлургия литейных алюминиевых сплавов: уч. издание / М.Б. Альтман; - М.: «Металлургия», 1972. – 152 с. Москвитин В.И. Металлургия легких металлов: учебник для вузов / В.И. Москвитин, И.В. Николаев, Б.А. Фомин; - М.: Интермет Инжиниринг, 2005. – 416 с. Г.Г. Минеев, Т.С. Минеева, И.А. Жучков, Е.В. Зелинская. Теория металлургических процессов: учебник / под общ. ред. Г.Г. Минеева. – Иркутск: Изд-во ИрГТУ, 2010. – 524 с. Беляев А.И. Металлургия легких металлов. – М.: «Металлургия», 1970. – 365 с. Лакерник М.М., Севрюков Н.Н. Металлургия цветныхметаллов. – М.: «Металлургиздат», 1957. – 537 с. Электрометаллургия алюминия: учеб. пособие / И.С. Гринберг, В.Г.Терентьев, В.И. Чалых [и др.].– Иркутск: Изд-во ИрГТУ,2009. –350 с. Производство алюминия и магния и проектирование цехов: метод. указания по выполнению курс. проекта [электронный вариант] / сост. Немчинова Н.В. – Иркутск: Изд-во ИрГТУ, 2012. |
