Лабораторная работа аналитическая химия. лаба 1-2. Методические указания по химии для студентов дневной и заочной форм обучения
 Скачать 2.84 Mb. Скачать 2.84 Mb.
|
|
МИНИСТЕРСТВО ОБРАЗОВАНИЯ НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ КазанскИЙ государственнЫЙ АРХИТЕКТУРНО-СТРОИТЕЛЬНЫЙ УНИВЕРСИТЕТ Кафедра химии и инженерной экологии в строительствеТЕХНИКА ЛАБОРАТОРНЫХ РАБОТ Методические указания по химии для студентов дневной и заочной форм обучения Казань 2015 УДК 543 ББК24.4 075 Техника лабораторных работ: Методические указания по химии для студентов 1- 3 курса дневной и заочной форм обучения /Сост. Н. Н. Комлева, Казань: КГАСУ, 2015.- 33 с.Печатается по решению Редакционно – издательского совета Казанского государственного университета архитектурно – строительного университета Методические указания содержат описание лабораторного химического оборудования, посуды и различных операций, которые приходится проводить при выполнении лабораторных работ по химии. Даны рекомендации по технике безопасности при выполнении химического эксперимента. Рецензент кандидат технических наук, доцент кафедры технологии строительных материалов и конструкций КГАСУ Г.Г. Ушакова © Казанский государственный архитектурно-строительный университет, 2015 © Комлева Н.Н., 2015 Порядок работы в химической лаборатории Студенты допускаются к работе в лаборатории практикума по аналитической химии только после инструктажа по технике безопасности и получения зачета по правилам работы в химической лаборатории и техники безопасности. Студенты обязаны расписаться в том, что они ознакомлены с правилами техники безопасности работ и обязуются их выполнять. Другим обязательным условием допуска к работе является теоретическая подготовленность студентов к предстоящей работе. В лаборатории запрещается курить, принимать пищу, входить в верхней одежде, шуметь. Правила безопасности Перед началом лабораторной работы необходимо внимательно ознакомиться с заданием, оборудованием, реактивами и правилами безопасности при выполнении данного задания. Химические реакции проводят с таким количеством реагентов указанной концентрации в тех приборах и посуде, которые указаны в руководстве. При этом необходимо решить вопрос о том (если это специально не указано в руководстве), где следует проводить опыт: на лабораторном столе или в вытяжном шкафу. На химическом лабораторном столе выполняются опыты, которые не представляют опасности для работающего. В вытяжном шкафу выполняются все опыты с ядовитыми, неприятно пахнущими веществами, с концентрированными кислотами и щелочами. Эти вещества должны находиться в вытяжном шкафу и выносить их на лабораторные столы запрещается. При работе с ядовитыми веществами в вытяжном шкафу, в целях более эффективного действия вентиляции, дверцы вытяжного шкафа поднимаются на 1/2 - 1/3 их подъёма. При работе с особо опасными веществами (твердые щелочи, фосфорный ангидрид, соединения мышьяка, фтористый водород, белый фосфор и др.) необходимо надеть защитные очки, а на руки - резиновые перчатки. Работа с легковоспламеняющимися веществами проводится в специальных помещениях, в которых не используется открытый огонь. Разбавление концентрированных кислот производится в вытяжном шкафу в тонкостенной химической посуде, при этом кислота вливается в воду небольшими порциями и при перемешивании. Особую осторожность нужно соблюдать при разбавлении концентрированной серной кислоты. Работы с металлической ртутью производить только на специальном подносе для ртути. Случайно пролитую ртуть необходимо тщательно собрать во избежание хронического отравления ртутью. При работе с электроприборами (электрические плитки, муфельные печи, сушильные шкафы и др.) обращать внимание на их исправность, правильную изоляцию контактов, заземление. Не использовать приборы с оголёнными контактами, неисправными вилками. При проведении опытов нельзя отвлекаться от основной работы и оставлять приборы без наблюдения. Запрещается исследовать запах газа, выделяющегося при реакции, непосредственно из реакционного сосуда. Нужно осторожным движением руки направить на себя воздух с примесью этого газа. Правила пользования реактивами, посудой, правила нагревания 1) Все реактивы, посуда, приборы, находятся в лаборатории в определённых местах. Растворы находятся в склянках, а сухие вещества – в материальных банках, на полках лабораторных столов. Концентрированные кислоты и щёлочи, а также неприятно пахнущие и ядовитые вещества – в вытяжном шкафу. Склянки и банки имеют с двух сторон четкие надписи формул. Посуда (стаканы, колбы, воронки и др.) находятся в шкафах лабораторных столов. Для пробок, зажимов, держалок, газоотводных трубок, лапок и др. отведены верхние ящики лабораторных столов. Необходимо ознакомиться и запомнить расположение всех этих предметов в лаборатории. После работы посуда и другие приспособления, приведены в порядок, складываются на свои места. Приборы либо в готовом виде выставляются на лабораторные столы, либо собираются из составных частей самими студентами. 2)Если необходимо провести пробирочную реакцию с растворами веществ, то при помощи пипетки, укрепленной в пробирке, закрывающей склянку (рис 1.), отбирается небольшое количество раствора и вводиться в пробирку. При этом нельзя глубоко опускать пипетку в пробирку и касаться стенок пробирки кончиком пипетки. Положение пробирки и пипетки указано на рис. 2. 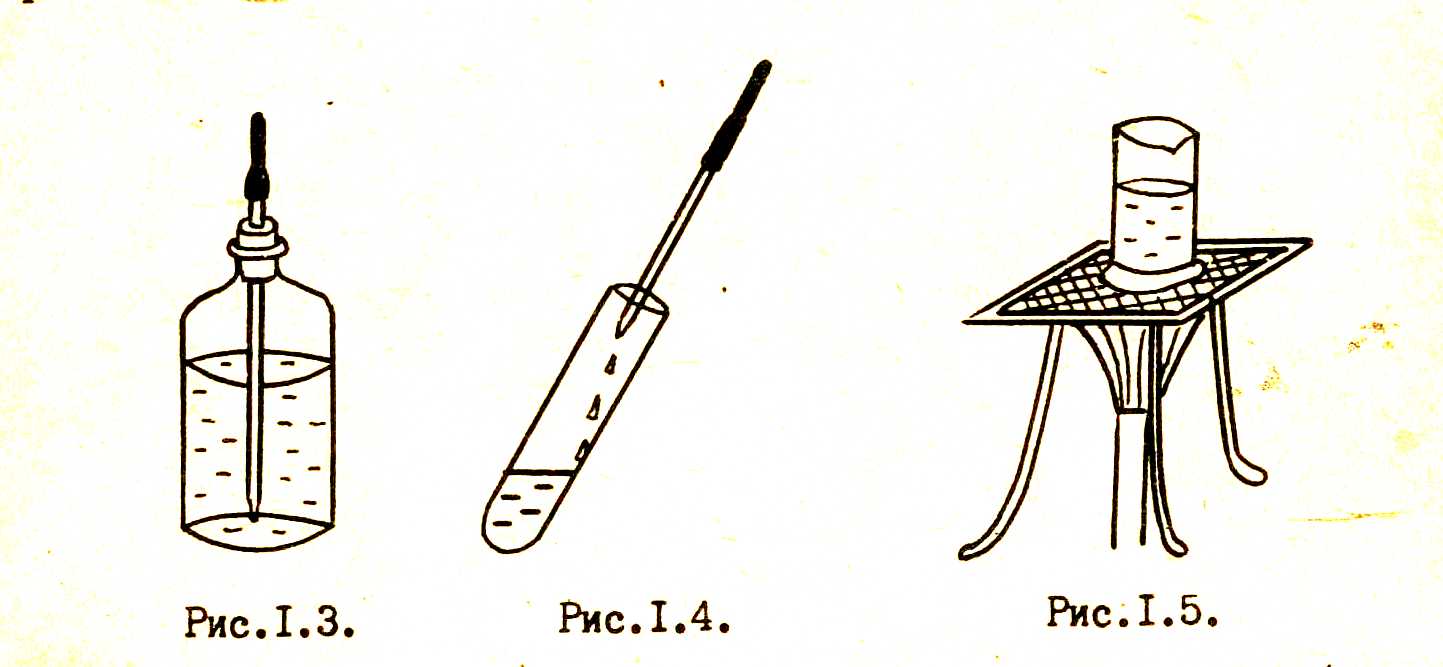 Рис. 1 Рис. 2 Рис. 3 Если в руководстве не указаны количества веществ, необходимых для выполнения опыта, то брать их нужно в малом количестве (1/6 объёма пробирки). Если раствора окажется в пробирке больше, чем нужно, то обратно в склянку этот раствор не выливать! 3)При работе с сухими веществами необходимо брать их специальной ложечкой или шпателем, который после употребления тщательно обтереть фильтрованной бумагой и только тогда можно брать другой реактив. Если в руководстве не указано количество сухого вещества, то брать его нужно в малом количестве (должно закрыть дно пробирки). Если сухого реактива оказалось несколько больше, то его избыток обратно в склянку не высыпать! 4)При нагревании раствора, содержащегося в пробирке, необходимо соблюдать следующие правила: пробирка вноситься в пламя при помощи специального держателя; отверстие пробирки должно быть направлено в сторону от себя и от других работающих; необходимо производить легкое перемешивание жидкости в пробирке, осторожно встряхивая её. 5)При нагревании сухого вещества, содержащегося в пробирке, соблюдается вышеуказанные правила, за исключением последнего. 6)При нагревании большого количества жидкости в стакане, колбе или другой посуде необходимо соблюдать следующие правила: насухо вытереть внешние стенки сосуда; нагрев производить не на голом огне, а поставить сосуд с жидкостью на асбестированную сетку (рис. 3); не наклоняться над сосудом, чтобы в лицо не попали брызги жидкости; перемешивание жидкости производить при помощи стеклянной палочки, не касаясь стенок сосуда, чтобы не разбить его. 7)Растворы, осадки, содержащие соединения серебра и других редких металлов, ни в коем случае не выливать в канализацию, а сливать в специальные сосуды для сбора остатков этих солей. Все эти растворы, осадки в дальнейшем регенерируются, чтобы не терять соединения дорогостоящих и редких металлов. 8) Студенты обязаны соблюдать в лаборатории чистоту и порядок, следить за своим рабочим местом, после окончания работы мыть посуду и приводить в порядок приборы. Группа на каждое занятие выделяет дежурного, который помогает преподавателю и лаборанту обеспечить порядок и безопасность работы в лаборатории. Оказание первой помощи в лаборатории. При небрежной работе и не соблюдении правил техники безопасности в лаборатории аналитической химии возможны следующие поражения: легкое отравление хлором, сероводородом, бромом, окисью углерода и др., легкие ожоги от нагревательных приборов, порезы стеклом, поражения концентрированными кислотами и щелочами. Во всех случаях поражений необходимо немедленно обратиться к преподавателю или лаборанту. В лаборатории имеются все средства первой помощи, и чем раньше они будут применены, тем меньше последствий останется у пострадавшего. 1. Попавшую на лицо или на руку кислоту тотчас смыть сильной струёй воды. Если на кожу в довольно большом количестве попала концентрированная серная кислота, то сначала её нужно удалить тампоном из ваты или марли, затем пораженное место вымыть большим количеством воды. Затем на пораженное место наложить повязку из ваты, смоченный разбавленным раствором соды. 2. Попавшую на лицо или руки щелочь смыть сильной струёй воды (пока кожа не перестанет быть скользкой) и наложить повязку с разбавленным раствором борной кислоты. 3. Обожженную горячими предметами кожу смочить крепким раствором перманганата калия. 4. В случае попадания белого фосфора на руки пораженное место обработать 2%-ым раствором сульфата меди. 5. При отравлении хлором, бромом, сероводородом и др. немедленно вывести пострадавшего на воздух. Лабораторная химическая посуда и приборы Химическая посуда, используемая при анализе. Химическую посуду, предназначенную для работы в аналитической лаборатории, можно условно разделить на две группы: посуда общего назначения и посуда специального назначения. К посуде общего назначения относят ту, которая обязательно присутствует в лаборатории и без которой нельзя провести многие работы по анализу. Это - пробирки, стаканы, колбы, воронки простые и делительные, колбы Бунзена Эрленмейера (конические), холодильники и др. К посуде специального назначения относят: аппарат Киппа, склянки Тищенко, дефлегматоры, пикнометры, ареометры, приборы для определения температур плавления и кипения и др. К мерной посуде относят: мерные цилиндры, пипетки и бюретки, мерные колбы. Аппарат Киппа (рис. 4) – прибор для получения газов (HCl и др.). Разборку, промывку и зарядку аппарата Киппа проводят под тягой. Ареометры (рис. 5) – приборы для определения плотности жидкости. Различают ареометры для жидкости легче воды и для жидкости тяжелее воды. У ареометров первого типа отсчет шкалы производиться от 1,000 до 0,700, а у арометров второго типа – от 1,000 и выше. Изменения плотности ареометром проводят при 200С. 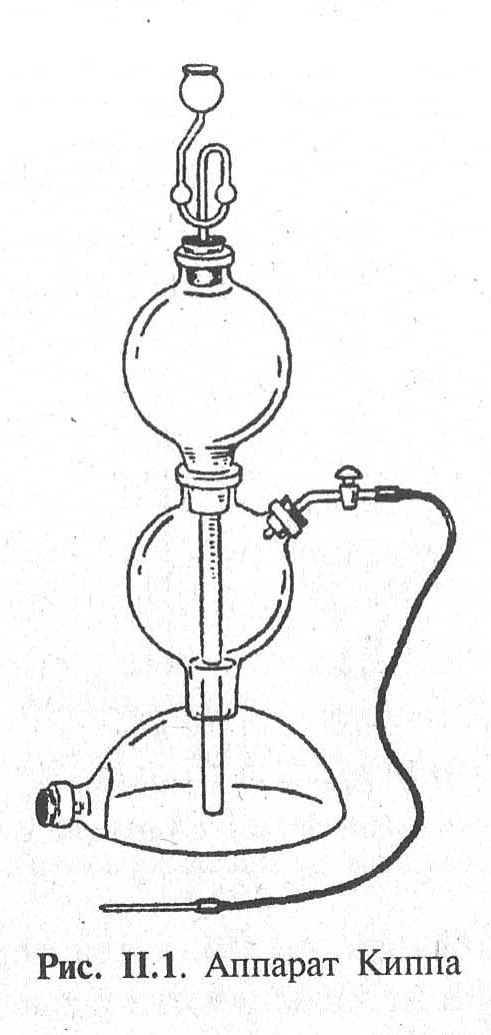 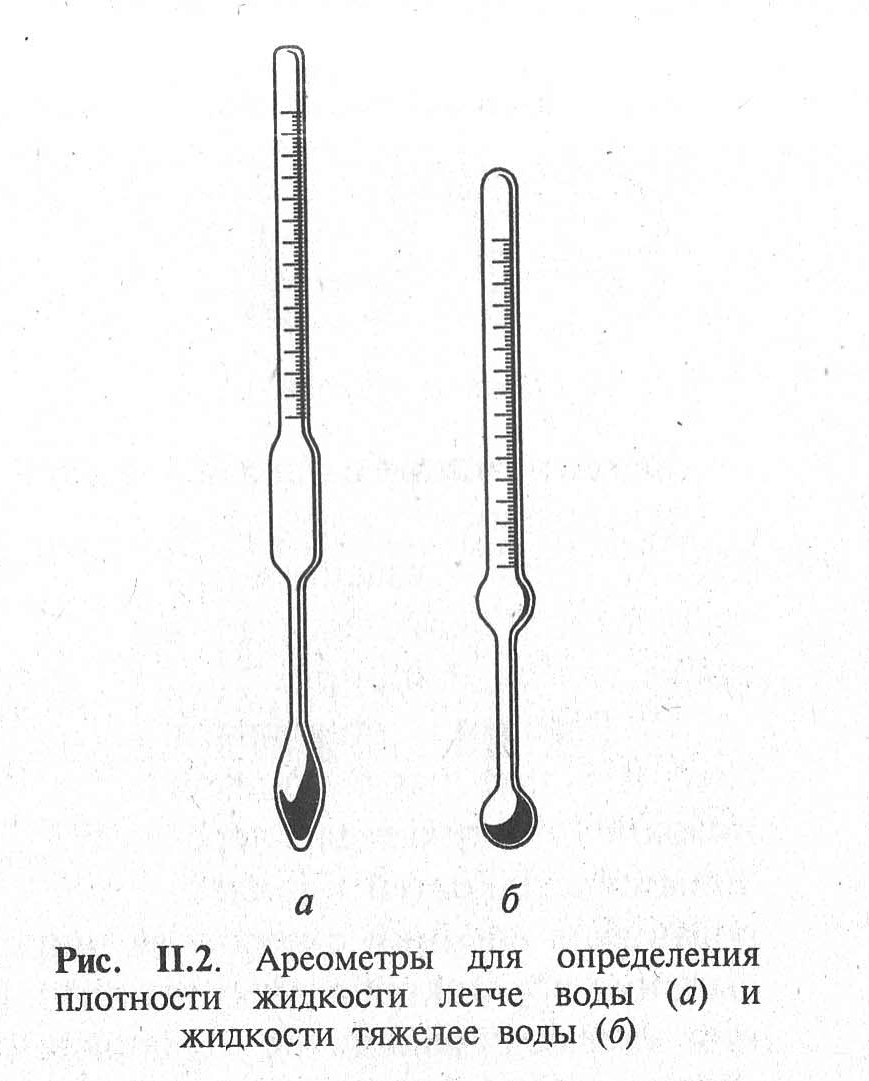 а б Рис. 4 Рис. 5 Бюретки (рис. 6) – служат для изменения объёма выливаемой жидкости. Бюретки могут быть со стеклянным краном и без крана (с зажимом или специальным шариковым запором). Наиболее часто применяются бюретки на 25 и 50 мл. Деления бюретки соответствуют мл и их десятым долям. В лабораторной практике бюретки в основном используются для титрования. Крепление бюретки для титрования изображено на рис. 6,г. 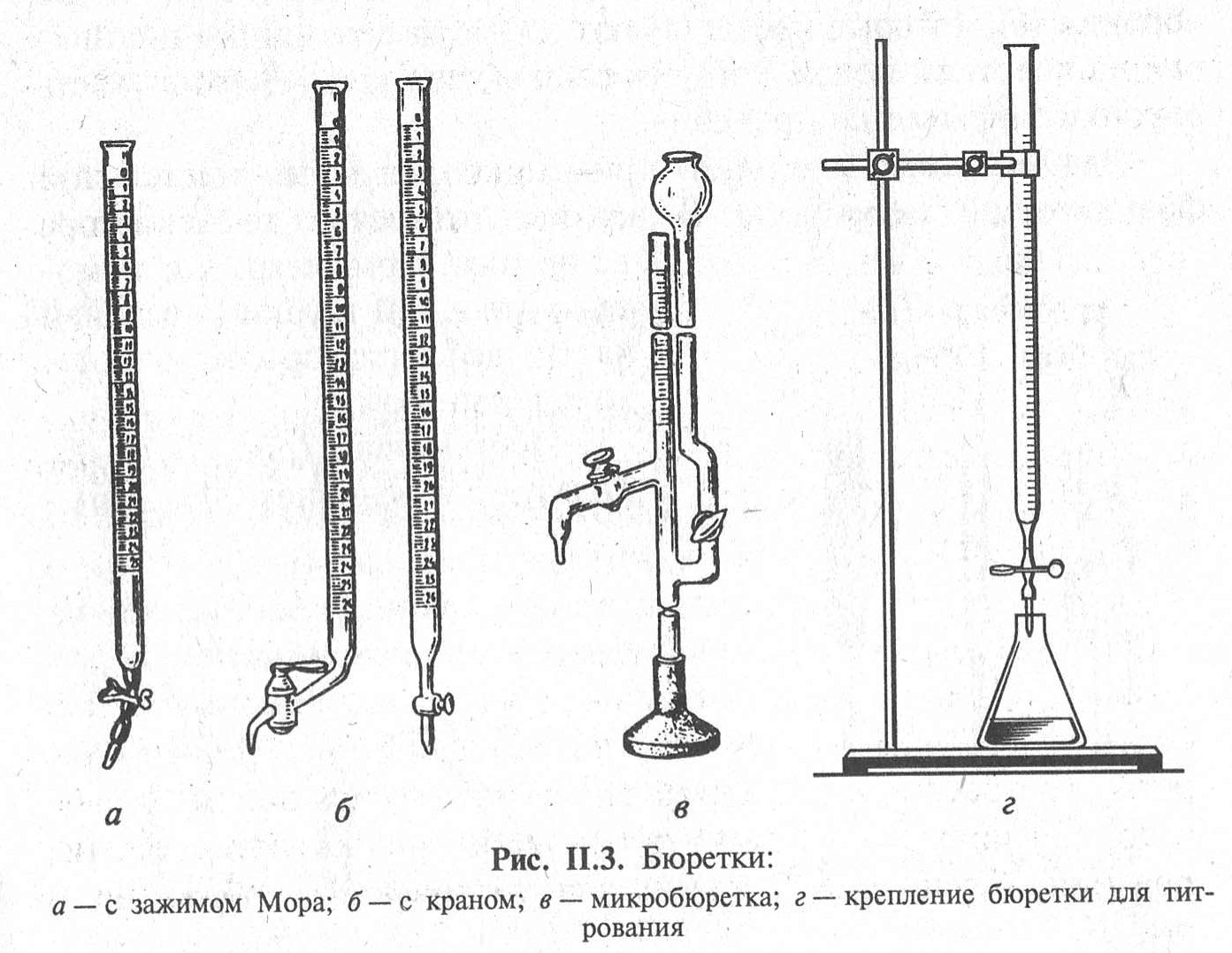 а б в г Рис. 6 а – с зажимом Мора; б – с краном; в – микробюретка; г – крепление бюретки для титрования Бюксы стеклянные (рис. 7) с притертыми крышками служат для взвешивания твердых и жидких веществ, а так же их хранения. 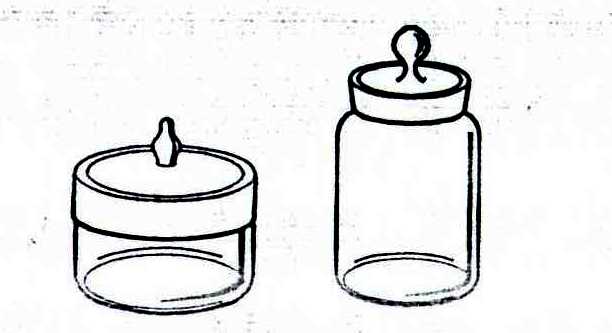 Рис.7 Бюксы стеклянные Капельницы (рис. 8) используют в основном для хранения индикаторов, а также для отмеривания жидкостей каплями. 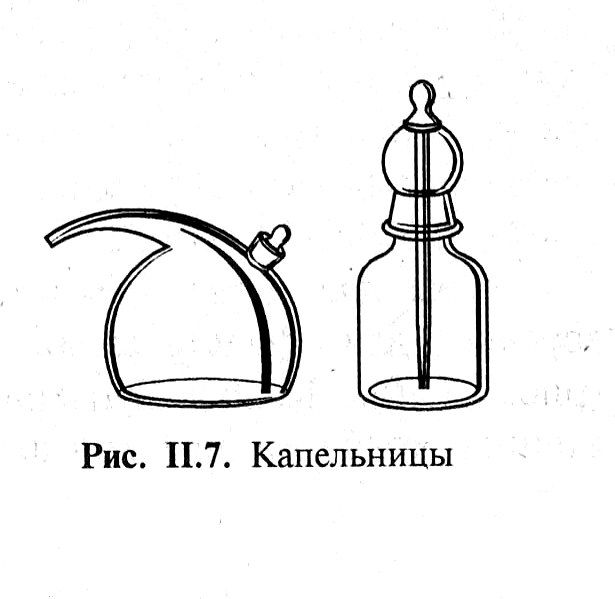 Рис. 8 Капельницы Дефлегматоры (рис. 9) применяют для более тщательной фракционной перегонки. В верхнее отверстие дефлегматора вставляют термометр, а с помощью отводной трубки (в верхней части) дефлегматор соединяют с холодильником. 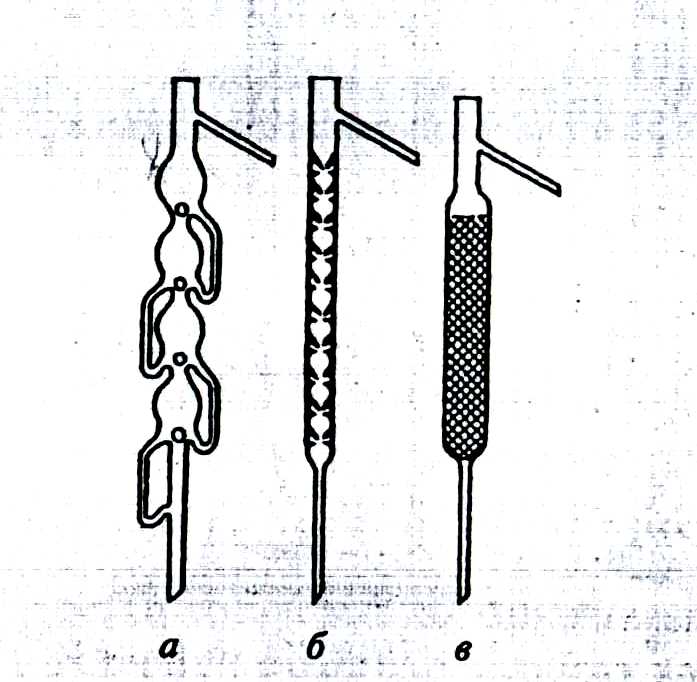 а б в Рис. 9 Дефлегматоры: а – шариковый; б – «ёлочка»; в – с пасадкой Воронки стеклянные (рис. 10) простые с длинной ножкой (а) служат для переливания жидкостей и фильтрования, а воронки с короткой ножкой (б) – для пересыпания порошкообразных веществ. При необходимости разделения несмешивающихся жидкостей используют делительные воронки (в), которые представляют собой толстостенные цилиндры, на которой ножке которых расположен кран. Верхняя часть воронки закрывается пробкой. 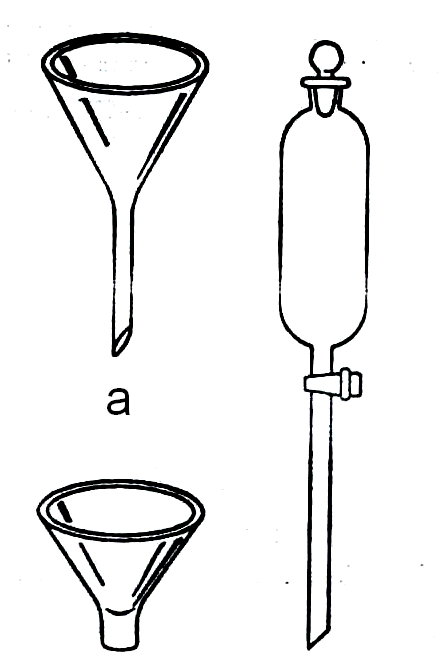 Рис. 10 Воронки стеклянные: а – с длинной ножкой; б – с короткой широкой ножкой; в – делительная воронка Колбы конические Эрленмейера (рис.11). Часто применяют при титровании. Конические колбы бывают различной вместимости. Нагревают содержимое в них только через асбестированную сетку или на бане. 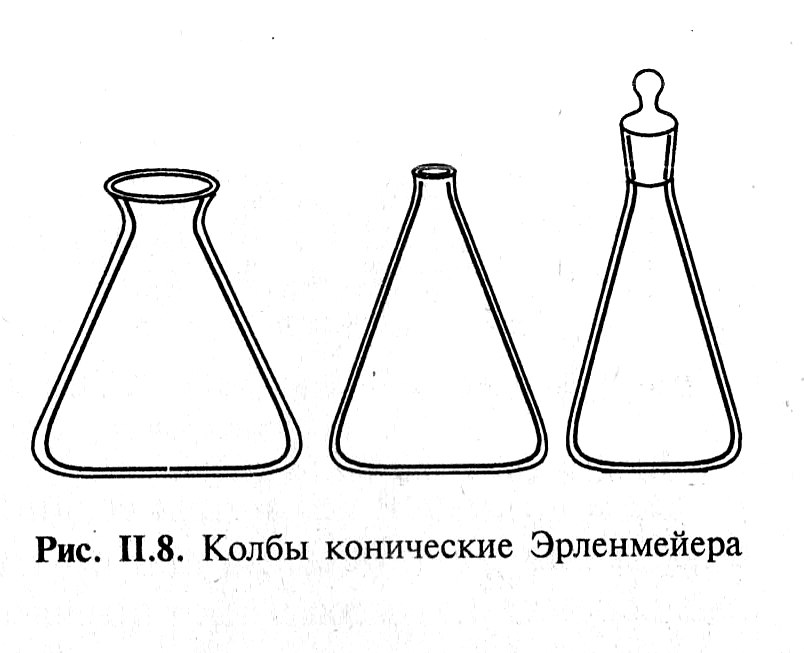 Рис.11 Колбы мерные (рис.12) используют для приготовления растворов точной концентрации. Они имеют удлиненную узкую шейку, на которой нанесена кольцевая черта, показывающая уровень наполнения. В отличие от бюреток и пипеток мерные колбы рассчитаны обычно не на выливание, а на вливание определённого объёма жидкости. Для количественного анализа наиболее часто используют мерные колбы вместимостью 50; 100; 200; 250; 500 и 1000 мл. 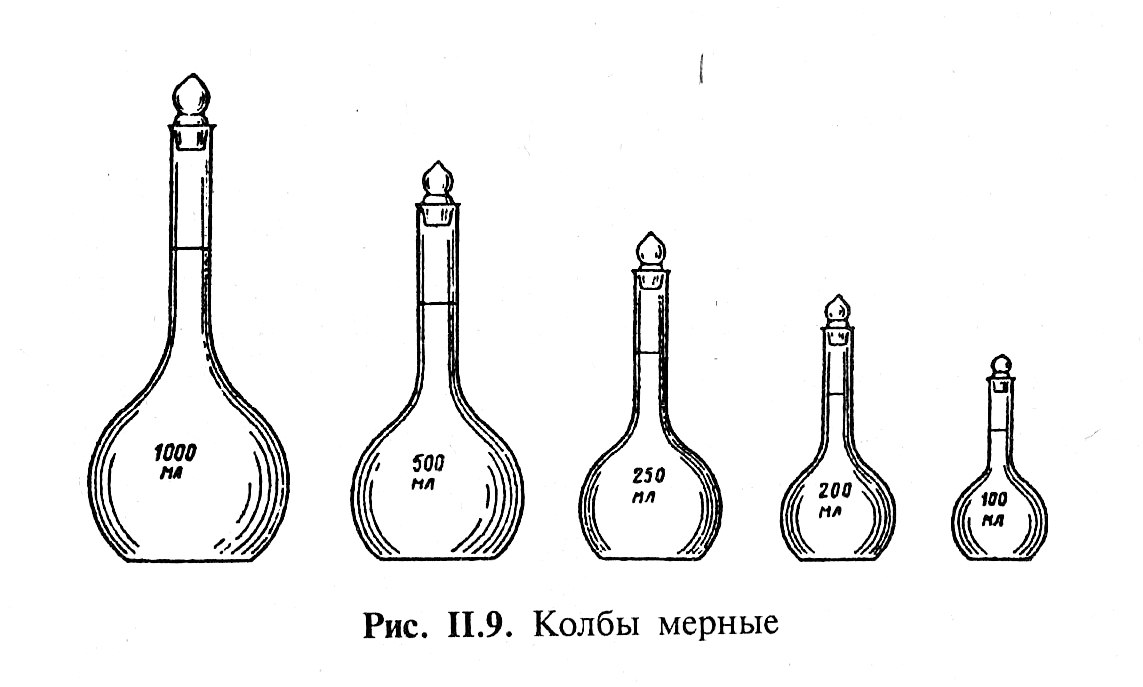 Рис. 12 Колбы для отсасывания (Бунзена) и воронки для фильтрования (Бюхнера) (рис.13). Колба Бунзена– толстостенная колба конической формы с отростком в верхней части (для соединения с вакуумным насосом), служит для фильтрования при пониженном давлении. Фарфоровые воронки Бюхнера имеют дырчатое дно, на которое укладывают влажный фильтр, закрывающий все отверстия на дне воронки. 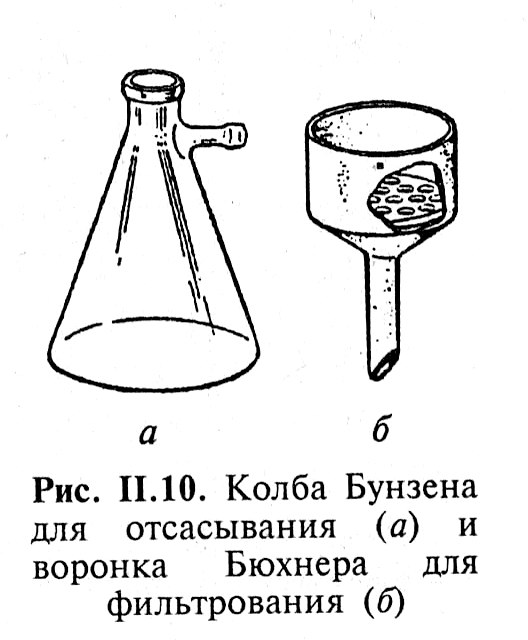 а б Рис.13 а – колбы для отсасывания (Бунзена), б – воронки для фильтрования (Бюхнера) Колбы химические (рис.14) бывают круглодонные и плоскодонные. Последние широко используются в аналитической практике. Служат для хранения жидких реактивов и растворов. Круглодонные колбы применяют для нагревания жидкостей и растворов. 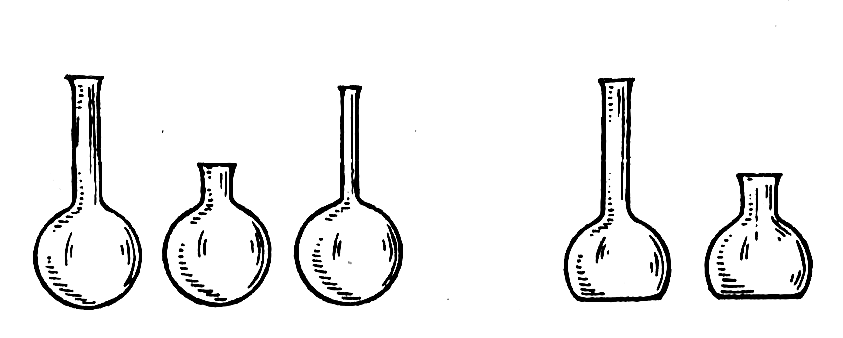 а б Рис. 14 а - круглодонные; б – плоскодонные Пробирки (рис 15). Обычно применяют стеклянные цилиндрические и конические пробирки вместимостью 2 – 5 мл. Цилиндрические пробирки используют для проведения качественных реакций, а конические – для реакций осаждения (разделения ионов и отделение раствора от осадка центрифугированием). Для хранения пробирок служат штативы. 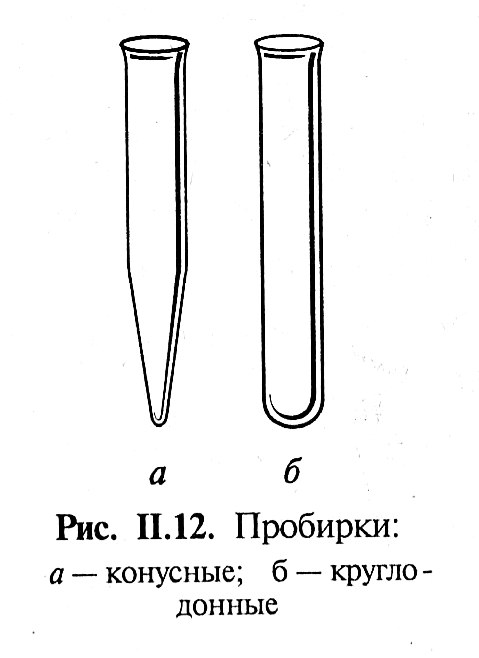 а б Рис.15 а – конусные; б - круглодонные Пипетки простые (рис.16) представляют собой стеклянные трубки диаметром 4 – 5 мм и длиной 25 – 40 мм. На один конец трубки надевают резиновый баллончик, а другой конец оттягивают до образования капилляра и слегка оплавляют его конец. Такие капиллярные пипетки применяют для отбора проб анализируемых растворов, отделение центрифугата от осадков, внесения реактивов и т.д. Для этих целей пригодны и обычные медицинские пипетки.  а б в Рис. 16 Пипетки простые а – капиллярная пипетка с резиновым баллончиком; б – положение пипетки при прибавлении реактива; в – отделение центрифугата от осадка Посуда фарфоровая (рис.17) используется для выпаривания жидкостей (стаканы, чашки) для фильтрования растворов (воронки), для измельчения образцов (ступка с пестиком), для прокаливания веществ (тигли). 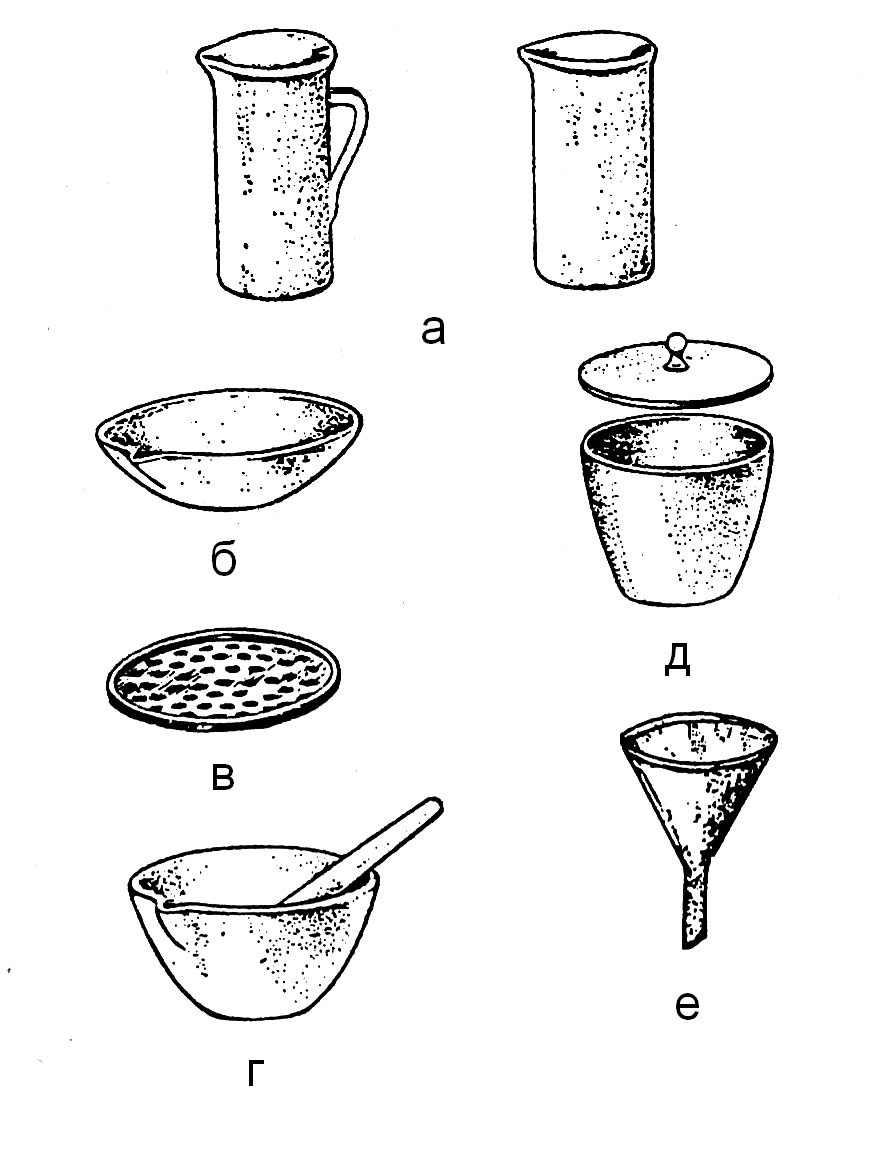 Рис. 17 Посуда фарфоровая а – стаканы; б – чашка для выпаривания жидкости; в – сетка для фильтрования; г – ступка с пестиком; д – тигель; е – воронка Пипетки мерные (градуированные пипетки и пипетки Мора) – длинные узкие трубки с расширением в середине (рис. 18). На узкой верхней части имеется специальная метка. Мерные пипетки служат для отбора, точно отмеренного объёма раствора (жидкости). Для этого оттянутый (нижний) конец пипетки глубоко погружают в жидкость и через верхний конец с помощью груши осторожно засасывают раствор. При этом нужно добиться, чтобы раствор . При этом нужно добиться, чтобы раствор заполнил пипетку выше метки приблизительно на 2 -3 мм. Затем быстро закрывают верхнее отверстие пипетки пальцем и вынимают её из жидкости. Осторожно манипулируя пальцем, выпускают лишнюю жидкость до тех пор, пока нижний край мениска не достигнет метки. Потом палец снова прижимают к отверстию. Наполненную таким образом пипетку переносят в другой сосуд, открывают верхнее отверстие и дают жидкости стечь. В лабораторной практике чаще всего используют пипетки Мора вместимостью 10; 20; 25 и 50 мл. Особая точность достигается с помощью микропипеток. 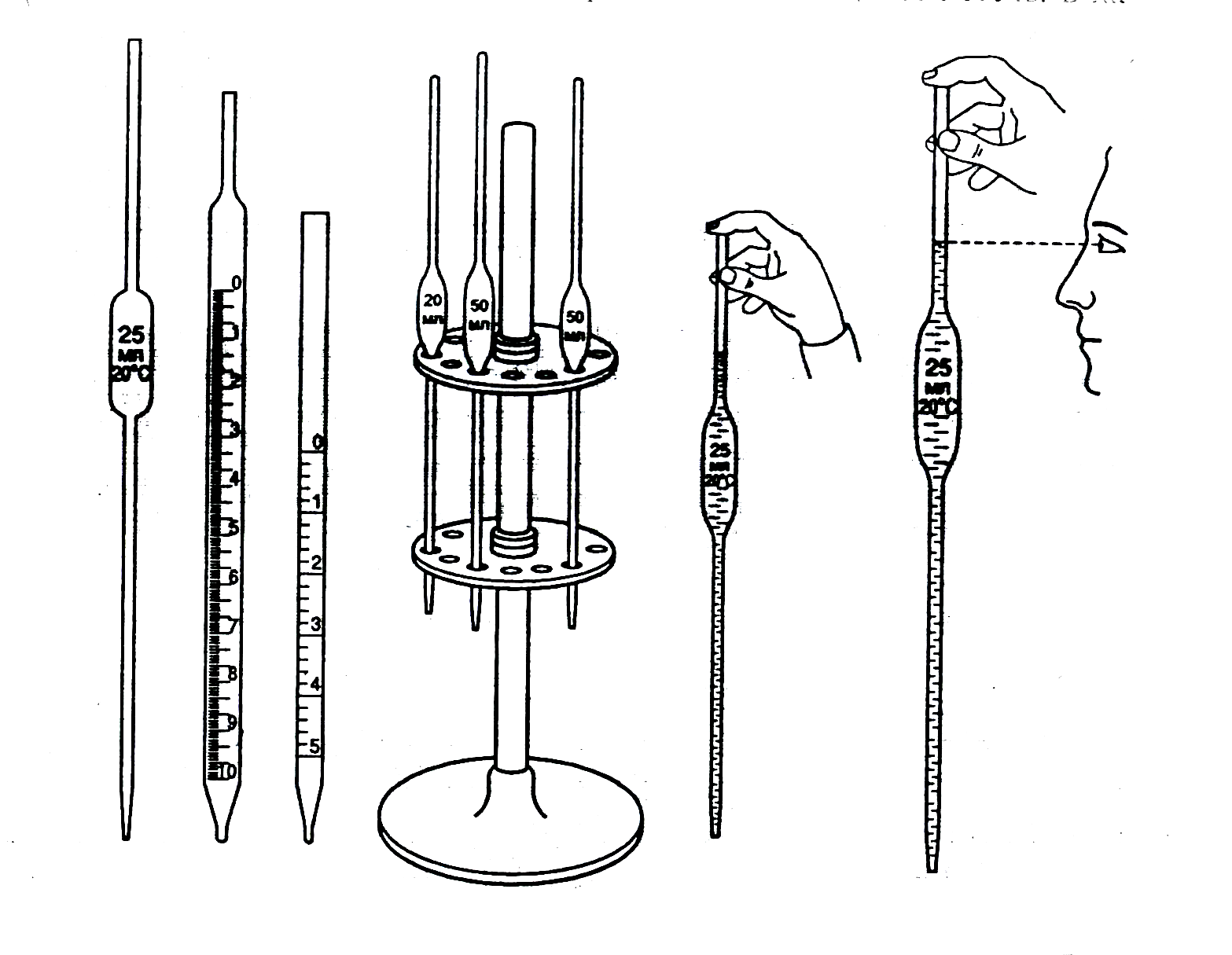 а б в г д е Рис.18 Пипетки мерные (градуированные пипетки и пипетки Мора): а – пипетка Мора; б – градуированная пипетка; в – микропипетка; г – штатив для мерных пипеток; д – заполнение пипетки Мора жидкостью; е – определение отмеренного объёма жидкости Пикнометр Оствальда (рис.19) – прибор для определения относительной плотности. Он состоит из трех частей : «носик», шарик и «хвостик» с меткой. При помощи груши, присоединенной к «хвостику»,через «носик» осторожно всасывают исследуемую жидкость (несколько выше метки). В течение 10 – 15 мин пикнометр термостатируют при 200С. Избыток жидкости убирают кусочком фильтровальной бумаги, прикасаясь к «носику» пикнометра. Пикнометр тщательно вытирают снаружи и взвешивают на аналитических весах. Ту же операцию проводят с дистиллированной водой. 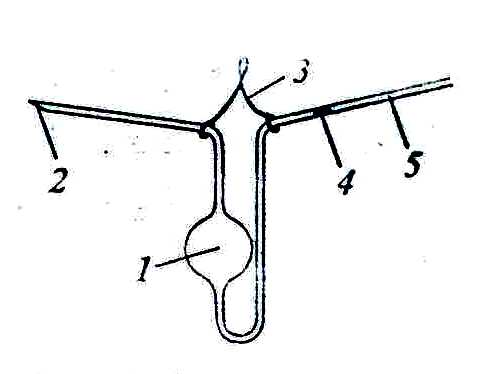 Рис. 19 Пикнометр Оствальда: 1 – шарик; 2 – «носик»; 3 проволочная петля;4 – метка; 5 – «хвостик» Промывалка (рис. 20) применяется для споласкивания лабораторной посуды дистиллированной водой, для добавления дистиллированной воды к раствору, промывания осадков и т.д.  Рис.20 Промывалка Приспособления для ускоренного микрофильтрования (рис. 21) состоит из трех частей: толстенного пробирки с отводом для создания вакуума, воронки и «гвоздика», которой опускается стержнем в воронку. На его шляпку накладывается фильтр, вырезанный в виде кружка. Диаметр фильтра немного больше шляпки «гвоздика». Перед фильтрованием кружок фильтра смачивают водой.  Рис. 21 Приспособление для ускоренного микрофильтрования: 1 – воронка; 2 – «гвоздик» с фильтром; 3 – толстостенная колба Реактивная склянка с пипеткой (рис. 22) служит ёмкостью для раствора реагентов. Обычно для этой цели используют чистые флаконы из – под пенициллина (вместимостью 10 – 15 мл), которые закрываются пробкой – пипеткой. На реактивную склянку наклеивают этикетку с названием реактива.  Рис. 22 Реактивная склянка с пипеткой Стеклянные палочки для перемешивания (рис. 23) обычная длина таких палочек 15 – 20 см, диаметр около 4 мм. На конце, которой немного оттянут, имеется небольшой шарик. Часто на конец палочки надевают кусочек резиновой трубки.  Рис. 23 Стеклянные палочки Склянки промывные (рис. 24) применяют для осушки, очистки или улавливания некоторых газов. Наиболее часто используют склянки Тищенко и Дрекселя. Заполняют их серной кислотой или концентрированным раствором щелочи.  Рис. 24 Склянки промывные: а – склянка Тищенко; б – склянка Дрекселя Стаканы химические (рис. 25) обычно изготавливаются из термостойкого стекла. Они отличаются различной вместимостью (от 50 до 1000 мл).  Рис. 25 Стаканы химические Термометры (рис. 26) без них не обходиться ни одна химическая лаборатория. Чаще всего используют ртутные термометры, представляющие собой стеклянные капилляры, имеющие на конце резервуар для ртути. Капилляр находится в центре полой стеклянной трубки и лежит на фарфоровой пластинке, на которую нанесена шкала в градусах Цельсия. Обычные химические термометры позволяют измерять температуру от -30 до 3600С. Наиболее распространены термометры со шкалой в 100, 150, 200, 250, 300 и 3600С. Для очень точных измерений температур (определения температур плавления и кипения) применяют специальные термометры («нормальные»), имеющие цену деления 0,10С. Термометры – очень хрупкие приборы, поэтому с ними нужно обращаться очень осторожно и бережно.  а б в г Рис. 26 Термометры: а – обычный ртутный; б – палочковый газонаполненный; в – технический прямой; г – технический угловой  Рис. 27 Установка для фильтрования холодных растворов через стеклянную воронку Установка для фильтрования холодных растворов через стеклянную воронку (рис. 27) на штативе крепиться стеклянная воронка, под которую ставят стакан. В воронку помещают бумажный фильтр. Холодильники (рис. 28) служат для охлаждения и конденсации паров, образующихся при кипении жидкостей. Существует несколько типов холодильников. В химической практике наиболее широко используется холодильник Либиха. Он бывает нисходящим и обратным. Нисходящий холодильник применяют в установках для простой перегонки, а так же для перегонки при уменьшенном давлении. В этом случае его крепят к установке с небольшим наклоном в сторону приёмника для перегоняемой жидкости. Если же холодильник используют как обратный, то его крепят в штативе строго вертикально. В этом положении он используется для концентрации паров долго кипящей жидкости. Охлаждённая вода подключается со стороны нижнего отвода.  а б в г д е Рис. 28 Холодильники: а – воздушный; б – Либиха; в – обратный шариковый; г – обратный с охлаждаемой спиралью (змеевиковый); д – обратный с охлаждаемой спиралью (Димрота); е – обратный с двойным охлаждением (рубашкой и охлаждающей спиралью) Цилиндры мерные (рис. 29) используют для измерения жидких реактивов, для приготовления растворов приблизительной концентрации (но не для точного измерения объёмов).  Рис. 29 Цилиндры мерные Эксикаторы (рис. 30) – ёмкости из толстостенного стекла, предназначенные для высушивания твердых веществ. Различают обычные и вакуум – эксикаторы. В последних на крышке имеется тубус, в который на резиновой пробке вставляют трубку с краном. Эту трубку через манометр и предохранительную склянку соединяют с водоструйным насосом (рис. 31) и создают в эксикаторе вакуум. Вещество, которое подвергают к сушке, на часовом стекле или чашке Петри ставят фарфоровую подставку, лежащую на выступающих бортах средней части эксикатора. В качестве осушающего агента применяют безводный хлорид кальция, сульфат магния, натронную известь, оксид фосфора (v) и др.   а б Рис. 32 Водоструйный Рис. 31 Эксикаторы вакуум-насос а – обычный; б - вакуумный Мытье химической посуды Химическая посуда должна быть совершенно чистой. От механически приставшей грязи посуду очищают при помощи специальных щёток и ершей, смоченных водой. В случае необходимости применяют мыло, 10%-ый раствор тринатрифосфата или другие моющие средства. Для мытья посуды применяют так же хромовую смесь (готовят её осторожным приливанием концентрированной серной кислоты (плотностью) к 6-10%-ому раствору бихромата калия или натрия)). При использовании хромовой смеси, её сначала подогревают, затем наливают в промываемый сосуд, предварительно сполоснутый водой. Хромовая смесь должна заполнить 1/3-1/4 объёма сосуда. Осторожно смачивают стенки сосуда и сливают хромовую смесь в тот же сосуд, где она хранилась. Промываемую посуду оставляют постоять несколько минут, затем смывают остатки хромовой смеси водопроводной водой и затем споласкивают дистиллированной водой. Хромовая смесь сильно действует на кожу и одежду и требует осторожно обращения! Признак хорошо вымытой посуды – равномерное стекание воды со стенок без заметных на глаз потёков. Взвешивание В лаборатории аналитической химии применяют различные весы. При синтетических работах (для взвешивания исходных веществ и конечных продуктов) применяются технохимические весы с точностью взвешивания до -0,01г (рис. 33). 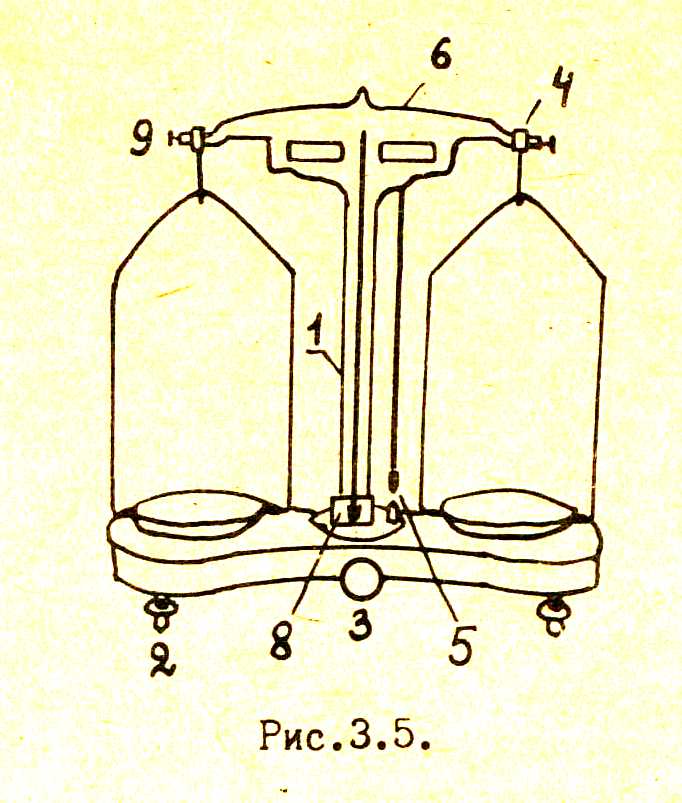 Рис. 33 Технохимические весы устанавливаются на лабораторных столах так, чтобы стойка весов (1) находилась в вертикальном положении, что определяется по отвесу(5). Это достигается регулированием установочных ножек-винтов(2). Перед взвешиванием необходимо убедиться в том, что чашки уравновешены. Для этого поворотом маховичка (3) вправо опускается специальное приспособление – арретир. Коромысло (6) при этом поднимается, и чашки повисают на стременах (4), опирающихся на призмы. Отклонение стрелки весов (7) на одинаковое число делений вправо и влево от среднего деления шкалы (8) говорит о правильной их установке. Если стрелка отклоняется в одну сторону больше, то равновесие достигается передвижением грузика (9) по винтовой нарезке. К весам придается набор гирек – разновесок, помещённый в футляр и называемый разновесом. При взвешивании необходимо соблюдать следующие правила: Взвешиваемый предмет с использованием пинцета помещать на середину левой чашки весов, а разновески – на середину правой. С начала и до конца работы пользоваться одними и теми же весами и разновесом. Класть и снимать разновески, а так же взвешиваемый предмет только при арретированных весах. Горячие, мокрые и грязные предметы не взвешивать. Жидкости взвешивать в стаканах, бюксах, тиглях и следить, чтобы они не попадали на чашку весов. После взвешивания весы арретировать, убрать разновески в свои гнёзда, убрать взвешиваемый предмет и следить за чистотой у весов. Взять у преподавателя взвешиваемый предмет, положить его на левую чашку весов, а на правую – гирю заведомо большего веса. Плавным поворотом маховичка левой рукой до конца опустить арретир и следить за чистотой у весов. Если стрелка отклоняется вправо, то вновь арретировать весы и взять следующую, большую по величине разновеску. Если стрелка отклоняется влево, то брать следующую меньшую по величине разновеску. Так продолжать до тех пор, пока не установиться равновесие, т.е. отклонение стрелки в обе стороны будет одинаковым. Приступить к подсчету веса взвешиваемого предмета. Вес записывать по пустым гнёздам футляра и проверять при укладывании разновесок, начиная с самых крупных. Вес записывается в граммах, например: 6,12 г. Более точно взвешивание (до 0,0002 г) производиться на аналитических весах (рис. 34) 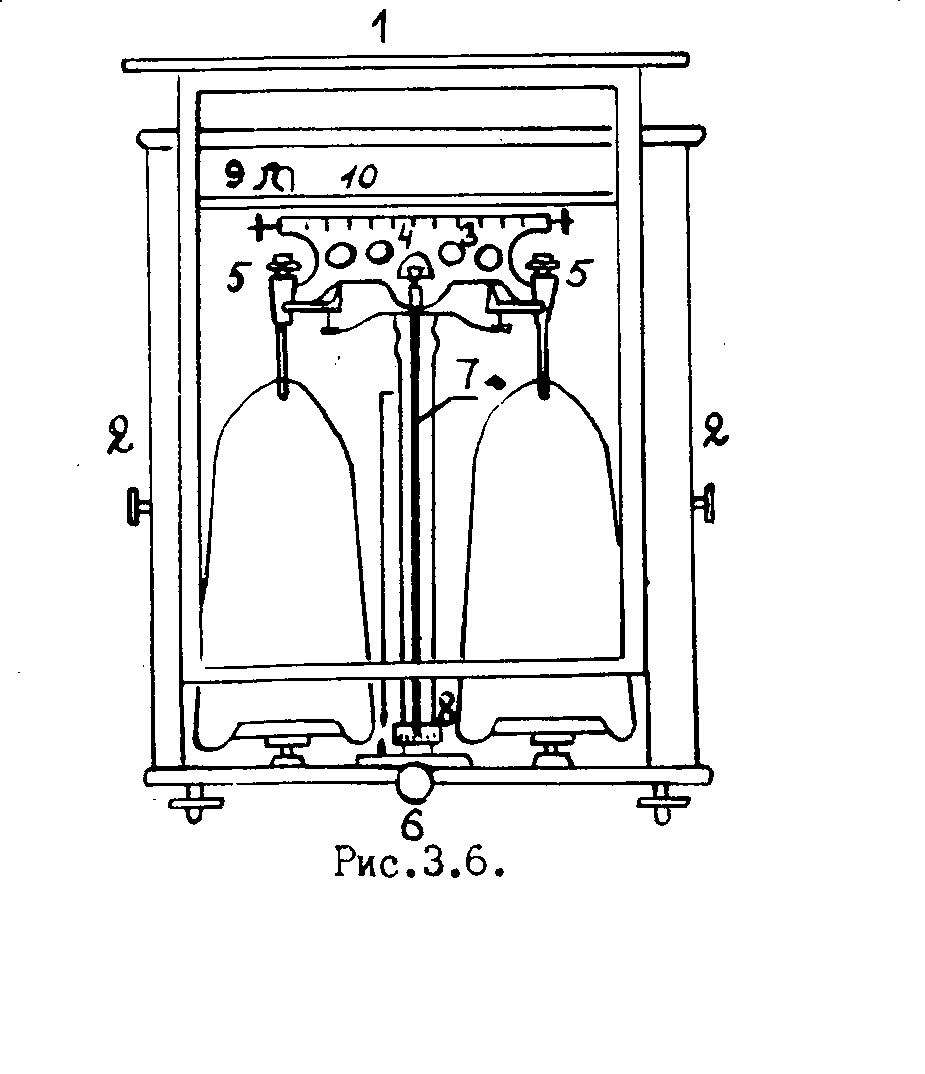 Рис. 34 Аналитические весы всегда заключены в футляр-шкафчик с застеклёнными дверцами. Передняя дверца футляра (1) поднимается вверх, две боковые дверцы(2) открываются вбок. Коромысло аналитических весов (3) опирается при взвешивании на среднюю призму (4). Имеются еще две боковые призмы (5), на которые опираются серёжки с подвешенными к ним чашками. Эти три призмы (особенно средняя) являются наиболее ответственным деталями аналитических весов. От их исправности зависит чувствительность весов. Поэтому необходимо особенно оберегать призмы. Для этого необходимо весы арретировать при помощи арретира (6) и использовать призмы только на короткое время при взвешивании. Коромысло весов имеет шкалы с делениями, к нему прикреплена стрелка (7), качающаяся вместе с коромыслом при взвешивании. Под стрелкой имеется еще одна небольшая шкала (8), разделённая на 20 отделений, среднее деление при этом принимается за «нуль». При взвешивании на аналитических весах применяют специальный аналитический разновес (набор очень точных гирек), в котором так же, как и в разновесе для технохимических весов, наименьшая разновеска весит 0,01 г. Разновески, при помощи которых можно произвести взвешивание с точностью до 0,0002 г., замены в аналитических весах так называемым рейтером (9). При помощи специального рейтерного приспособления(10) рейтер помещается на определенное деление коромысла весов. Некоторые системы аналитических весов не снабжены рейтером, его заменяет особое устройство, состоящее из ползунка со шкалой. Снаружи, справа на футляре весов помещается в этом случае ручка, при вращении которой ползунок передвигается по шкале и изменяет нагрузку на коромысле весов. Все правила взвешивания на технохимических весах, описанные ранее, необходимо соблюдать и при работе с аналитическими весами. Однако при этом необходимо соблюдать еще большую аккуратность и тщательно следить за чистотой при взвешивании. Масса взвешиваемого предмета будет равна массе разновесок только в том случае, если при взвешивании положение равновесия, определяемого также по колебаниям стрелки, будет совпадать с найденным положением «нуля». Перед взвешиванием необходимо проверить, плавно ли совершаются колебания стрелки. Помещать взвешиваемые предметы, гири, рейтер можно только при арретированных весах. Открываются лишь боковые дверки и только при арретированных весах. В настоящие время предпочитают пользоваться весами апериодического качания, имеющими приспособление для воздушного или магнитного торможения колебаний коромысла и стрелки весов. Определить положение «нуля» аналитических весов. Произвести взвешивание бюкса (или другого предмета, вещества по указанию преподавателя), соблюдая все правила взвешивания на аналитических весах. Подсчитать вес с точностью до 0,0002 г. Очистка жидкостей. Фильтрование Фильтрование применяется для освобождения жидкости от находящихся в ней твердых нерастворимых веществ. Для этого жидкость пропускают через гладкий (простой) или складчатый фильтры, сделанные из фильтровальной (не проклеенной) бумаги. Приготовление гладкого фильтра заключается в следующем. Лист фильтровальной бумаги (рис. 35), имеющий форму квадрата (а), складывается пополам (б), затем вчетверо и обрезается ножницами по дуге (в); затем один слой бумаги отделяется от остальных трех. При этом должен получиться конус (г). Фильтр вставляется в воронку так, чтобы он плотно пристал к её стенке – д. Прижимая фильтр пальцем к стенке, осторожно смачивают его небольшим количеством дистиллированной воды. Гладкий фильтр имеет недостаток – большая часть поверхности его не используется. У складчатого фильтра вся поверхность рабочая. Его изготовление состоит из следующих операций. Вначале свертывают и обрезают лист фильтровальной бумаги аналогично тому, как это делается при изготовлении гладкого фильтра (Рис. 36,а). 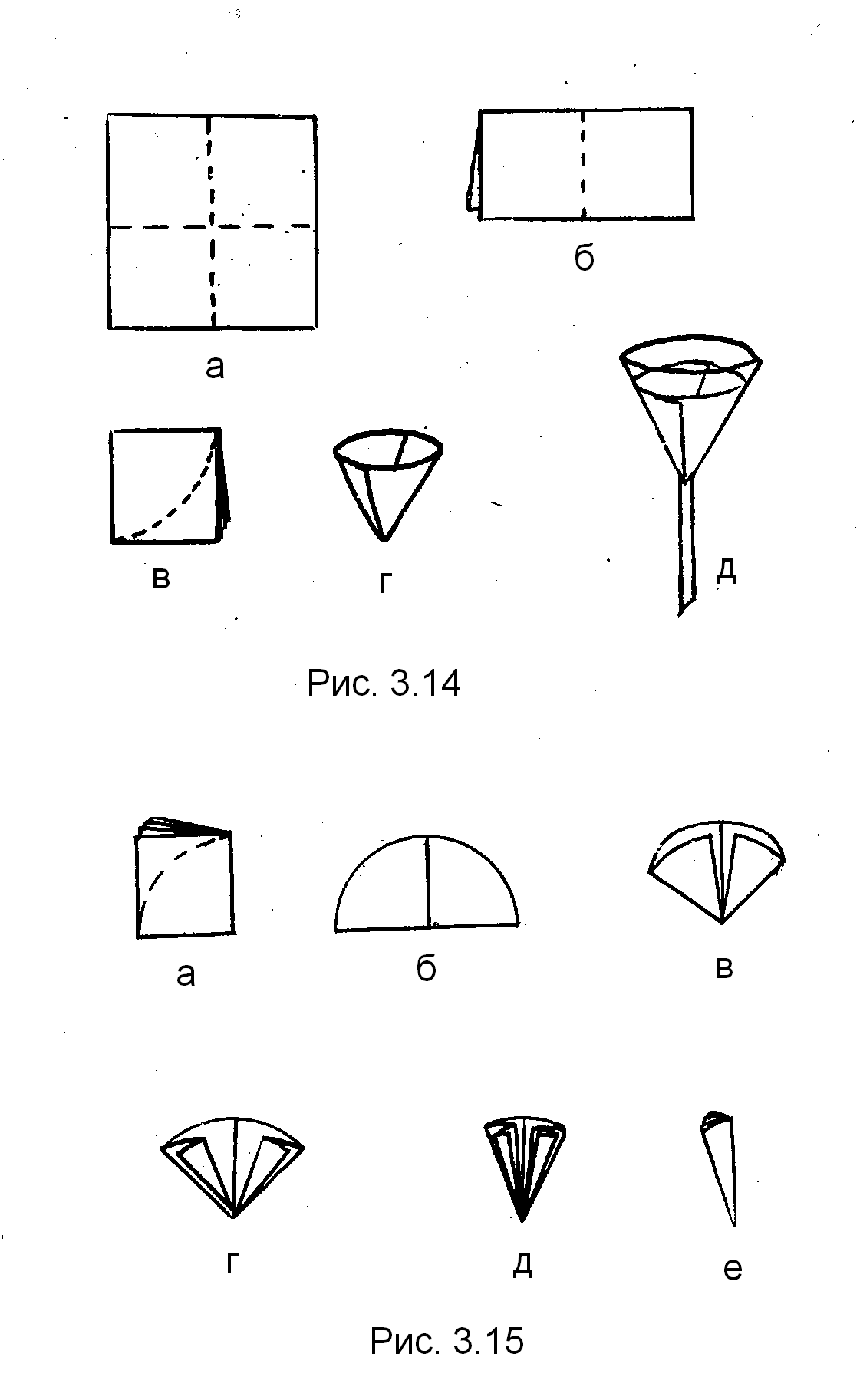 Рис. 35  Рис.36 После этого нужно расправить фильтровальный лист (рис. 36), перегнуть концы навстречу друг другу (в), отогнуть их в обратную сторону (г), перевернуть фильтр обратной стороной и перегнуть навстречу друг другу (д). Перегнуть еще раз в обратном направлении (е), расправить и вставить воронку. Край фильтра должен быть на 3-5 мм ниже края воронки. Укрепить воронку на кольце штатива так, чтобы нижний конец воронки касался стенки стакана, в который собирается фильтрат (рис. 37). Отфильтровать 20-30 см3 воды. Воду в воронку на фильтр вливать по стеклянной полочке во избежание разрыва фильтра и разбрызгивания жидкости. Фильтрование под вакуумом Для быстрого фильтрования и отделения осадка от фильтрата часто пользуются фильтрованием под вакуумом. Для этого в приёмнике фильтрата создают уменьшенное давление. Для фильтрования под вакуумом собирается установка (рис. 38), состоящая из толстостенной склянки Бунзена (1), фарфоровой воронки Бюхнера (2), предохранительной склянки Вульфа (3) и водоструйного вакуум-насоса (4). Вырезать круглый фильтр, который должен закрывать отверстия фарфоровой воронки, но в то же время свободно ложиться на дно воронки, не загибаясь у её краёв (для этого фильтр по диаметру должен быть несколько меньше внутреннего диаметра воронки). Смочить фильтрованную бумагу небольшим количеством воды и подсоединить к склянке насос на 1-2 минуты. Затем в воронку налить жидкость или раствор с фильтратом и произвести фильтрование. 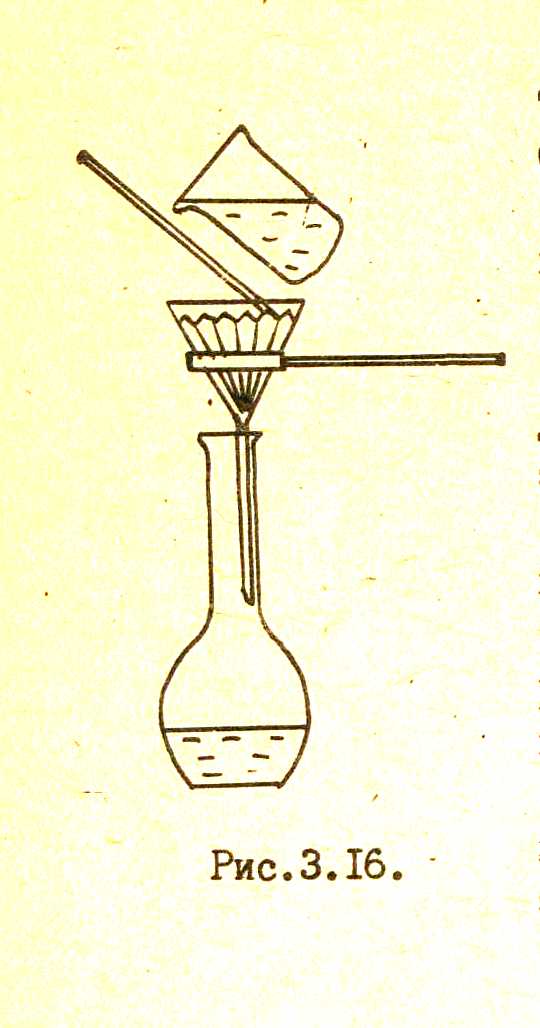 Рис. 37 Фильтрование при нагревании Растворы вязких веществ и растворы, насыщенные растворённым веществом при высокой температуре, фильтруют при нагревании. Для этой цели применяют воронки для горячего фильтрования (рис. 39) В холодную воронку для горячего фильтрования вставить стеклянную воронку с соответствующим фильтром, под неё поставить стакан – приёмник фильтрата (как показано на (рис. 39)). Затем горелкой нагреть боковой отвод водяной воронки, пока вода не нагреется до нужной температуры, или включить в сеть электрическую воронку. После того, как стеклянная воронка прогреется, на неё налить небольшое количество горячего раствора. Во время фильтрования горячий раствор подливать небольшими порциями. После окончания фильтрования убрать нагрев, воронку охладить и только после этого устройство разобрать. 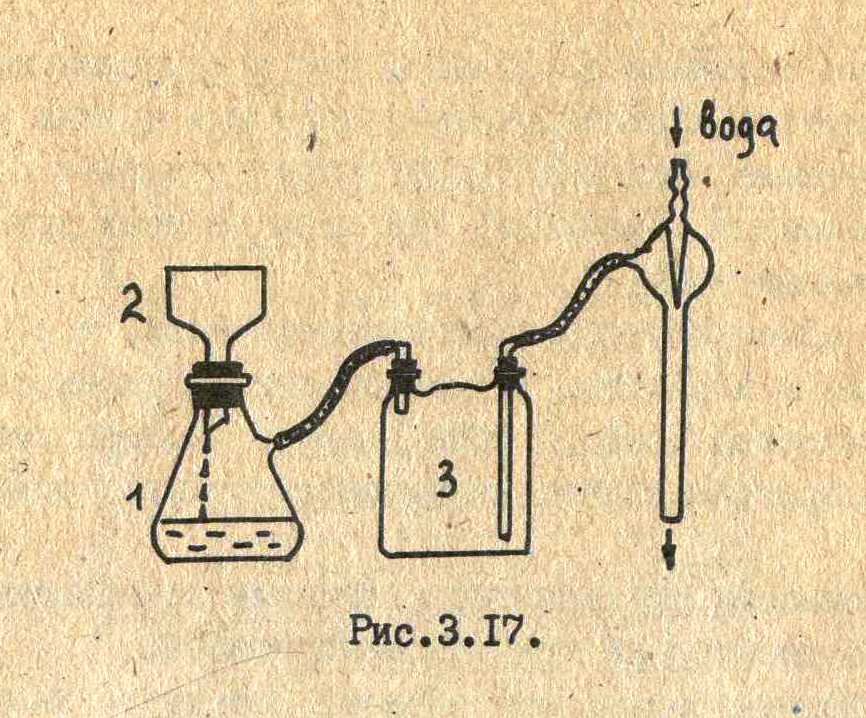 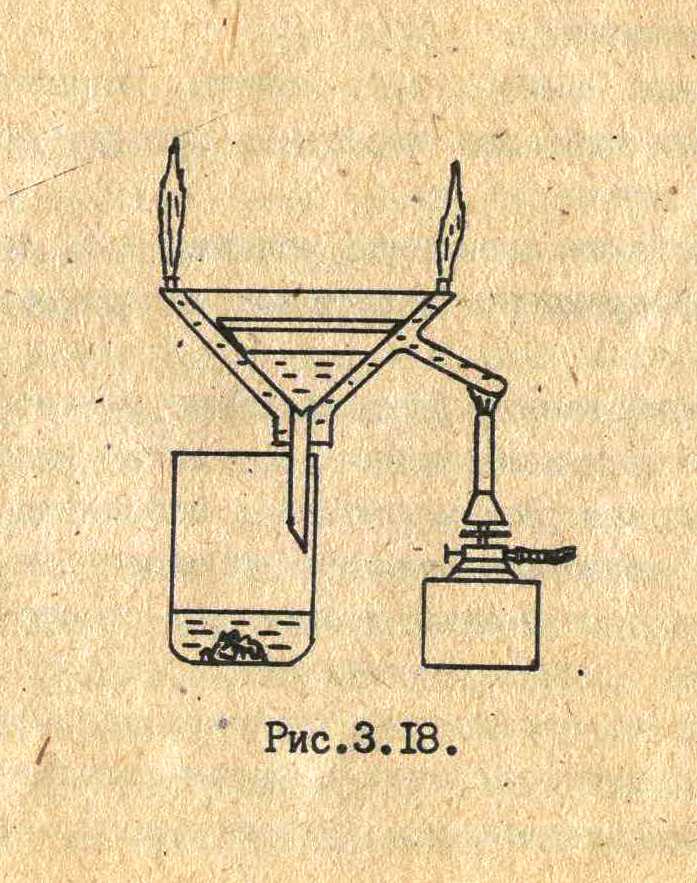 Рис. 38 Рис. 39 Перегонка воды Собрать прибор (рис. 40), состоящий из колбы Вюрца (1), холодильника (2), колбы-приёмника (3), аллонжа (4) с отростком, к которому при помощи резиновой трубки присоединена хлоркальциевая трубка (6) с натронной известью для поглощения углекислоты. В колбу Вюрца налить 1/3 объёма профильтрованной воды, добавить несколько кристаллов перманганата калия для окисления всевозможных примесей органических веществ. Туда же поместить капиллярные трубки или кусочки красного кирпича для равномерного кипения. Присоединить колбу Вюрца к холодильнику и заполнить его водой. Ток воды подавать снизу вверх по принципу противотока. Приёмник плотно закрыть пробкой, через которою проходит узкая часть аллонжа. Колбу (1) закрыть пробкой, через которую проходит термометр (5), и нагреть содержимое колбы Вюрца до кипения. Отогнать 10-20 см3 воды. Несколько капель перегнанной (дистиллированной) воды выпарить на часовом стекле и убедиться в отсутствии твердого остатка. 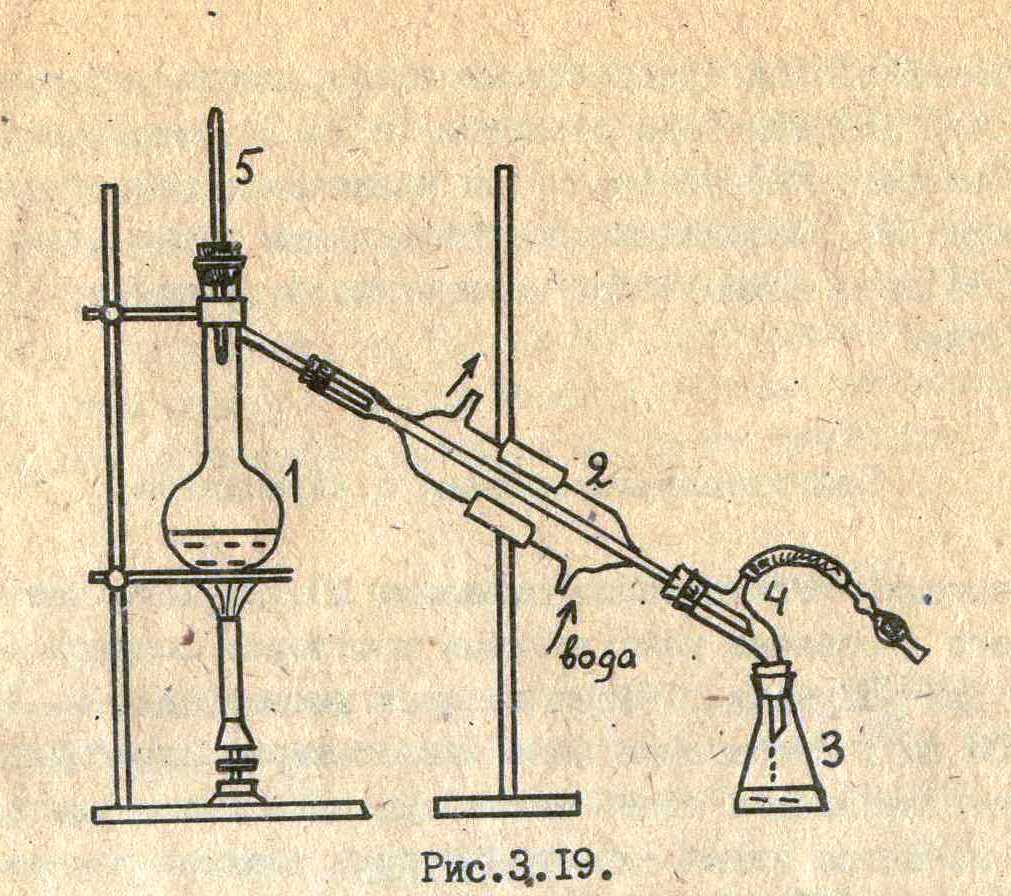 Рис. 40 Очистка воды методом ионного обмена Ионитами называются органические и неорганические вещества, практически нерастворимые вещества, практически нерастворимые в воде и в других растворителях, содержащие активные (ионогенные) группы с подвижными ионами и способные обменивать эти ионы на ионы других элементов (поглощаемые ионы). Ионный обмен протекает стехиометрически, т.е. вместо поглощенного иона в раствор из ионообменника переходит эквивалентное количество другого иона, причем процесс протекает обратимо. Температура влияет на процессы ионного обмена незначительно. В зависимости от характера введения ионообменных групп все сорбенты делятся на три основных класса: а) Сорбенты, содержащие в своей структуре кислотные группы, т.е. сорбенты, обладающие свойствами кислот и способные к обмену катионов (катиониты). б) Сорбенты, содержащие в структуре основные группы, т.е. сорбенты, обладающие свойствами оснований и способные к обмену анионов (аниониты). в) Амфотерные иониты, т.е. иониты, ионогенная группа которых может вести себя как кислотная или как основная, в зависимости от рН среды. Существуют также смешанные иониты, т.е. сорбенты, в структуры которых одновременно входят как кислотные, так и основные группы. Основные требования, предъявляемые к ионообменным смолам, следующие: высокая механическая прочность, химическая устойчивость, минимальная растворимость и небольшая набухаемость при контакте с раствором, высокая обменная способность (смола должна содержать достаточное количество пространственно доступных ионообменных групп), достаточная скорость обмена, желательная избирательность поглощения определённого типа ионов. Катионы могут содержать в своём составе различные кислотные группы: карбоксильные, сульфогруппы, фенольные, фосфатные и другие. В состав анионов в качестве функциональных групп могут входить первичные, вторичные и третичные аминогруппы, четвертичные аммониевые и пиридиновые основания. В зависимости от величины константы диссоциации катионов в Н+ - форме анионитов в ОН- - форме все смолы делятся на сильно- и слабоосновные аниониты. При выборе сорбентов в первую очередь нужно учесть, с чем удобнее работать: с катионитом или анионитом. Многие задачи могут быть успешно решены и на том, и на другом типе сорбентов. Например, для разделения ионов металлов можно с успехом применить катионы. Однако применение для этой же цели анионитов, основанное на разделении анионных комплексов этих металлов, часто бывает проще и быстрее. Необходимо учитывать также избирательность поглощения сорбентами тех или иных ионов, которая обусловлена химической природой сорбента, т.е. прочностью связей между ним и обменивающимися ионами. При этом энергия связи сорбируемого иона зависит не только от прочности его связей с любыми другими, так называемыми неактивными, структурными группами ионита. Настоящая работа предполагает использовать метод ионного обмена для очистки воды от ионов Fe3+. Для этого используются в лабораторных условиях так называемые ионообменные колонки-бюретки, заполненные подготовленным катионитом. В качестве последнего можно использовать любой катионит: КУ-1, КУ-2 и другие. Приготовление колонки с катионитом На технохимических весах отвесить 10 г. сухого катионита и залить его в стакан его в стакане с разбавленным раствором соляной кислоты (2н) для набухания. Через полчаса кислоту слить. В бюретку на 50 см3, снабжённую винтовым зажимом, поместить в нижнюю часть небольшой слой стекловаты. Для этого взять некоторое количество стекловаты пинцетом!, сделать из неё тампон (руками не касаться!), затем поместить его в бюретку и осторожно подвинуть его в нижнюю часть стеклянной палочкой. Катионит в стакане залить небольшой порцией воды, взболтать и вылить вместе с водой в бюретку. Добавить в стакан ещё воды и перенести остатки катионита. В слое катионита не должно быть воздушных пузырьков. Затем открыть зажим и слить излишнюю воду так, чтобы над катионитом остался слой воды в 1-2 см. При всех дальнейших работах с колонкой внимательно следить, чтобы над слоем катионита всё время оставался небольшой слой жидкости, так как попадания воздуха между зёрнами катионита уменьшит его рабочую поверхность, а следовательно количество поглощаемых ионов. Для переведения катионита в Н+ - форму через него медленно (со скоростью 5-10 см3 в минуту), пропускают раствор соляной кислоты (1:5). Всего достаточно пропустить 100 -150 см3 этого раствора. Некоторые сорта катионитов содержат много ионов железа. В этих случаях необходимо промывать колонку кислотой до отрицательной реакции промывных вод на железо (III) (реакция с роданид-ионом). Затем колонку промывают дистиллированной водой до нейтральной реакции промывных вод. Количество ионов, которое может быть поглощено колонкой (её общая ёмкость), зависит от количества содержащейся в ней смолы. Ёмкость ионообменной колонки выражают числом мг-эквивалентов элемента, поглощаемого единицей веса смолы. Для практических целей важнее динамическая ёмкость колонки, т.е. её ёмкость до «проскока» поглощаемого иона в фильтрат. Эта ёмкость меньше общей и зависит от формы колонки, скорости протекания раствора и других факторов. Очистка воды от ионов железа (III) Взять у лаборанта воду, содержащую ионы железа (III). Испытать её на присутствие ионов железа (III), для чего налить в пробирку около 2 см3 этой воды и добавить несколько капель насыщенного раствора роданида калия (KSCN). Темно-красная окраска образующегося роданида железа свидетельствует о наличии ионов железа (III). Оставить пробирку для сравнения. Получить у лаборанта готовую колонку с катионитом, открыв винтовой зажим, слить в стакан избыток воды, оставив над катионитом слой в несколько см. Затем с помощью зажима отрегулировать скорость вытекания воды так, чтобы она равнялась 1 капле в секунду. Следить за тем, чтобы уровень воды не опускался ниже уровня катионита. Если это произойдет, закрыть зажим и обратиться к преподавателю. Когда слой воды над катионитом будет 1-2 см, прилить в колонку очищаемую воду и дать ей вытекать с той же скоростью, собирая фильтрат в чистый стакан. После очистки всей взятой воды закрыть зажим колонки, а пропущенную через неё воду испытать на присутствие ионов железа (III). Регенерация колонки Промыть колонку раствором соляной кислоты (1:5) до отрицательной реакции промывных вод на ионы железа (III). При этом скорость пропускания раствора может быть в 2-3 раза больше, чем при очистке воды. Затем колонку промывают дистиллированной водой, полностью открыв зажим, до нейтральной реакции промывных вод по метиловому оранжевому. Регенерация остатков После проведения тех или иных опытов с химическими веществами, являющимися ядовитыми, редкими или особоценными, все растворы собираются в специальные сосуды и затем по мере накопления подвергаются регенерации. Литература Артеменко А.И., Тикунова И.В., Малеванный В.А. / Справочное руководство по химии. – М: Высшая школа,2003, - 367с. Клюквина Е.Ю., Безрядин С.Г., Учебное пособие по аналитической химии (количественный анализ). – Оренбург: изд-во ОГАУ,2002. – 200с. Основы аналитической химии. Практическое руководство / Фадеева В.И., Шеховцова Т.Н., Иванов В.М. и др. / Под. Ред. Ю.А. Золотова – М: Высшая школа, 2003. – 463с. Безрядин С.Г., Клюквина Е.Ю. Аналитическая химия. – Оренбург: изд-во ОГАУ, 2004.- 100с. Тикунова И.В., Шаповалов Н.А., Артеменко А.И. Практикум по аналитической химии и физико – химическим методам анализа. - М: Высшая школа, 2006. – 207с. Техника лабораторных работМетодические указания по химии для студентов дневной и заочной форм обучения Составитель: Комлева Наталья Николаевна Редактор: Редакционно-издательский отдел Казанской государственной архитектурно-строительный университет Подписано в печать Заказ Тираж экз. Формат 60х84/16 Печать офсетная Бумага тип № Усл. печ. л. 2.0 Уч.-изд. Л. 2.0 Печатно-множительный отдел КГАСУ |
