химия. Название ацетоуксусной кислоты по номенклатуре iupac 3оксобутановая кислота
 Скачать 36.67 Kb. Скачать 36.67 Kb.
|
|
ЮЛЯ Доброкачественность ацетилсалициловой кислоты определяется отсутствием – салициловой кислоты Название ацетоуксусной кислоты по номенклатуре IUPAC- 3-оксобутановая кислота Пировиноградная кислота реагирует с этанолом за счет- карбоксильной группы Пятичленные гетероциклы с одним и двумя гетероатомами относятся к п-избыточным потому что- число электронов, образующих ароматическую систему, превышает общее число атомов в цикле В реакции восстановления пировиноградной кислоты образуется- молочная кислота При нагревании y-оксикислоты образуется-лактон Никотинамид-это витаминное и противопеллагрическое средство При нагревании a-аминокислоты в присутствии гидроксида бария образуется-амин Соли лимонной кислоты называются- цитраты Качественной на салициловую кислоту является реакция ч – FeCl3 При нагревании a-оксикислоты образуется –лактид Реакция сульфирования тиофена, пиррола,фурана протекает по механизму-электрофильного замещения Пировиноградная кислота вступает в реакции за счет-кето-группы Примесь салициловой кислоты в ацетилсалициловой кислоте появляется в результате реакции-гидролиза Название пировиноградной кислоты по номенклатуре IUPAC-2-оксопропановая кислота При окислении молочной кислоты образуется-пировиноградная кислота Парацетамол является производным- п-аминофенола Для получения новокаина из этилового эфира п-аминобензойной кислоты необходимо- HOCH2-CH2N(C2H5)2,H В медицине производные 5-нитрофурана применяют как- противомикробные КАТЯ 1. Обнаружить примесь салициловой кислоты в ацетилсалициловой кислоте можно по реакции с ХЛОРИДОМ ЖЕЛЕЗА 3 2. Качественной на салициловую кислоту является реакция с ХЛОРИДОМ ЖЕЛЕЗА 3 3. Лекарственное средство, в основе которого лежит структура пиразолона-3(5) АНАЛЬГИН 4. Препарат 5-нок является производным ХИНОЛИНА 5. Пировиноградная кислота реагирует с гидроксидом натрия за счет КАРБОКСИЛЬНОЙ ГРУППЫ 6. Доброкачественность ацетилсалициловой кислоты определяется отсутствием примеси САЛИЦИЛОВОЙ КИСЛОТЫ 7. Аминокислота триптофан является производным гетероцикла ИНДОЛА 8. n-аминофенол вступает в реакции ацилирования за счет АМИНОГРУППЫ 9. Гидразид изоникотиновой кислоты ( изониазид ) это- ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО 10. В медицине производные 5-нитрофурана применяют как ПРОТИВОМИКРОБНЫЕ СРЕДСТВА 11. Пировиноградная кислота реагирует с этанолом за счет КАРБОКСИЛЬНОЙ ГРУППЫ 12. Барбитуровая кислота проявляет сильные кислотные свойства за счет ЛАКТИМНОЙ ТАУТОМЕРНОЙ ФОРМЫ 13. Соли винной кислоты ТАРТРАТЫ 14. Пиррол содержит в цикле атом АЗОТА АНЯ 1. качественным признаком реакции салициловой кислоты с хлоридом железа 3 является—появление фиолетового окрашивания 2. количество электронов делокализованных в сопряженной системе пурина—8 3. новокаин является производным—п-аминобензойной кислоты 4. при нагревании альфа амино кислоты в присутствии гидроксида бария образуется—амин 5.антибактериальное действие оксина связывают с его—способностью образовывать хелатные комплексы Аминокислота гистидин является производным гидроцикла—имидазола 6. в медицине производные 5 нитрофурана применяют как—противомикробные средства 7. стрептоцид является производным –сульфаниловой кислоты 8. парацетомол является производным –п-аминофенола 9. азотсодержащий пятичленный гетероцикл с одним гетероатомом—пиррол 10. пировиноградная кислота реагирует с гидроксидом натрия за счет—гидроксильной группы 11. При нагревании бета - аминокислоты образуется—а,b-непридельная кислота 12. реакция S1 протекает в молекуле хинолина по положению—5 и 8 бензольного кольца 13. Соли яблочной кислоты называются—малаты 14. При нагревании альфа - оксикислоты образуется--лактид К альдопентозам относится Д-РИБОЗА Макроэргические связи в структуре днк являются АНГИДРИДНЫМИ Нуклеотид днк: ТИМИДИН-5-ФОСФАТ ДЕЗОКСИАДЕНОЗИН-5-ФОСФАТ АДЕНОЗИН-3-ФОСФАТ Растительные масла могут быть переведены в твердые жиры путем ГИДРОГЕНИЗАЦИИ Изоэлектрическая точка асп-тир-вал лежит в НЕЙТРАЛЬНОЙ области Нуклеотид рнк: АДЕНОЗИН-5-ФОСФАТ УРИДИЛОВАЯ КИСЛОТА ГУАНИЛОВАЯ КИСЛОТА Кислотные свойства альфа-аминокислот проявляются за счет КАРБОКСИЛЬНОЙ ГРУППЫ L-глюкоза является АЛЬДОГЕКСОЗОЙ Восстанавливающие свойства дисахаридов проявляются за счет ПОЛУАЦЕТАЛЬНОГО ГИДРОКСИЛА Моносахаридные звенья сахарозы: ГЛЮКОПИРАНОЗА ФРУКТОФУРАНОЗА Для получения глюконовой кислоты из глюкозы в качестве окислителя используют БРОМНУЮ ВОДУ Ненасыщенные жирные кислоты: ОЛЕИНОВАЯ ЛИНОЛЕВАЯ ЛИНОЛЕНОВАЯ Для проведения реакции Селиванова используют РЕЗОРЦИН И КОНЦ СОЛЯНУЮ КИСЛОТУ При нагревании фенилаланина с конц азотной кислотой появляется ЖЕЛТОЕ окрашивание, в щелочной среде ОРАНЖЕВОЕ Для доказательства непредельности жира используют реакции с ПЕРМАНГАНАТОМ КАЛИЯ И БРОМНОЙ ВОДОЙ Для алкилирования маннозы можно использовать ХЛОРЭТАН При дезаминировании валина ин витро образуется АЗОТ D-манноза является АЛЬДОГЕКСОЗОЙ О-этил-В-Д-галактопираноза ГИДРОЛИЗ В КИСЛОЙ СРЕДЕ Энантиомеры: Д и Л-галактоза Основные свойства альфа-аминокислот проявляются за счет АМИНОГРУППЫ Гликоген гидролизуется В КИСЛОЙ СРЕДЕ И В ПРИСУТСТВИИ ФЕРМЕНТОВ Линейная последовательность аминокислотных остатков в полипептидной цепи называется ПЕРВИЧНОЙ структурой белка Дисахарид, построенный из двух остатков глюкопиранозы, связанный b- 1, 4 –гликозидной связью- целлобиоза Аминоациладенилатный комплекс является- смешанным ангидридом альфа аминокислоты и АМФ Пептидная связь представляет собой p- п – сопряженную систему, в которой делокализовано 2 электрона Биологически важные жирные кислоты- это, как правило, монокарбоновые кислоты с неразветвленной углеродной цепью и четным числом атомов углерода Как спирт фруктоза может вступать в реакцию- образования N – гликозидов 1. Фенилаланин реагирует со щелочью за счет- карбоксильная группа 2. В результате частичного окисления жира его йодное число- уменьшается 3. При взаимодействии фруктозы с Cu(oh)2 при комнатной температуре наблюдается-образование ярко –синего раствора 4. В молекулах кефалинов фосфатидовые кислоты этерифицированы по фосфатному гидроксилу-коламин и серин 5. колба с гавном-остатков серосодержащих аминокислот 6. л глюкоза является-альдогексозой 7. фруктозу можно отличить от глюкозы использую реакцию- Селиванов 8. качественным признаком реакции на серосодержащие кислоты белков с ацетатом свинца является появление- черного осадка 9. при образовании молекулы невосстанавливающего дисахарида- взаимодействуют полуацетальные гидроксилы двух моносахаридов 10. пуриновые основания- аденин гуанин 11. пиримидиновы основания- урацил цитозин тимин 12. изоэлектрическая точка изолейцина находится в – нейтральной области 13. принимают участие ЦИС изомеры ненасыщенных карбоновых кислот 14. катализатором в реакции получения че то там этил D-маннопиранозида является-газообразный хлороводород 15. нуклеотид РНК- аденозин 5 фосфат, уридиловая кислота, гуаниловая кислота 16. для получения галактаровой кислоты из галактозы в качестве окислителя используют-разбавленную азотную кислоту 17. Такой эффект реакции белка с концентрированной азотной кислотой при нагревании свидетельствует о присутствии в его молекуле- остатков ароматических аминокислот 1) Эпимерами являются—D-манноза и D-глюкоза 2) Фенилаланин реагирует со щёлочью за счёт—карбоксильной группы 3) При нагревании фенилаланина с концентрированной азотной кислотой появляется ЖЕЛТОЕ окрашивание .которое в щелочной среде изменится на ОРАНЖЕВОЕ 4) Моносахаридные звенья сахарозы—фруктопираноза,глюкопираноза 5) Изоэлектрическая точка лизина находится в—нейтральной области Ph 6) Диастереомерами являются—D-галактоза и D-глюкоза 1) В сильнощелочной среде аланин существует в виде-- биполярного иона 2) Качественные реакции на ароматические аминокислоты белков является реакция—HNO3 3)Гликоген гидролизуется—в присутствии ферментов ,в кислой среде 4) При взаимодействии глюкозы с гидроксидом меди 2 при нагревании наблюдается—образование ярко-синего раствора 5)L-фруктоза является—кетогексозой 6) Для ацилирования глюкозы можно использовать—уксусный ангидрид 7) Катализатором в реакции получения о-этил-а-d-маннопиранозида является—газообразный хлороводород 8) Качественным признаком ксантопротеиновой реакции на белок является—появление желтого окрашивания ,переходящего в оранжевое в щелочной среде 9) качественным признаком биуретовой реакции служит появление—синего окрашивания раствора 10) для получения глюконовой кислоты из глюкозы в качестве окислителя используют—Ag(NH3)2OH 11) Как спирт фруктоза может вступать в реакцию—серебряного зеркала 12) Глюкоза проявляет свойства многоатомных спиртов в реакции с—гидроксидом меди(2)при комнатной температуре 13) Реагентом для биуретовой реакции является—гидроксид меди 2 14) В реакции аминокислоты с нитритом натрия в кислой среде образуется—непредельная кислота 15)Установите соответствие дисахарид-тип гликозидной связи— Мальтоза-а-1,4 Сахароза-1.2 Целлобиоза-b-1,4 16) Восстанавливающие свойства глюкозы проявляются в реакции с—водородом на никелевом катализаторе 17) Как спирт рибоза может вступать в реакцию—СЕРЕБРЯНОГО ЗЕРКАЛА 18)классификация а-аминокислот по числу амино-и карбоксильных групп— Лизин-основная Цистеин –кислая 19) Качественными признаками реакции а-аминокислот с солями меди 2 является образование продукта—синего цвета 1.Эритроциты находятся в растворе хлорида натрия с массовой долей 0,9 % какой процесс при этом наблюдается ОСМОТИЧЕСКОЕ РАВНОВЕСИЕ 2.Химическое равновесие- это состояние системы, при котором СКОРОСТИ ПРЯМОЙ И ОБРАТНОЙ РЕАКЦИИ РАВНЫ 3.Выберите пример физической адсорбации из списка АДСОРБАЦИЯ ИНЕРТНЫХ ГАЗОВ АКТИВИРОВАННЫМ УГЛЁМ 4.Метод разделения и определения смеси веществ с использованием сорбентов называется ХРОМАТОГРАФИЯ 5.Проникновение молекул растворителя из раствора с большей концентрацией в раствор с меньшей концентрацией называется ОСМОТИЧЕСКИЙ ТОК 6.Укажите агрегатное состояние компонентов в дисперсной системе костная ткань ТВЁРДОЕ ВЕЩ-ВО-ДИСПЕРСНАЯ ФАЗА, ТВЁРДОЕ ВЕЩ-ВО-ДИСПЕРСИОННАЯ СРЕДА 7.Вещества,уменьшающие поверхностное натяжение растворителя называются ПОВЕРХНОСТНО-АКТИВНЫЕ 8.Свойства ферментов ДЕЙСТВУЮТ ПРИ ЗНАЧЕНИИ Ph 7,35-7,45 9.Температура, при которой давление насыщенного водяного пара над жидкостью равно внешнему давлению называется ТЕМПЕРАТУРА КИПЕНИЯ 10.Преимущественно одностороннее проникновение молекул растворителя......ОСМОС 11.Вещества, не изменяющие поверхностное натяжение растворителя называются ПОВЕРХНОСТНО-НЕАКТИВНЫЕ 12.Поглощение вещества всем объемом сорбента называется АБСОРБАЦИЯ 13.Дисперсной системой называется ГЕТЕРОГЕННАЯ СИСТЕМА, В КОТОРОЙ ОДНА ИЗ ФАЗ.... 14.Самопроизвольный процесс может быть если изменение энергии гиббса ОТРИЦАТЕЛЬНОЕ 15.Эритроциты находятся в растворе хлорида натрия с массовой долей 0,09%. Какой процесс при этом наблюдается ЭНДООСМОС 16.Укажите агрегатное состояние компонентов в дисперсной системе слюна ЖИДКОСТЬ-ДИСПЕРСНАЯ ФАЗА,ТВЁРДОЕ ВЕЩЕСТВО-ДИСПЕРСИОННАЯ СРЕДА 17.Дано уравнение реакции (N2+3H2=2NH3)Как изменится скорость прямой реакции,если объём в системе увеличить в 2 раза УМЕНЬШИТСЯ В 16 РАЗ 18.Дано уравнение 4HCl+O2=2CL2+2H2O Как изменится скорость прямой реакции, если концентрацию HCL в системе уменьшить в 2 раза УМЕНЬШИТСЯ В 16 РАЗ 19.Укажите агрегат в структуре мицеллы, образованной при взаимодействии нитрата серебра с избытком йодида калия ОТВЕТ M[Agl]nl- 20.Укажите гранулу в структуре мицеллы, образованной при взаимодействии нитрата серебра с избытком йодида калия ОТВЕТ {m[Agl]nl-(n-x)K+} 21. Свойства растворов,которые не зависят от природы растворенного вещества,а только от его концентрации, называются КОЛЛИГАТИВНЫЕ 22.Раствор с массовой долей хлорида натрия 9% по отношению к плазме крови является ГИПЕРТОНИЧЕСКИМ 23.Если 20 г вещества растворить в 80 граммах воды, то массовая доля компонента будет ОТВЕТ 20 % 24.Найдите реакцию, в которой изменение энергии энтропии будет положительным 2С2H2+502=4CO2+2H2O 25.Дано уравнение реакции N2+O2(стрелочки в обе стороны)2NO H=180,8 КДЖ Как изменится химическое равновесие при повышенном давлении в системе НИ В КАКУЮ СТОРОНУ НЕ СМЕСТИТСЯ 26.Какой объём занимает 10 моль кислорода 6,02*10(в 25 СТЕПЕНИ) 27.Какое количество молей содержится в 200 миллимоль N2 ОТВЕТ 0,2 28.Эритроциты находятся в растворе хлорида натрия с массовой долей 0,9%.Какой процесс при этом наблюдается Эритроциты не изменяются. 29.Укажите вещество с наибольшей поверхностной активностью в гомологическом ряду БУТАНОЛ 30.Если 98 грамм серной кислоты находится в 1 л раствора, то молярная концентрация раствора будет равна 1 МОЛЬ/Л 31.При каком варианте набухания достигается предельное значение массы или объёма полимера , после чего процесс не зависит от времени ОГРАНИЧЕННОЕ 32.Степень набухания в изоэлектрической точке белка МИНИМАЛЬНАЯ 11 11 33.Если полимеры состоят из разных атомов в цепи, то они называются ГЕТЕРОЦЕПНЫЕ 34.Раствор с массовой долей глюкозы 0,5% по отношению к плазме крови является ГИПОТОНИЧЕСКИМ 35.Если реакция проходит с уменьшением энтальпии, то эта реакция ЭКЗОТЕРМИЧЕСКАЯ 36.Размерность молярной концентрации МОЛЬ/КГ // МОЛЬ/Л 37.Процесс, проходящий при постоянном объёме, называется ИЗОХОРНЫЙ 38.Процесс проникновения растворителя в полимерное вещество , сопровождаемый увеличением объёма и массы называется НАБУХАНИЕ 39.Функция состояния системы, которая является мерой неупорядочености системы называется ЭНТРОПИЯ 40.Какое количество миллимолей содержится в 0,5 моль NO2 ОТВЕТ 500 41.Метод удаление из крови различных токсических вещество......называется ГЕМОСОРБЦИЯ 42.Принцип метода очистки коллоидных систем - электродиализ УДАЛЕНИЕ НИЗКОМОЛЕКУЛЯРНЫХ ЧАСТИЦ С ПОМОЩЬЮ МЕМБРАНЫ.... 43.Принцип метода очистки коллоидных систем- фильтрация ПРОДАВЛИВАНИЕ РАЗДЕЛЯЕМОЙ СМЕСИ.... 44.Объёмная доля компонента рассчитывается как ОТНОШЕНИЕ ОБЪЕМА РАСТВОРЕННОГО ВЕЩЕСТВА К ОБЪЁМУ РАСТВОРА 45.Выберите поверхностно-неактивное вещество из списка САХАРОЗА 46.При каком варианте набухания достигается предельное значение массы или объема полимера, после чего процесс не зависит от времени ОГРАНИЧЕННОЕ 47.Найдите реакцию, в которой энтропия НЕ ИЗМЕНЯЕТСЯ ОТВЕТ H2+I2=2HI 48.Молялность РАВНА ОТНОШЕНИЮ КОЛИЧЕСТВА РАСТВОРЕННОГО ВЕЩЕСТВА К ОБЪЕМУ РАСТВОРА 49.К какому электроду при электрофорезе будет двигаться белок с изоэлектрической точкой 5 при значении ph 5 НЕ БУДЕТ ДВИГАТЬСЯ 50.К какому электроду при электрофорезе будет двигаться белок изоэлектрической точкой 6 при значении ph 9 К АНОДУ 51.Самопроизвольный процесс может быть при изменении энергии гиббса ОТРИЦАТЕЛЬНОЕ 52.Выберите гетерогенную систему из списка КРОВЬ 53.Система, в которой отсутствует обмен с окружающей средой энергией и веществом называется ИЗОЛИРОВАННАЯ 54.Эритроциты находятся в растворе хлорида натрия с массовой долей 15%Какой процесс при этом наблюдается ГЕМОЛИЗ 55.Процесс, проходящий при постоянном объёме, ИЗОХОРНЫЙ 56. Выберите пример гомогенного катализа ОКИСЛЕНИЕ АММИАКА КИСЛОРОДОМ ВОЗДУХА В ПРИСУТСТВИИ ОКСИДА ХРОМА 3 57.Молярная доля компонента рассчитывается как ОТНОШЕНИЕ КОЛИЧЕСТВА РАСТВОРЕННОГО ВЕЩЕСТВА К СУММЕ ВСЕХ КОЛИЧЕСТВ ВЕЩЕСТВ В РАСТВОРЕ 58.Давление, создаваемое за счёт наличия белков в биожидкостях организма называется ОНКОТИЧЕСКОЕ 59.Укажите вещество с наибольшей поверхностной активностью в гомологическом ряду МАСЛЯНАЯ КИСЛОТА 60.Температурный коэффициент скорости реакции равен 2 , температура в системе понизилась с 60 до 30 Как изменится скорость реакции УВЕЛИЧИТСЯ В 8 РАЗ 61.Функция состояния системы, которая является критерием возможности протекания самопроизвольного процесса называется ЭНЕРГИЯ ГИББСА 62.Обратимый процесс восстановления геля после его разжижжения в результате резкого механического воздействия называется ТИКСОТРОПИЯ 63.Поверхностная активность веществ одного и того же гомологического ряда возрастает примерно в 3 раза.....ПРАВИЛО ДЮКЛО-ТРАУБЕ 64.Коэффициент поверхностного натяжения это РАБОТА ОБРАЗОВАНИЯ ЕДИНИЦЫ ПОВЕРХНОСТИ 65.Выберите пример гомогенного катализа ВЗАИМОДЕЙСТВИЕ ГАЗООБРАЗНЫХ HCL И NH3 ПРИ УЧАСТИИ ПАРОВ ВОДЫ 66.Термодинамические, устойчивы, самопроизвольные организующиеся системы называются ЛИОФИЛЬНЫЕ 67.Укажите агрегатное состояние компонентов в дисперсной системе кровь ЖИДКОСТЬ-ДИСПЕРСНАЯ ФАЗА,ЖИДКОСТЬ - ДИСПЕРСИОННАЯ СРЕДА 68.Какой фактор не влияет на состояние равновесия в системе ИСПОЛЬЗОВАНИЕ КАТАЛИЗАТОРА 69. Какие растворы используются в медицине для внутрисосудистых инъекций ИЗОТОНИЧЕСКИЕ 70.Какое количество атомов содержится в 0,5 моль азота(газ) 3.01 *10^23 71.При повышении температуры на 10 градусов скорость реакции увеличится в 2-4 раза ПРАВИЛО ВАНТ-ГОФФА 72.Свойства катализаторов ПОВЫШАЮТ ЭНЕРГИЮ АКТИВАЦИИ 73.Какое количество молекул содержится в 0,5 моль азотной кислоты ОТВЕТ 3,01*10(В 23 СТЕПЕНИ) 1.Степень диссоциации слабой кислоты зависит от -природы вещества 2.Щелочную среду имеет раствор -сульфит натрия 3.pH раствора H2SO4 с концентрацией 0,005 моль/л равен -2 4.По катиону гидролизуется соль -нитрат аммония 5.Фенолфталеин в щелочной среде придает раствору цвет -малиновый 6.Кислую среду имеют растворы -хлорида аммония, сульфата железа 7.По аниону гидролизуется соль -сульфит натрия 8.Ионному произведению воды соответствует выражение -Кводы = [H+]*[OH-] 9.Отношение количества электролита, распавшегося на ионы, к общему количеству растворенного электролита называют -степенью электрической диссоциации 10.Ионное произведение воды численно равно -10-14 11.Нейтральную среду имеет раствор -бензоат аммония 12.Концентрация протонов в растворе с pOH 4,0 равна -1,0*10-10 13.Не подвергается гидролизу соли -хлорид натрия, сульфат лития 14.По катиону и аниону гидролизуются соли -ацетат аммония, сульфид цинка 15.При расчете водородного показателя концентрацию протонов вырожают в единицах -моль/л 16.pH раствора NaOH с концентрацией 0,001 моль/л равен -11 17.Значение pH крови при субкомпенстрованном алкалозе составляет -7,45-7,55 18.Значение pH жидкости организма находится вне границ нормы Моча 2-3 19.Для купирования ацидоза можно ввести в распорядок дня -прогулки на свежем воздухе 20.Значение pH жидкости организма находится вне границ нормы -желудочный сок 3-6 21.Среда нейтральная, если соблюдается условие -[OH] = 10-7 моль/л 22.Для купирования ацидоза можно ввести в диету -арбузы 23.Смещение pH крови в область 7,2-7,3 называется -ацидемия 24.Для купирования алкалоза можно применить -аммония хлорид 25.Для купирования ацидоза можно ввести в диету -клубничное варенье 26.Значение pH крови при субкомпенстрованном ацидозе составляет -7,25-7,35 27.Значение pH крови в норме составляет -7,35-7,45 28.Значение pH крови при алкалозе составляет -7,45-7,8 29.Среда нейтральная, если соблюдается условие -pOH=7 30.Для купирования ацидоза можно применить -натрия карбонат 31.Для купирования респираторного ацидоза можно -выполнить дыхательные упражнения 32.Среда щелочная, если соблюдается условие -pOH < 5 33.Формула расчета pH -pH = -lg[H+] 34.Среда кислая, если соблюдается условие -[H+] > [OH-] 35.Значение pH жидкостей организма находится в границах нормы -кровь 7,35-7,45, моча 5-7 36.Кровезаменяющие растворы для внутривенного влияния должны иметь pH -около 7,35 37.Укажите ошибку! Донорами в буферных системах являются -Hb в гемоглобиновой 38.Укажите ошибку! В кислой моче могут быть представлены -угольная кислота и дигидрофосфатная система 39.Укажите ошибку! Донорами в буферных системах являются -H2CO3 40.Укажите ошибку! Буферные системы представлены -аммиачная и ацетатная во внеклеточной жидкости 41.Укажите ошибку! Буферными системами являются -Na2CO3/CaHCO3 42.Акцептором «H+» в гидрокарбонатной буферной системе является -HCO3- 43.Протолитические буферные системы – это водные растворы, поддерживающие постоянное значение -pH 44.Донором в гидрокарбонатной буферной системе является -H2CO3 45.Укажите ошибку! Акцепторными в буферных системах являются -HCO3- в карбонатной 46.pH аммиачной буферной системы можно рассчитать по уравнению -pH = 14-pKb + lg[NH4OH/NH4+] 47.Укажите ошибку! Буферными системами являются -трисамин 48.pH гидрофосфатной буферной системы рассчитать по уравнению -pH=pK+lg[HPO42-/H2PO4-] 49.Буферными системами являются все смеси в выборке -H3PO4/NaH2PO4, Na3PO4/Na2HPO4 50.Буферная система, функционирующая только в эритроцитах -гемоглобиновая 51.Укажите ошибку! Буферными системами являются смеси -сильная кислота и ее соль 52.В фосфатном буфере добавляемая кислота связывается -ионом HPO42- 53.Укажите ошибку! При купировании ацидоза и алкалоза рекомендованы -гидрофталат натрия и дигидрофосфат калия 54.В гидрофосфатном буфере добавляемая кислота связывается -ионом H2PO4- 55.Буферными системами являются все смеси в выборке -HCN/NaCN, CH3COOH/CH3COONa 56.Укажите ошибку! Акцепторами в буферных системах являются -H3PO4 в фосфатной 57.Окислительно-восстановительная двойственность характерна для -перекиси водорода 58.Двойственными окислительно-восстановительными свойствами обладает ион -сульфит 59.Продуктами реакции KMnO4 + K2SO3 + H2O являются -MnO2 + K2SO4 + KOH 60.Укажите ошибку! Продукт восстановления перманганата иона в зависимости от среды -MnO42- в кислой 61.Донор электронов в окислительно-восстановительных реакциях выполняет роль -восстановления 62.Степень окисления марганца в перманганат-ионе [MnO4]- равна -+7 63.Полуреакции восстановления окислителя представлены в выборке - 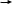 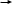 Fe2 Fe3+;Cr2O72- Cr3+ Fe2 Fe3+;Cr2O72- Cr3+64.Укажите ошибку! Роль частицы в окислительно-восстановительных реакциях -марганца (III) катион-окислитель 65.Электродный потенциал медного электрода его стандартному значению при активной концентрации ионов равной: -1,0 моль/кг 66.Укажите ошибку! Окислительно-восстановительная роль частицы -дихромат анион – восстановитель 67.Пероксид водорода в полуреакции H2O2 = 2OH- выполняет роль -восстановителя в щелочной среде 68.Укажите ошибку! Антиоксиданты представлены в перечне -анальгин, симетикон 69.В электрохимическом ряду напряжений металлы расположены по возрастанию -стандартных электродных потенциалов 70.Укажите ошибку! Роль частицы в окислительно-восстановительных реакциях -хромат анион-восстановитель 71.Укажите ошибку! Соединения с окислительно-восстановительними свойствами, которые применяются в качестве лекарственных средств -дихромат калия 72.Укажите ошибку! Роль частицы в окислительно-восстановительных реакциях -дихромат анион-восстановитель 73.Укажите ошибку! Окислительный стресс это -снижение психической устойчивости во время эпидемии 74.Полуреакции окисления восстановителя представлены в выборке - 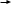 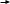 Mn-2 MnO4-; Zn0 Zn2+ Mn-2 MnO4-; Zn0 Zn2+75.Частица, принимающая электроны в окислительно-восстановительных реакциях, выполняет роль -окислителя 76.Наибольшую склонность к комплексообразованию имеют -d-элементы 77.Укажите ошибку! Характеристики соединения [Cr(H2O)3F3] -заряд внутренней сферы 3+ 78.Перечислены комплексные соединения только катионного типа -[Cu((NH3)4]SO4, [Ni(H2O)(NH3)5]Cl2, [Ag(NH3)2]Cl 79.Укажите ошибку! Тип гибридизации комплексного соединения и строение частицы -sp3d2 – тетраэдрическое 80.Укажите ошибку! Центральный атом в биологическом комплексе -хлорофилл –Cu2+ 81.Укажите ошибку! Внутренняя сфера комплексного соединения может быть -радикалом 82.Координационное число комплексообразователя в K4[Fe(F)6] равно -6 83.Кобальт входит в состав -витамина B12 84.Частица, занимающая центральное место в комплексном соединении называется -комплексообразователь 85.Перечислены комплексные соединения являющиеся кислотами -H2[PbCl4], H[Cr(H2O)2(CNS)4] 86.Укажите ошибку! Характеристики соединения K2[PtI4] -координационное число 2 87.Укажите ошибку! Центральный атом в биологическом комплексе -цианокобаламин – Zn2+ 88.Укажите ошибку! Характеристика соединения [Ni(CO)4] -заряд внутренней сферы 4+ 89.Перечислены комплексные соединения с координационным числом центрального атома 6 -[Cd(NH3)3(H2O)3]SO4, K[Cr(H2O)2(CNS)4, [Co(H2O)4(OH)2] 90.Название «сульфат гексааквакобальта II» соответствует соединению -[Co(H2O)6]SO4 91.Комплексным называют соединение, в котором присутствует хотя бы одна -ковалентная связь 92.Укажите ошибку! Тип гибридизации комплексного соединения и строения частицы -sp3d2 – тетраэдрическое 93.Перечислены комплексные соединения являющиеся нейтральным (недиссоциирующими) -[Fe(H2O)4(OH)2], [Ni(CO)4] 94.Название «дигидроксотетраакважелезо II» соответствует соединению -[Fe(H2O)4(OH)2] 95.Название «сульфат гидроксопентаакважелеза III» соответствует соединению -[Fe(H2O)5(OH)]SO4 96.Перечислены комплексные соединения с координационным числом центрального атома 4 -K2[PbCl4], [Cu(NH3)4]SO4, [Ni(CO)4] 97.Укажите ошибку! Характеристики соединения K2[PtI4] -координационное число 2 98.Укажите ошибку! Лигандом комплексного соединения может быть -катион металла 99.Перечислены комплексного соединения анионного типа -K4[CdCl6], K[Cr(H2O)2(CNS)4], Na2[HgBr4] 100.В медицине используется в качестве лекарственного препарата раствор -K[I3] 101.Укажите ошибочно составленное выражение произведения растворимости по формуле соли (ПР обозначает Ks) ZnS ПР=[K][A] -Cu(NO3)2 Понятие ПР неприменимо 102.Основным неорганическим соединением кальция в ткани кости является -Ca10(PO4)6(OH)2 103.Найдите ошибку! Наборы продуктов, богатых хорошо усвояемым кальцием -подсолнечное масло сахар 104.Условием выпадения осадка является (ПР обозначает Ks) -ИП > ПР 105.Раствор, в котором при данной температуре не может растворится дополнительное количество растворяемого вещество, является -насыщенным 106.Осадок растворится при условии (ПР обозначает Ks) -ИП < ПР 107.Наиболее растворимая соль, исходя из значения константы растворимости (ПР обозначает Ks) -BaCO3 ПР=3,3*10-5 108.Состояние, при котором из ткани кости выходит неорганическая составляющая называется -остеопороз 109.Произведение растворимости (ПР обозначает Ks) бинарного электролита равно 10-10, его растворимость (моль/л) равна -1*10-5 110.Кислотность мочи при образовании камней в почках -при снижении pH мочи уратные 111.Раствор, в котором при данной температуре может растворится дополнительное количество растворимого вещества, является -ненасыщенным 112.Укажите ошибочно составленное выражение произведения растворимести по формуле соли (ПР обозначает Ks) -BaSO4 ПР=[K+][A-] 113.Максимальная концентрация карбонат-иона наблюдается в насыщенном растворе (ПР обозначает Ks) -CdCO3 ПР=2,5*10-14 114.Укажите наиболее растворимую соль -CaCrO4 (ПР=7*10-4) 115.Нарушение остеосинтеза, связанное с недостаточностью минерализация костей называется -рахит 116.Ионное произведение (ИП) показывает -концентрации ионов малорастворимого вещество 117.Процессы, связанные с нарушением гетерогенного равновесия -образования камней в почках, кариес 118.Исходя из константы растворимости (ПР обозначает Ks), укажите соль, которая первая выпадает в осадок при добавлении корбонат-ионов -CdCO3 ПР=2,5*10 ( в минус 14) 119.Кислотность мочи при образовании камней в почках -при снижении pH мочи уратные 120.В природном апатите ткани зуба гидроксильные группы частично замещены анионом -F- 121.Камни в почках бывают -оксатальные, фосфатные, уратные, цистиновые 36)Если в 20 грамм вещества растворить в 80 граммах воды, то массовая доля компонента будет –20% 38)Найдите реакцию , в которой энтропия не изменяется –H2+I2=2HI 40)Основным неорганическим соединением кальция в ткани кости является – Ca10(PO4)6(OH)2 7. окислительно – восстановительная двойственность характерна для- перекиси водорода 9. Камни в почках бывают- оксалатные, фосфатные , уратные, цистиновые 12. размерность моляльной концентрации – моль\кг 40. основным неорганическим соединением кальция в ткани кости является- Ca10(PO4)6(OH)2 41.Концентрация протонов в растворе с pOH 4,0 равна-1,0*10 (в -10) 44. Дано уравнение ( образ NH3) если объем в системе увеличить в 2 раза, то скорость прямой реакции- увеличится в 2 раза 46. Степень окисления марганца в перманганат – ионе ( MnO4) равна - +7 47. Фактор, не влияющий на состояние равновесия в системе- использование катализатора 48.Протолитические буферные системы- это водные растворы, поддерживающие постоянное значение- ph 25)Координационное число комплексообразователя в K4[Fe(F)6] равно –6 26)Раствор с массовой долей глюкозы 0,5 % по отношению к плазме крови является –гипотоническим 27)Обнаружить примесь салициловой кислоты в ацетилсалициловой кислоте можно по реакции с –хлоридом железа 3 31)Наиболее растворимая соль ,исходя из значения константы растворимости –CdCO3 ПР=2,5*10-14 35)Буферная система , функционирующая только в эритроцитах –гемоглобиновая 36)Если в 20 грамм вещества растворить в 80 граммах воды, то массовая доля компонента будет –20% 38)Найдите реакцию , в которой энтропия не изменяется –H2+I2=2HI 40)Основным неорганическим соединением кальция в ткани кости является – Ca10(PO4)6(OH)2 1. pH водного раствора KOH равен 12, молярная концентрация вещества в растворе равна- 10 в минус 12моль\л 3. Перечислены комплексные соединения только анионного типа- K4(CdCl6)\ K(Cr(H2O)2(CNS)4)\ Na2(HGBr4) 5. При повышении температуры на 10 градусов скорость реакции увеличивается в 2-4 раза-правило Вант-Гоффа 13. Количество молей вещества в 200 миллимоль N2-2 15. Железо входит в состав – гемоглобина 19.Значение pH крови в норме составляет-7,35-7,45 Донором в гидрокарбонатной буферной системе является- H2co3 |
