Теория горения и взрыва. ТГиВ 2 вариант. Образовательное учреждение высшего образования академия государственной противопожарной службы министерства российской федерации по делам
 Скачать 87.65 Kb. Скачать 87.65 Kb.
|
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ АКАДЕМИЯ ГОСУДАРСТВЕННОЙ ПРОТИВОПОЖАРНОЙ СЛУЖБЫ МИНИСТЕРСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ ПО ДЕЛАМ ГРАЖДАНСКОЙ ОБОРОНЫ, ЧРЕЗВЫЧАЙНЫМ СИТУАЦИЯМ И ЛИКВИДАЦИИ ПОСЛЕДСТВИЙ СТИХИЙНЫХ БЕДСТВИЙ Институт управления и комплексной безопасности Кафедра: Процессы горения Дисциплина: Теория горения и взрыва Курсовая работа Вариант № 2 Выполнил: студент 3120С учебной группы Биджиев А.Р. Проверил: Профессор кафедры процессов горения, к.т.н. Комраков П. В. Москва 2021г.
Часть 1 Расчет адиабатической температуры горения (Тад) методом последовательных приближений: С5H12О +7.5(O2+3,76N2 )→ 5CO2+6H2O+7.5*3,76N2 где: VCO2=5 моль/моль; VH2O=6 моль/моль; VN2=7.5*3,76=28.2 моль/моль; Vпг=39.2моль/моль; По закону Гесса расчет низшей теплоты сгорания Qн=H0fCO2nCO2+H0fH2OnH2O-H0C5H12ОnC5H12О=5*396,6+6*242,2-102,3=3333,9(кДж/моль) Среднее теплосодержание продуктов горения Hср= Qн/∑Vпгi= 3333,9/39,2=85(кДж/моль) Ориентируясь на азот, установил, какой температуре соответствует такое тепловыделение. При Т1=23000С: Q`пг=VСО2НСО2+VH2OHH2O+VN2HN2=5*126,9+6*104,2+28,2*77,8 = 3453,6(кДж/моль) т.к. Q`пг Qн , →Т2=22000С. Q``пг=VСО2НСО2+VH2OHH2O+VN2HN2=5*120,8+6*98,8+28,2*74,1= 3286,4(кДж/моль) Q`пг Qн Q``пг →температура горения имеет значение между 2300 и 2200. Установим методом линейной интерполяции: Тадг=Т2+(Т1-Т2)(Qн-Q2)/(Q1-Q2)=(2200+(2300-2200)*(3333,9-3286,4)/(3453,6-3286,4)=2501К Расчет температуры взрыва(Твз): Qн = 3333,9 (кДж/моль) Среднее значение вн. продуктов взрыва: Vср= Qн/∑Vпгi= Hср=85(кДж/моль) Из таблицы 2, ориентируясь на азот, установил, какой температуре соответствует такое значение вн. энергии: Т1=28000С: Q1=5*134,2+6*107+28,2*73,1= 3374(кДж/моль) Т2=27000С: Q2=5*128,9+6*102,4+28,2*70,2=3238,5(кДж/моль) т.к. Q1 Qн Q2 → температура взрыва имеет значение между 2800 и 2700. Установим методом линейной интерполяции: Твз=Т2+(Т1-Т2)(Qн-Q2)/(Q1-Q2)=2700+(100*(3333,9-3238,5)/3374-3238,5=2770(0С)=3043К Концентрационные пределы распространения пламени (КПР) ϕн(в)=100/(аn+b): где n=7,5, значения а=8,684; b=4,679- для нижнего предела. ϕн=100/(8,684*7,5+4,679)=1,4% Значения a=0,768; b=6,554- для верхнего предела. ϕв= 100/(0,768*7,5+6,554)=8,1% Расчет минимальной флегматизирующей концентрации (МФК) Воспользовались уравнением теплового баланса С5H12О+5O2+5*3,76N2CO+6H2O+5*3,76N2 Qн=5*112,7+6*242,2-102,3=1914,4(кДж/моль) Значения Ср приведены в таблице. Vф = =13,9( моль/моль) Минимальная флегматизирующая концентрация равна ϕмфк=(nф*100)/(nг+ nО2+ nN2+ nф) =36% ϕг= 1*100/(37,6)=2,6% По полученным данным КПР, МФК и концентрации горючего в точке флегматизации строим график зависимости КПР от коцентрации флегмфтизатора     8  7  6  5   4  3    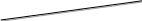 2  1        0 0 10 20 30 40 Минимальное взрывоопасное содержание кислорода (МВСК) ϕО2=(nО2*100=(5*100)/38,\=13% Температурные пределы распространение пламени (ТПР) определяют по расчётным значениям концентрационных пределов, использовали уравнение Антуана. Рн=ϕн*Ро/100=1,4*101325/100=1418,5 (Па) Рв=ϕв*Ро/100=8,1 *101325/100=8207,3 (Па) Рн= = 7 мм.рт.ст. Рв= 61,554 мм.рт.ст. t= (B/(A-lgP))-C из таблицы : А=6,44711; B=1252,216; С=180,301. lgPн= lg1,418= 0,15 lgPв= lg8,2073= 0,91 tн= (1252,216/(6,44711-0,15))-180,301= 18,50C)(K) tв=(1252,216/(6,44711-0,91))-180,301= 45,8(0C) 318(K) Расчет температуры самовоспламенения вещества (Тсв) Определяем по длине углеводородной цепи Структурная формула: |
| 1-4 | 1-6 | 4-5 | 4-6 | 1-5 | |
| 4 | 2 | 4 | 3 | 3 | |
По таблице 9 определяем Тсв=528К=255оС
Максимальное давление взрыва (Рмах) рассчитываем по формуле 4.1
Рмахвз= (Po*Tвзр*nпг)/(nc*To) , где То=273К, Ро=101,3кПА, Твз=3043К;
nпг=39,2 моль; nс=24,8 моль.
Рмахвз =(101325*3043*39,2)/(24,8*273)=1785к Па
Тротиловый эквивалент вещества (тнт)
тнт=Qвзр/Qтнт=37885/4187=9,05кг
где Qтнт=4187 (кДж/кг)-теплота взрыва тротила,
Qвзр=3333,9/(88*10-3)=37885 кДж/кг
Часть 2
Заносим в таблицу рассчитанные параметры
| Параметр горения и взрыва | Тад, (К) | Твз, (К) | КПР, % | МФК (N2), % | МВСК, % | ТПР, (К) | Tсв, (К) | Рмах, (Па) | тнт |
| Значение параметра | 2501 | 3043 | ϕв=8,1 ϕн=1,4 | 36 | 13 | Тн=291,8 Тв=318 | 528 | 1785,2 | 9,05 |
Вывод пожарной опасности вещества: температура самовоспламенения по расчетным данным велика, объясняется погрешностями расчета, а также влиянием исходной температуры.
Часть 3
Количество вещества (кг), которое должно испарится из уравнения материального баланса горения найдем стехиометрическую концентрацию вещества А:
ϕст= 1*100/(1+7,5+7,5*3,76)=2,72%
Найдем объем помещения :
Vпом=5,0*4,0*2,5=50(м3)
Объем паров помещения:
Vп=ϕст*Vпом= 0,0272*50=1,36 (м3)
М=88*10-3кг/кмоль mг=88*1,36/22,4 =5,34 кг
Тротиловый эквивалент взрыва (Мтнт) парогазовой смеси в помещении
Мтнт=mQтнт, где m-кол-во горючего вещества, - доля потенциальной энергии перешедшей в кинематическую взрыва (=1)
Мтнт=9,05*5,34*1=48,3 (кг тротила)
Размер безопасной зоны (Rбез) по действию давления воздушной ударной волны:
Rбез=15 (Мтнт)1/3=15*(43,8)1/3 = 52,8 (м)
Определение количества диоксида углерода (МСО2):
С5H12O+ 7,5(O2+*3,76N2)+nфСО25CO2+6H2O+7,5*3,76N2+nфСО2
Qн=(3333,9-(1500-273)(5*50,85+6*39,87+7,5*3,76*31,81)*10-3)/((1500-273)*50,85*10-3 )=( моль/моль) 5*112,7+6*242,2-102,3=1914,4(кДж/моль)
Vф =13,9 моль/моль
Фмфк=13,9*100/(1+7,5+7,5*3,76+13,9)=27,4
Vпco2=27.4*88/100=24.1м3=1.07кмоль
mпco2=1.07*100=107.5кг
Параметры взрыва паровоздушной смеси вещества А:
| Параметр горения и взрыва | Vпом, м3 | Mг, кг | Мтнт, Кг | Rбез, М | МСО2, кг |
| Значение параметра | 50 | 5,34 | 48,3 | 52,8 | 107.5 |
Вывод: в курсовой работе определили параметры горения и взрыва горючего вещества: трет-амиловый спирт(С5Н12О)
С точки зрения пожарной охраны наиболее важны концентрационные пределы распространения пламени:
ϕн=1,4% ϕвн=8,1%
Определили уровни образования наиболее взрывоопасной паровоздушной смеси, параметры взрыва и рассчитали количество флегматизатора, необходимого для предотвращения взрыва такой смеси.
Литература:
Примеры и задачи по курсу «Теория горения и взрыва», А.С. Андросов, Е.П. Салеев, 2008 г. Москва.
Справочник «Пожаровзрывоопасность веществ и материалов и средств их тушения» Москва – «Химия», 1990г.