контрольные и самостоятельные работы по теме Кислородосодержащие. кр и см кислородосодержащие. Одноатомные спирты
 Скачать 42.3 Kb. Скачать 42.3 Kb.
|
|
САМОСТОЯТЕЛЬНАЯ РАБОТА « одноатомные СПИРТЫ» Назовите вещество: 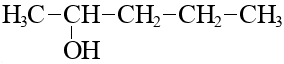 2. Составьте формулу изомера для вещества, указанного в задании 1, и назовите его. 3.Вещества, формулы которых 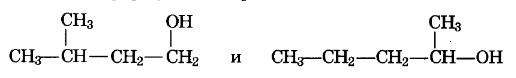 Являются: Изомерами Гомологами Одним и тем же веществом Веществами разных классов 4.В схеме превращений C2H2-> А-> Б (+вода,ортофосфорная кислота;Оксид меди) Вещества А и Б являются: Этан Этановая кислота Этанол Диэтиловый эфир Метилацетат 5.По термохимическому уравнению Вычислите массу этанола, которая потребуется для получения 130кДж теплоты. САМОСТОЯТЕЛЬНАЯ РАБОТА «многоатомные СПИРТЫ» 1. Укажите формулы пропандиола-1,3 и пропандиола-1,2. 1) СН2ОН-СНОН-СН2OН 2) СН2ОН-СН2OН-СН2OН 3) СН2ОН-СНОН-СН3 4) СН2ОН-СНОН-СНОН-СН3 5) СН2ОН-СНОН-СН2-СН2OН 2. Различить этановый спирт и глицерин можно с помощью: Серная кислота Фенолфталеин Оксид меди(II) Гидроксид меди(II) 3. Этиленгликоль можно получить при взаимодействии в растворе между собой следующих веществ: 1) CH-CH 2) СН2=СН2 3) KMnO4 4) HBr 5) Cu(OH)2 4. Определите вещества X и Y в схеме этан → X → этанол → Y → этиленгликоль 1) метанол 2) глицерин 3) 1,1-дихлорэтан 4) этилен 5) хлорэтан 5. При взаимодействии калия с избытком этиленгликоля выделилось 980мл (н.у.) водорода. Определите а) массу выделившегося водорода б) массу вступившего в реакцию калия 1) 2) 3) 4) 5) САМОСТОЯТЕЛЬНАЯ РАБОТА «Фенол» 1.Выберите молекулярную формулу фенола C6H5-CH3 С2Н5ОН С6Н5-ОН С3Н5(ОН)3 2. Фенол реагирует с гидроксидом натрия с образованием Глицерат натрия Циклогексан Фенолят натрия Бензоат натрия 3. Фенол и глицерин нельзя различить с помощью Раствором марганцовки Бромной водой Хлоридом железа Гидроксидом меди (II) 4. Перечислите все химические свойства фенола 5.Рассчитайте массу фенолята натрия, который потребуется для получения 10,49г фенола. САМОСТОЯТЕЛЬНАЯ РАБОТА «Альдегиды» 1. Составьте структурную формулу вещества, название которого 4-этилгексан-3-аль. 2. Для вещества из задания 1 составьте формулу изомера и гомолога 3.Уксусный альдегид нельзя получить из: Ацетилена и воды Этанового спирта и кислорода Этанола и оксида меди(II) Этена и воды 4. Наличие альдегидной группы в органическом веществе можно установить с помощью бромной воды аммиачного раствора Ag2O индикатора – лакмуса гидроксида натрия. 5.Составьте уравнения реакции, с помощью которых можно осуществить следующие превращения: Пентаналь-пентанол-1-пентен-пентин САМОСТОЯТЕЛЬНАЯ РАБОТА «Карбоновые кислоты» 1. Молекулярная формула карболовой кислоты: а) С2Н5ОН С6Н5ОН С6Н5 – СН2ОН СН3ОН 2. Функциональная группа карбоновых кислот называется 1) карбонильной 2) гидроксильной 3) карбоксильной 4) сложноэфирной 3. Обесцвечивает бромную воду кислота 1) пальмитиновая 2) олеиновая 3) стеариновая 4) уксусная 4. В реакцию этерификации вступают: а) спирт и альдегид б) фенол и натрий в) спирт и карбоновая кислота г) два спирта Напишите уравнения этих реакций 5. Определите вещества X и Y в схеме этан → уксусная кислота → метилацетат (+Х, +У) Водород Этанол Оксид меди (II) Гидроксид меди (II) Контрольная работа 1.В названиях спиртов используют суффикс а) – ол б) –ил в) – ин г) – ан 2. Вещество, формула которого СН3 ОН является а) алканом б) спиртом в) альдегидом г) карбоновой кислотой 3.Укажите, с какими из веществ взаимодействует пропанол-1: а) калий б) гидроксид натрия в) бромоводород г) конц.серная кислота 4.Найдите вещество, образующегося при окислении бутанола-2 а) альдегид б) карбоновая кислота в) кетон г) бутанол-1 5.Этилат натрия получается при взаимодействии а) СН3ОН с Na б) СН3ОН с NaОН (раствор) в) С2Н5ОН с Na г) С2Н5ОН с NaОН (раствор) 6. Для осуществления превращения фенол → фенолят калия + вода необходимо к фенолу прибавить а) калий б) оксид калия в) гидроксид калия г) хлорид калия 7.При бромировании фенола избытком брома образуется а) 2 – бромфенол б) 2,3 – дибромфенол в) 2,5 – дибромфенол г) 2,4,6 – трибромфенол 8. При окислении альдегидов образуются: а) фенолы; б) углеводороды; в) спирты; г) кислоты. 9. Реактивом для определения альдегидов является: а) водород; б) раствор KMnO4; в) бром; г) аммиачный раствор оксида серебра. 10. Щавелевая кислота является: а) двухосновной; б) одноосновной; в) непредельной; г) многоосновной. 11. Для качественного определения непредельной олеиновой кислоты применяют: а) водород; б) бромную воду; в) гидроксид меди (II); г) синий лакмус. 12. Изомером бутановой кислоты является а) метилацетат б) этилацетат в) этиловый спирт г) этилформиат 13. Из формальдегида массой 45 г образуется метанол массой … г , при выходе 95 %. а) 40 г; б) 45 г; в) 120 г; г) 80г. 14. Вычислите массу метилового эфира уксусной кислоты, который может быть получен при взаимодействии 90 г. 10% раствора уксусной кислоты с 16 г. метанола, если выход продукта реакции составляет 85%. 15.Осуществите превращение: +H2O, Hg2+/ H+ СН4 → С2Н2 → Х → CH3СОOH → CH3СОOСН3 → CH3СОOК |
