отчёт эквивалент. отчёт лр№1. Определение эквивалентной массы металла
 Скачать 37.41 Kb. Скачать 37.41 Kb.
|
|
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ В РОССИИ  МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ федеральное государственное бюджетное образовательное учреждение высшего образования «САНКТ-ПЕТЕРБУГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ» Кафедра общей химии Лабораторная работа №1 По дисциплине ХИМИЯ Тема: Определение эквивалентной массы металла Автор: студент гр. САМ-22 /Скуковский П. А./ подпись (Ф.И.О.) ОЦЕНКА: ______________ Дата: ___________________ ПРОВЕРИЛ / . . / должность подпись (Ф.И.О.) Санкт-Петербург 2022 год Цель работы: Усвоить понятие о химическом эквиваленте и научиться определять эквивалентны вещества Ход эксперимента: 1. Наполнить водой кристаллизатор и бюретку (стеклянную трубку с делениями и краном для выпуска жидкости внизу). Проверить, плотно ли закрыт кран бюретки. 2. Закрыв верхнее отверстие пальцем, перевернуть бюретку и опустить ее в кристаллизатор с водой. Палец убрать под водой, при этом вода из бюретки не вытечет. 3. Закрепить бюретку в штативе. Уровень волы в ней не должен быть выше крайнего деления шкалы. 4. В колбу Вюрца (круглодонная колба с боковым отводом) при помощи мерного цилиндра отобрать 15-20 мл соляной кислоты: 5. Вытереть насухо горло колбы фильтром. 6. Расположив колбу горизонтально, поместить в се горло навеску металла плотно закрыть колбу пробкой. 7. Стеклянную трубку бокового отвода колбы Вюрца соединить с расположенной под водой частью бюретки. 8. Отметить уровень жидкости в бюретке, Показания следует снимать по положению нижнего края вогнутого мениска жидкости при нахождении сто на уровне глаз. Цифры на шкале бюретки - объем в миллилитрах (мм), при снятии показаний необходимо учитывать, что бюретка со шкалой перевернута. 9. Перевести колбу в вертикальное положение, сбрасывая навеску металла в кислоту. В результате реакции выделяется водород, который вытесняет воду из бюретки. Во время протекания реакции не следует держать колбу в руках во избежание се нагревания и искажения результатов за счет теплового расширения газа. 10. Когда выделение пузырьков водорода прекратите, отметить конечный уровень воды в бюретке. 11. При помощи полоски миллиметровой бумаги измерить высоту столба воды в бюретке от нижнего края мениска до уровня волы в кристаллизаторе. 12. По показаниям барометра и термометра определить атмосферное давление и температуру в лаборатории. Экспериментальные данные: Масса навески металла -  = 0,0123 г = 0,0123 гОбъем воды в бюретке в начале эксперимента —  = 24,9 мл. = 24,9 мл.Объем воды в бюретке по окончании эксперимента —  = 10,6 мл = 10,6 млОбъем выделившегося водорода —  = =  — —  = 14,3 мл = 14,3 млВысота столба воды в бюретке — h = 245 мм. Атмосферное давление в лаборатории —  = 98525 Па = 98525 ПаТемпература в лаборатории — Т=24 °С =297К Обработка экспериментальных данных   P =  P = 98525 – 2352 – 3172,5 = 93000,5 Па P = 98525 – 2352 – 3172,5 = 93000,5 Па = =   = =  = 0,001076 г. = 0,001076 г.  (Me) = (Me) =   (Me) = (Me) = = 11,43 = 11,43  Валентность 2 => Mg =>  (Me)=12,1525 (Me)=12,1525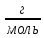 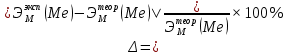 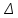 = = 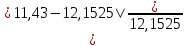 *100% = 5,94 % *100% = 5,94 %P – давление водорода V – объём водорода  – давление столба воды в бюретке – давление столба воды в бюретке R = 8,31  – универсальная газовая постоянная – универсальная газовая постоянная – давление насыщенного пара – давление насыщенного пара  (Н) = 1 (Н) = 1  – эквивалентная масса водорода – эквивалентная масса водорода - 1000 - 1000  – плотность воды – плотность воды – масса выделившегося водорода – масса выделившегося водорода = 2 = 2  Вывод: Благодаря лабораторной работе я усвоил понятие о химическом эквиваленте и научился определять эквивалентные массы вещества. В ходе эксперимента определил металл экспериментально – магний. |
