Определение кислотности нефтепродуктов методом потенциометрического титрования
 Скачать 0.58 Mb. Скачать 0.58 Mb.
|
|
ПЕРВОЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ  МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ федеральное государственное бюджетное образовательное учреждении высшего образования «САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ» Кафедра общей и физической химии Лабораторная работа № 1 По дисциплине: «Органическая химия» на тему: «Определение кислотности нефтепродуктов методом потенциометрического титрования»
Оценка:__________ Дата:_____________
Санкт-Петербург 2023 год Теоретический материал: Титрование – метод количественного анализа, основанный на измерении объема раствора реагента точно известной концентрации, расходуемого для реакции с определяемым веществом. Точка эквивалентности – это точка на кривой титрования, в которой количество затраченного титранта эквивалентно количеству реагирующего с ним вещества. Потенциометрическое титрование – способ определения объема титранта, затраченного на титрование определяемого вещества в анализируемом растворе, путем измерения ЭДС с помощью гальванической цепи, составленной из индикаторного электрода и электрода сравнения. Комбинированными называются электроды, объединяющие в одном корпусе измерительный электрод и электрод сравнения. Кислотность – это мера концентрации ионов водорода в растворе. Цель работы: определить уровень кислотности в предложенной пробе нефтепродукта. Сущность метода: определение уровня кислотности основано на реакции нейтрализации 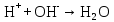 . Вследствие протекания реакции потенциал стеклянного электрода постепенно понижается. Как только все ионы . Вследствие протекания реакции потенциал стеклянного электрода постепенно понижается. Как только все ионы 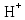 окажутся связанными, наступает резкий скачок потенциала. При дальнейшем добавлении щелочи потенциал электрода меняется незначительно. окажутся связанными, наступает резкий скачок потенциала. При дальнейшем добавлении щелочи потенциал электрода меняется незначительно.Ход работы: в стакан налили 50 мл пробы нефтепродукта. Поместили в стакан якорь магнитной мешалки. Установили стакан на магнитную мешалку и включили ее. Опустили комбинированный электрод в стакан с пробой. Включаем pH-метр в режим измерения ЭДС. Титруем раствором KOH с шагом 0,5 мл 14 раз. Обработка экспериментальных данных:
Пример расчета: рассчитаем ΔЕ/ΔV для №5 ΔЕ = 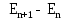 = = 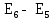 = -0,540+ 0,650 = 0,11 мВ = -0,540+ 0,650 = 0,11 мВΔЕ/ΔV = 0,11/0,5 = 0,22 В/л На основании полученных результатов строим график зависимости Е от 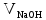 и дифференциальную кривую (зависимость ΔЕ/ΔV от и дифференциальную кривую (зависимость ΔЕ/ΔV от 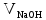 ). ).Графики: 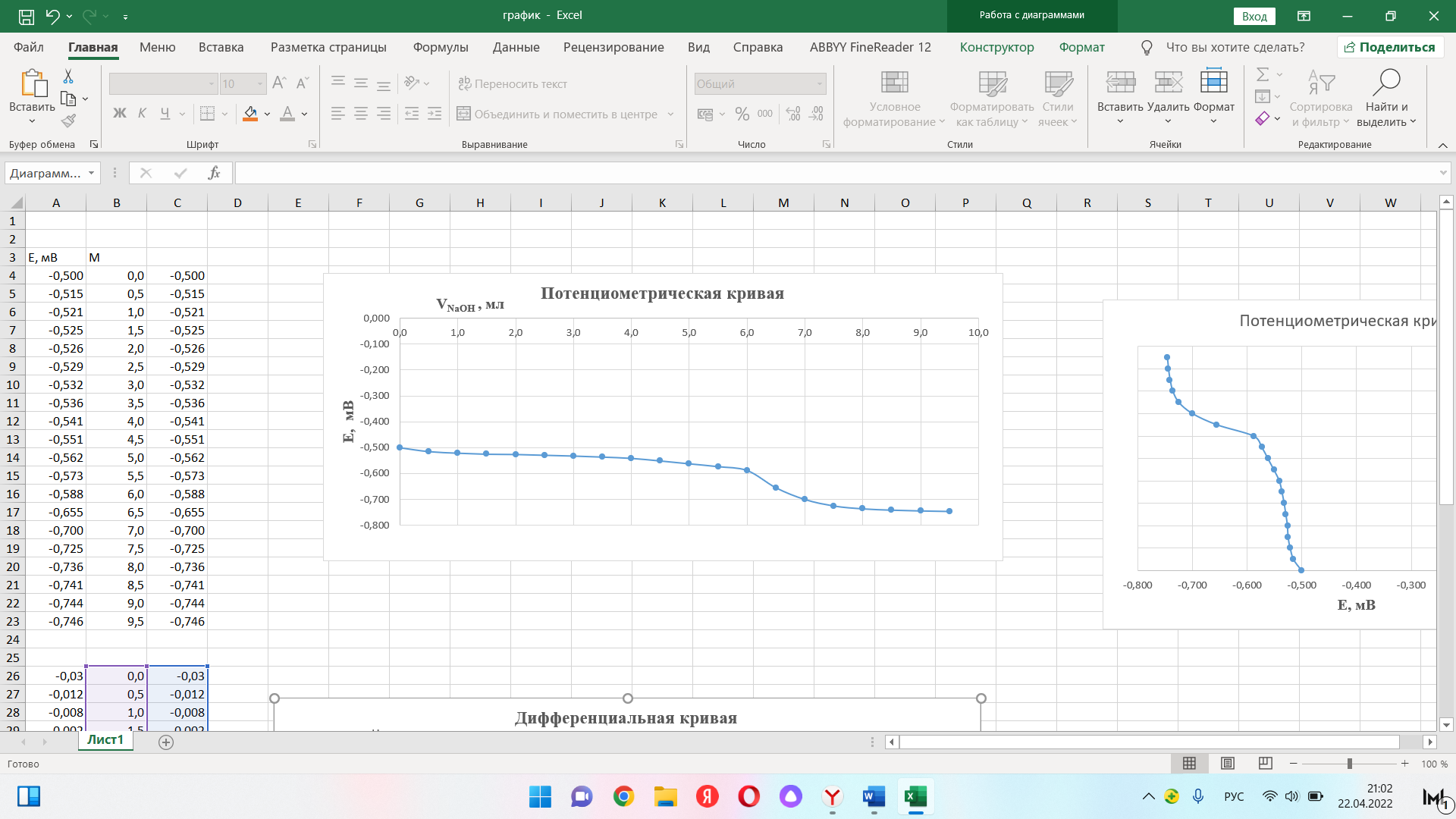 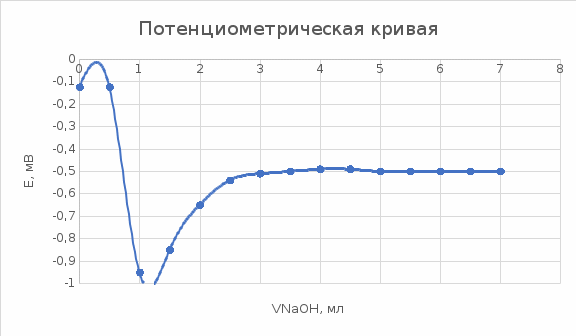 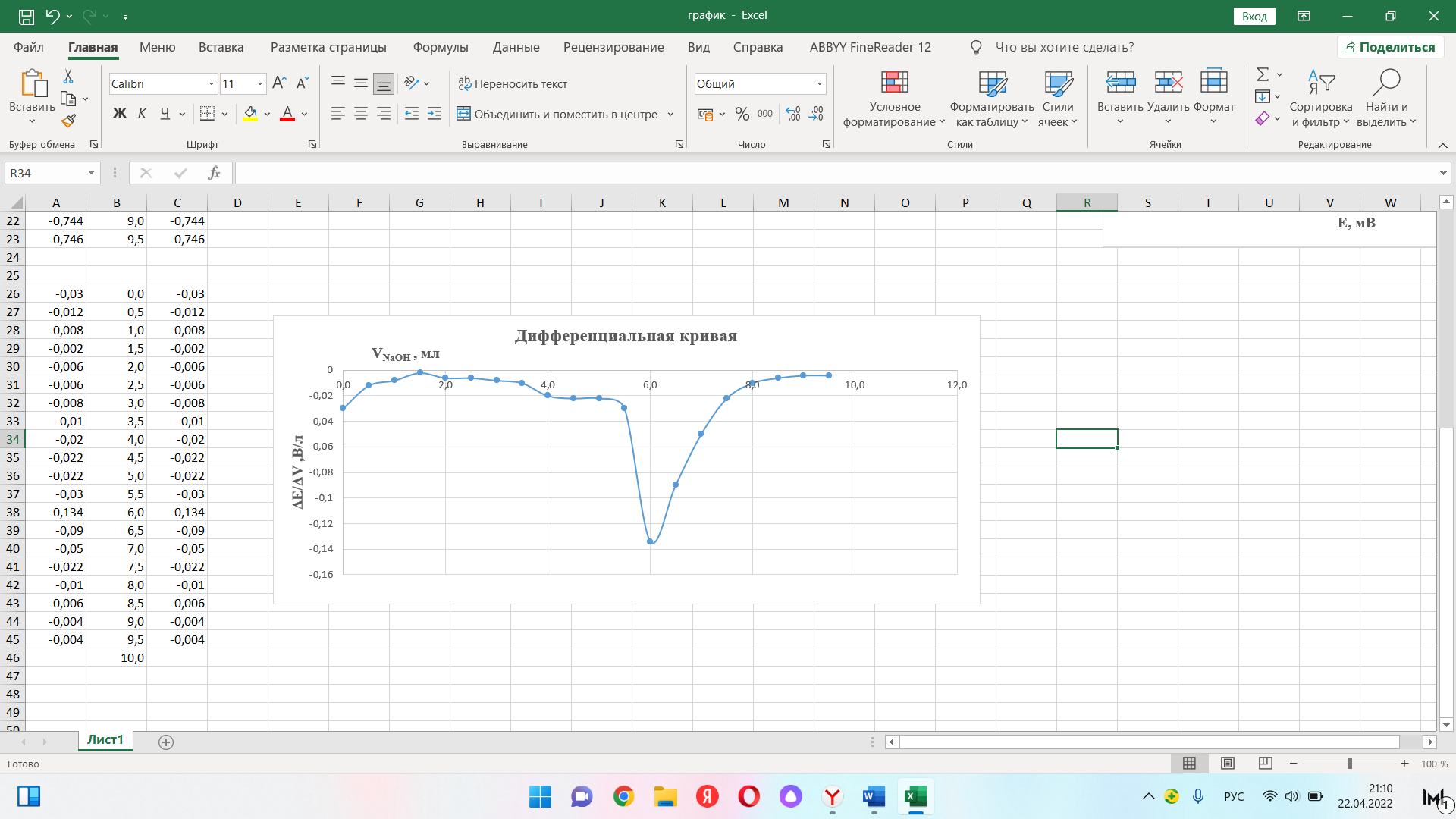 Определение кислотности: рассчитаем концентрацию кислоты по формуле 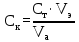 , ,где 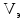 – объем NaOH в точке эквивалентности (мл), – объем NaOH в точке эквивалентности (мл), 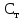 – концентрация NaOH (экв/л), – концентрация NaOH (экв/л), 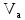 – объем пробы, взятой для анализа (мл) – объем пробы, взятой для анализа (мл)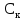 = = 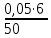 = 0,006 экв/л = 0,006 экв/лВывод: Согласно ГОСТ 32327-2013 «Нефтепродукты. Определение кислотного числа потенциометрическим титрованием», данная проба нефтепродукта является среднекислотной , и требуется дальнейшая ее переработка для изготовления качественного топлива. |

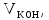 мл
мл