определение отношения теплоемкостей воздуха
 Скачать 119.47 Kb. Скачать 119.47 Kb.
|
|
Нижегородский государственный архитектурно-строительный университет Кафедра физики ОТЧЁТ по лабораторной работе № 7 (4): «ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ ВОЗДУХА» Преподаватель: Краснов А.А Студент гр. СУЗ.24: Кикоть Д.А \ 2022 ЦЕЛЬ РАБОТЫ Экспериментальное определение показателя адиабатического процесса 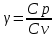 для для воздуха, где  , , 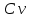 — соответственно молярные теплоемкости идеального газа при постоянном давлении P и постоянном объеме V. — соответственно молярные теплоемкости идеального газа при постоянном давлении P и постоянном объеме V.ЛАБОРАТОРНАЯ УСТАНОВКА И МЕТОД ИЗМЕРЕНИЯ Для измерения соотношения  изготовлена лабораторная установка (рис. 3), в которой в качестве рабочего тела используется воздух. изготовлена лабораторная установка (рис. 3), в которой в качестве рабочего тела используется воздух.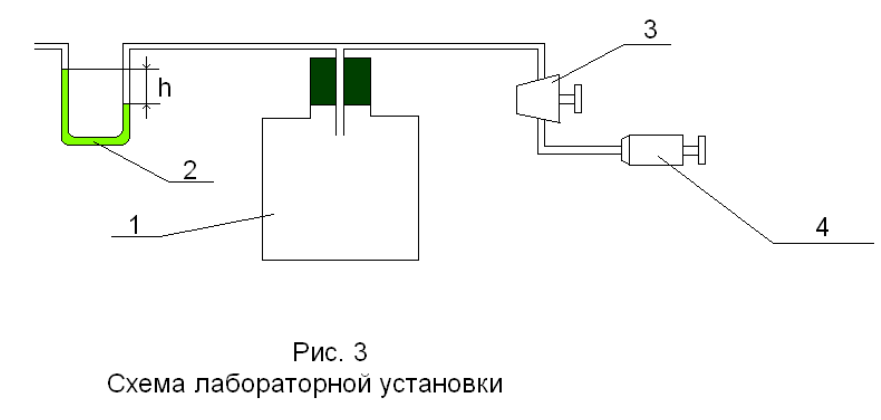 На рис. 3 показаны: 1 — сосуд, 2 — водяной манометр U-образной формы (для удобства измерений вода подкрашена), 3 — кран, соединяющий сосуд либо с атмосферой, либо с насосом, h — разности уровней водяного столба в манометре, 4 — насос. На этом рисунке показания манометра соответствуют давлению в сосуде P = Pатм + ρgh , ρ — плотность воды, g ≈ 10 м/c2 . В этой установке проводят два процесса: адиабатическое расширение, при котором воздух в установке охлаждается до T2 < Tатм, и изохорический процесс нагревания воздуха от T2 до Tатм . Соответственно на рис. 4 проведены на плоскости (P,V ) графики процессов, реализуемых в лабораторной установке. 1. Исходное состояние (точка (1) на рис. 4) с P1 > Pатм и T1 = Tср получают, предварительно накачав насосом воздух в сосуд до давления P1> Pатм . Для этого предварительно соединяют краном 3 сосуд 1 с насосом 4. Затем, после накачивания, закрывают. Когда показания манометра станут стабильными (газ остынет после нагрева и температура станет равной температуре среды, т. е. комнатной температуре: T1 = Tср ), измеряют давление P1 :  и записывают значение h1 разности высот в коленах манометра в таблицу. Рекомендованные значения h1 составляют 15 ÷ 20 сантиметров. 2. Открывают кран (3), сообщая сосуд с атмосферой. При этом часть воздуха выходит в атмосферу, и давление газа быстро выравнивается с атмосферным давлением Pатм (точка (а) на рис. 4). 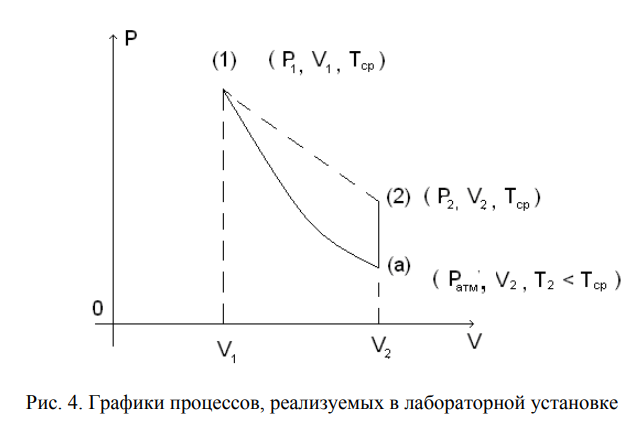 После этого кран закрывают (при показаниях манометра h ≈ 0 ). Оставшаяся часть воздуха массой m1 расширилась и заняла весь объем сосуда V2 =Vсосуда . В первом состоянии P1 > Pатм эта масса воздуха m1 занима  ла только часть объемаV1 ла только часть объемаV1  Здесь необходимо учитывать, что в точке (а) объем V2 =Vсосуда, а давление равно Pатм . В результате этого расширения воздух в сосуде охладится до некоторой температуры T2 3. Последний переход. Газ в сосуде нагревается при постоянном объеме до комнатной температуры Tср (точка (2) на рис. 4). Здесь давление P2 можно найти по показаниям манометра  Состояния «1» и «2» имеют одинаковые температуры T1 = T3 = Tср и, следовательно, из уравнения Менделеева-Клапейрона имеем:  Далее, состояния «1» и «а» связаны адиабатическим процессом, для которого выполняется формула (13). Введем для удобства записи обозначения   . При этом . При этом 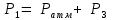 , , 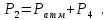 Подставляя (15) в (13) и логарифмируя, находим: Подставляя (15) в (13) и логарифмируя, находим: 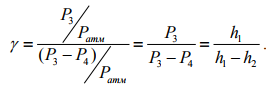 Следовательно, получаем расчётную формулу для  : : ТАБЛИЦА ИЗМЕРЯЕМЫХ И РАСЧЁТНЫХ ВЕЛИЧИН
ВЫПОЛНЕНИЕ РАСЧЁТОВ   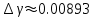 2) 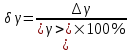  i- коэффициент свободы 3) 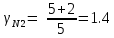    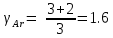 Вывод: Показатель адиабатного процесса считается приблизительно равным 1.4. Но в связи с погрешность вычислений и повышенной концентрацией CO2 и паров воды в воздухе экспериментально 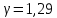 |
