лабораторная. Определение отношения теплоёмкости газа при постоянном давлении к теплоёмкости при постоянном объёме
 Скачать 76.93 Kb. Скачать 76.93 Kb.
|
 УГТУ-УПИ им. С. М. Кирова УГТУ-УПИ им. С. М. Кировакафедра физики Отчёт по лабораторной работе № 7 Определение отношения теплоёмкости газа при постоянном давлении к теплоёмкости при постоянном объёме. Студент: Дёмин Алексей Группа: Р-184 Дата: г. Екатеринбург 1997 Некоторые сведения из теории. Теплоемкостью тела называется физическая величина, числено равная количеству тепла, которое необходимо сообщить телу, чтобы повысить его температуру на 1 кельвин. Теплоемкость единицы массы называется удельной теплоемкостью, а теплоемкость одного моля вещества - молярной теплоемкостью. Таким образом, 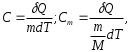 где C и Cm - удельная и молярная теплоемкости; где C и Cm - удельная и молярная теплоемкости;Q - количество тепла, сообщенного телу; dT - приращение температуры; m - масса тела; M - малярная масса. Величина теплоемкости вещества в общем случае зависит от условий нагревания и температуры. Выражение для молярной теплоемкости идеального газа при постоянном давлении имеет вид: 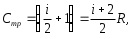 где i - число степеней свободы молекул газа; где i - число степеней свободы молекул газа;R - универсальная газовая постоянная. Молярная теплоемкость равна 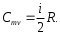 Из выражений следует, что отношение теплоемкости Cmp к теплоемкости Cmv равно Из выражений следует, что отношение теплоемкости Cmp к теплоемкости Cmv равно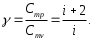 Величину называют коэффициентом Пуассона или показателем адиабаты. Целью настоящей работы является определение воздуха весьма простым экспериментальным методом Клемана-Дезорма. Метод Клемана-Дезорма. 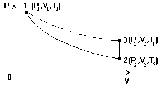 Рис. A Метод Клемана-Дезорма по определению базируется на измерении давления газа, заключенного в одном и том же сосуде и последовательно проходящего через три состояния: из первого во второй газ переходит адиабатически, из второго в третье - изохорически (рис. 1). Расчетная формула для определения имеет вид: 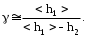 где h2 – разность высот столбов жидкости в водяном манометре, определяемая экстараполяйией опытных значений для времени =0 по графику. Работа при адиабатическом процессе. В данной работе также определяется работа при адиабатическом расширении газа на участке кривой 1-2 (рис. 1). Адиабатическим называется процесс, происходящий баз теплообмена с окружающей средой. Расчетная формула работы при адиабатическом расширении газа в рассматриваемом случае имеет вид: 1 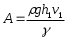 где V1 - первоначальный объем газа, который хотя и меньше объема баллона V2, но на небольшую величину. Поэтому при расчете работы за величину V1 принимают объем баллона. Величина - плотность жидкости (воды) в манометре. 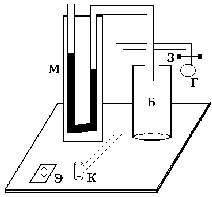 Рис. B Описание установки. Порядок выполнения работы. Установка (рис. 2) состоит из стеклянного баллона Б, U-образного манометра М, резиновой груши Г с зажимом Мора З и электроклапана К, который позволяет одновременно соединить баллон с атмосферой и электросекундомером. Одно колено жидкостного (водяного) U-образного манометра открыто, а другое соединено с баллоном, поэтому, когда баллон соединен с атмосферой, уровни жидкости в обоих коленах одинаковы. Резиновая груша служит для нагнетания воздуха в баллон. Порядок выполнения работы 1. Прежде всего, необходимо проверить, нет ли утечки воздуха из баллона. Для этого с помощью резиновой груши медленно нагнетают в баллон воздух до давления больше атмосферного. Давление измеряется по разности уровней в коленах манометра. Так как при этом воздух в баллоне несколько нагревается, то следует подождать 5-6 минут, пока установится тепловое равновесие. После этого, если показания манометра не изменяются (нет утечки воздуха), записывают значение h1, соответствующее состоянию 1. 2. Затем нажимают клапан К, соединяя баллон с атмосферой; воздух при этом выходит из баллона со слабым свистом, и как только он прекратится, клапан закрывают. Предполагается, что этот процесс соответствует адиабате 1-2 на рис. 1. Давление воздуха в баллоне к моменту закрытия клапана (состояние 2) равно внешнему атмосферному. Через некоторое время после закрытия клапана газ по изохоре перейдет в состояние 3 и, казалось бы, изменив состояние h2 по манометру, можно по формуле рассчитать . Однако описанный способ является довольно грубым, что сказывается на точности определения . На самом деле это не так. Поэтому, учитывая неадиабатичность и, главное, неравновесность процесса между состояниями 1 и 2, мы получаем не значение h2, которое необходимо для расчета , а некоторое другое значение h’2; при этом значение h’2 будет тем меньше, чем больше время , в течение которого из баллона выпускается воздух. В предельном случае при большой выдержке температуры вне и внутри баллона могут сравняться; и после закрытия клапана давление в баллоне не изменится, то есть h’2 будет равно 0. Установлено, что между h2 и h’2 достаточно хорошо выполняется следующая зависимость: 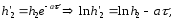 где a - константа, зависящая от параметров установки и условий опыта; - время, в течение которого выпускается из баллона воздух (открыт клапан). 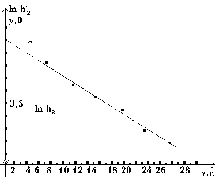 Рис. 3 Эта формула позволяет по экспериментальным значениям h’2, полученным из опыта, определить h2, а затем и более точно рассчитать . На рис. 3 представлен график зависимости, из которого видно, что, повторив опыт несколько раз, (при одной и той же величине h1) с различным временем, можно путем экстраполяции определить h2. Таким образом, второй этап опыта (пункт 2) следует проверить в следующем порядке: а) соединить баллон при помощи клапана К (на клапан нажимать резко и до упора) с атмосферой на 5 секунд, после чего клапан закрыть. Время определяется по секундомеру; б) выждать, пока давление перестанет меняться (2-3 минуты), и сделать отсчет разности уровней манометра h’2; в) операции а) и б) повторить со временем соединения баллона с атмосферой: 5, 9, 13, 17, 21, 25 с. При этом максимальное время должно быть выбрано так, чтобы соответствующая ему разность уровней h’2 была значительно больше погрешности манометра. Необходимо следить за тем, чтобы начальное превышение давления h1 в баллоне перед открытием клапана в каждом опыте было одно и то же. C этой целью исходное давление достигается осторожным нагнетанием воздуха в баллон грушей Г до тех пор, пока в манометре уровень жидкости не достигнет красной метки. Вычисление работы адиабатического расширения воздуха. Работа газа вычисляется по формуле (1). Значение показателя адиабаты * берется из эксперимента. Все величины, входящие в формулу (1) нужно выразить в СИ. Средства измерений и их характеристики.
Установка №1 Объем баллона V=19.5 дм3, V=0.3 дм3. воды=1000 кг/м3, g=9,81 м/с2. Результаты измерений.
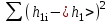 = 669.5 мм2 вод. ст.. = 669.5 мм2 вод. ст..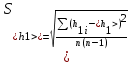 =4.724 мм вод. ст.. tp,n=2.57 =4.724 мм вод. ст.. tp,n=2.57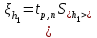 =12.14 мм вод. ст.. =12.14 мм вод. ст..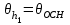 =1 мм вод. ст. =1 мм вод. ст.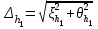 =12.18 мм вод. ст. =12.18 мм вод. ст.По графику находим ln h2=4.06 ,тогда h2=57.97 мм вод. ст. 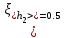 мм вод. ст. мм вод. ст.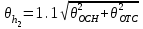 =1.2 мм вод. ст. =1.2 мм вод. ст.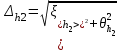 =1.3 мм вод. ст. =1.3 мм вод. ст.Расчет искомых величин. 1. Расчет коэффициента Пуассона 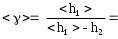 1.346 1.3462. Расчет работы при адиабатическом расширении газа 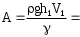 32.048 Дж. 32.048 Дж.Расчет границы относительной погрешности результата измерения показателя адиабаты (коэффициент Пуассона). 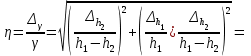 0.31 0.31Расчет границы абсолютной погрешности результата измерения коэффициента Пуассона. 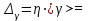 0.42 0.42Окончательный результат. 1. Коэффициент Пуассона воздуха равен =<>=1.30.4 2. Работа при адиабатическом расширении воздуха равна A= 32.048 Дж Выводы. В данной лабораторной работе я определил отношение теплоёмкости газа при постоянном давлении к теплоёмкости при постоянном объёме - коэффициент Пуассона воздуха и получил его равным 1.30.4 . Это значение, в пределах погрешности, вполне соответствует теоретическому значению. Также в своей работе я рассчитал работу при адиабатическом расширении воздуха. Её численное значение 32.048 Дж, что также входит в рамки разумного значения при данных условиях эксперимента. |
