Пр.8 Физика 1 курс. пр 8. Определение заряда электрона. Электролиз
 Скачать 144.04 Kb. Скачать 144.04 Kb.
|
|
Практическое занятие № 8 Тема : Определение заряда электрона. Электролиз. Цель работы: научиться определять заряд электрона экспериментальным путем. Оборудование: электролитическая ванна с раствором медного купороса, выпрямитель, амперметр, реостат, ключ, весы с разновесами, секундомер, сушильный шкаф, соединительные провода. Теория Пропуская электрический ток через раствор электролита, например CuSO4 , происходит выделение вещества на электроды. Такое явление называется электролиз. Итак, пронаблюдаем процессы которые происходят при электролизе. Диссоциация молекул сульфата меди в водном растворе протекает по следующей схеме CuSO4  4 Cu2SO2 Нейтрализовавшиеся атомы меди отлагаются в виде твердого осадка на катоде. Пройдя через электролит, масса вещества, выделившиеся на электроде, прямо пропорциональна общему заряду. В 1832 году Майкл Фарадей* открыл эту закономерность. k neNa mkIt, где электрохимический эквивалент вещества, постоянная величина равная отношению массы иона к его заряду, где n- валентность вещества, его молярная масса. Молярная масса меди 63,5103 кг/моль. Вследствие этого, закон Фарадея будет таким: m neNa It. При помощи этого закона (закон Фарадея) вычисляется заряд электрона. Числом Фарадея назвали произведение заряда электрона на число Авогадро Na. Электрический заряд, переносимый в количестве 1 моль при e _ It. mnNa Описание экспериментальной установки  – амперметр, – электронный блок управления с секундомером, – блок с начальными параметрами электролиза, – выпрямитель В-24м – электролитическая ванна с раствором медного купороса, – электронные весы, – блок с набором электродов: медь, никель, кобальт, железо, хром, – электроды Ход работы Запустить виртуальную лабораторную установку. Если необходимо, то обнулите данные. С помощью курсора, перенести медный электрод на весы и взвесить их. Изучить собранную цепь, которая соединяет последовательно батарею, амперметр, реостат, сосуд с раствором сульфата меди (медного купороса), ключ, по рисунку 1. За 15 минут, нужно сделать электролиз медного купороса. С помощью реостата, поддерживать силу тока 1 А неизменной. Выключите ток, выньте и обсушите электроды над электрической плиткой. 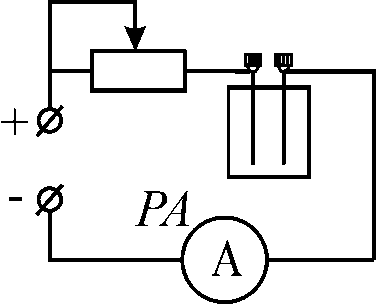 Рис. 1 Еще раз взвесить электроды. Узнать массу вещества, выделившегося на катоде ( mm2 m1 ). Таблица1
Благодаря полученным данным из опыта, вычислить, заряд электрона, число Фарадея и электрохимический эквивалент меди. Рассчитать погрешности измерения заряда e: Максимальные относительная и абсолютная погрешности измерения заряда электрона определяются по формулам: εе = 2Δm/m2 -m1 +ΔI / I + Δt / t Δe = eэксп * εе
Ответить на вопросы _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ В чем заключается существенное отличие проводимости электролитов от проводимости металлических проводников _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Сформулируйте законы электролиза. __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Можно ли определить электрохимический эквивалент, если через ванну пропускать переменный ток __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ |
