Курсовая по ОНХ, 1 курс. Определить стандартную энтропию кристаллического бромида франция при 298,15к s
 Скачать 118.15 Kb. Скачать 118.15 Kb.
|
|
Задание №467. Определить стандартную энтропию кристаллического бромида франция при 298,15К S˚298 (FrBr(к)), используя вышеприведенные данные для задания 466.
I способ. Метода наименьших квадратов (МНК). Этот метод заключается в определении коэффициентов уравнения линейной зависимости y=ax+b. Для расчета a и b воспользуемся формулами для математического ожидания величины x - mx, математического ожидания величины y – my, корреляционного момента - Kxy и дисперсии величины y– Dx:  Коэффициенты a и b находятся по формулам: 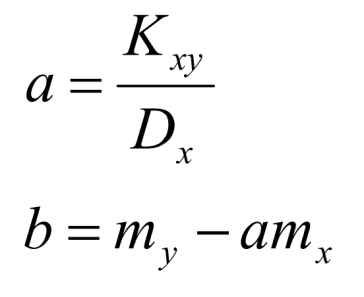 Для нахождения искомой величины нужно провести экстраполяцию известных значений. Чтобы это сделать, нужно найти коэффициенты a и b в уравнении вида: S˚298(FrBr(к)) = a * S˚298(FrI(к)) + b; Используя формулы, найдем: mx = (18,0 + 22,6 + 25,3 + 29,4)/4 = 23,825; my = (16,7 + 20,6 + 23,1 + 26,3)/4 = 21,675; Kxy = ((18,0 – 23,825)*(16,7 – 21,675) + (22,6 – 23,825)*(20,6 – 21,675) + (25,3 – 23,825)*(23,1 – 21,675) + (29,4 – 23,825)*(26,3 – 21,675))/4 = 14,5456; Dx = ((18,0 – 23,825)2 + (22,6 – 23,825)2 + (25,3 – 23,825)2 + (29,4 – 23,825)2)/4 = 17,1719; Зная корреляционный момент и дисперсию величины y, найдем коэффициенты a и b: a = 14,5456/17,1719 = 0,8471; b = 21,675 – 0,8471 * 23,825 = 1,4928; Подставив полученные коэффициенты в уравнение S˚298(FrBr(к)) = a * S˚298(FrI(к)) + b, получим: S˚298(FrBr(к)) = 0,8471 * 33,1 + 1,4928 = 29,5 кал/(моль*К); Ответ: S˚298(FrBr(к)) = 29,5 кал/(моль*К). II способ. Данный способ подразумевает использование функций программы Excel. Она позволяет путем построения графика по известным величинам установить усредняющую линию тренда и вывести ее уравнение. Подставив значение аргумента (или функции), можно найти неизвестную величину. Задав значения энтропии бромидов щелочных металлов (y) и значения энтропии йодидов щелочных металлов (х), получим такой график: 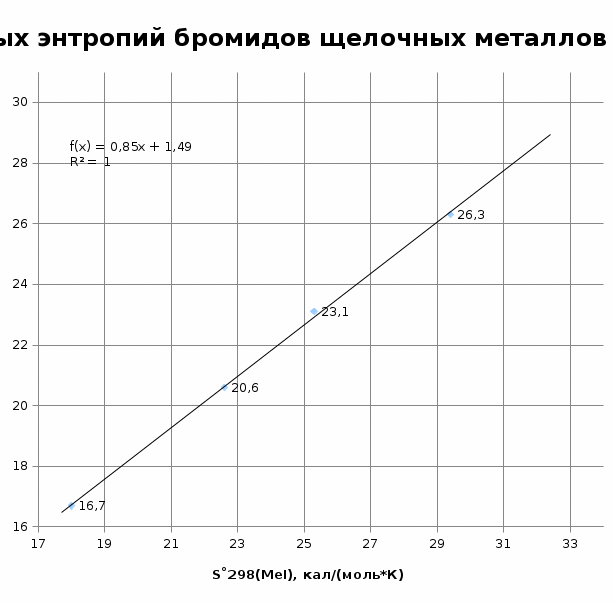 В итоге имеем уравнение линии тренда: y = 0,8471 · x + 1,4938; где y – S˚298(FrBr(к)), а x - S˚298(FrI(к)). Подставив значения в полученное уравнение, найдем: S˚298(FrBr(к)) = 0,8471 * 33,1 + 1,4938 = 29,5 кал/(моль*К). Ответ: S˚298(FrBr(к)) = 29,5 кал/(моль*К). Вывод: I способ – S˚298(FrBr(к)) = 29,5 кал/(моль*К). II способ – S˚298(FrBr(к)) = 29,5 кал/(моль*К). Результаты обоих исследований практически не различаются, что говорит о эффективности методов сравнительных расчетов Михаила Христофоровича Карапетьянца. Методы расчета М. Х. Карапетьянца позволяют установить одну и ту же величину различными способами (в нашем случае – методом наименьших квадратов (I способ), нахождением уравнения линии тренда в Excel (II способ)) и построении линии тренда на миллиметровой бумаге (III способ) и сравнить полученные результаты. В итоге, используя различные методы расчета, мы получили одну и ту же величину, и все значения оказались примерно равны. Это говорит о действенности и большом значении методов сравнительного расчета Михаила Христофоровича Карапетьянца в современных исследованиях химических свойств веществ и элементов и во всей науке в целом. |
