спирты задачи. Правильные ответы показаны на (слайде 3)!!!
 Скачать 333.24 Kb. Скачать 333.24 Kb.
|
|
1. Относительная плотность паров предельного одноатомного спирта Правильные ответы показаны на (слайде 3)!!!
по кислороду равна 2,75. Выведите молекулярную формулу спирта.  2. Предельный простой эфир массой 10 г при нормальных условиях занимает объем 4.87 л. Выведите молекулярную формулу эфира.  3. Относительная плотность паров органического соединения по воздуху равна 2,552. Массовая доля углерода в этом веществе равна 64,86%, массовая доля водорода равна 13,51%, массовая доля кислорода равна 21,63%. Выведите молекулярную формулу этого вещества.  4. Относительная плотность паров органического соединения по водороду равна 65. Массовая доля углерода в этом веществе равна 73,85%, массовая доля водорода равна 13,85%, массовая доля кислорода равна 12,3%. Выведите молекулярную формулу этого вещества.  5. Относительная плотность паров органического соединения по водороду равна 51. При сжигании 30,6 г этого вещества образовалось 79,2 г диоксида углерода и 37,8 г воды. Выведите молекулярную формулу органического соединения.  6. Относительная плотность паров органического соединения по кислороду равна 3,625.11ри сжигании 29 г этого вещества образуется 39,2 л углекислого газа (н. у.) и 36 г воды. Выведите молекулярную формулу органического соединения.  Задача: При действии избытка натрия на раствор фенола в метаноле выделилось 1176 мл газа (н. у.). Для нейтрализации такого же количества раствора потребовалось 10 мл водного раствора NaОН с концентрацией 20 мг/мл. Чему равна массовая доля фенола в исходном растворе? Решение: Для начала давайте распишем все химические процессы в задаче: 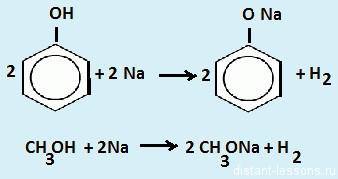 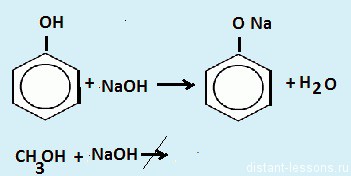 1. Во второй реакции проявляется то самое различие между спиртами и фенолами — из второй реакции, в которой метанол не взаимодействует с щелочью, мы можем найти количество моль фенола, 2. в условии сказано, что такое же количество прореагировало с Na в первой реакции — в этой реакции и спирт и фенол реагируют с Na одинаково. 3. Значит, мы можем найти то количество водорода (газ), которое соответствует фенолу, 4. найти остаток водорода и вычислить количество моль метанола. В вопросе сказано найти массовую долю фенола, значит, используем стандартную формулу для массовой доли вещества в растворе Давайте напишем подробное решение: 1. Дано 10 мл водного раствора NaОН с концентрацией 20 мг/мл. Значит, находим количество моль: n (NaOH) = m\Mr=V*C(концентрация)\Mr = 10 (мл) * 0,020( г\мл) \40 (г\моль) \= 0,005 моль Значит, по уравнению реакции, n(фенола) = 0,005 моль 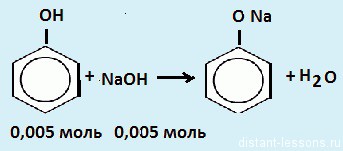 2. Значит, количество фенола, вступившего в первую реакцию тоже 0,05 моль 3. Водорода по уравнению реакции получается в 2 раза меньше, чем фенола: 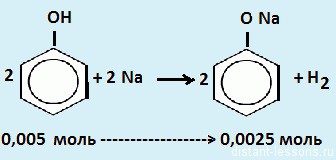 4. При действии избытка натрия на раствор фенола в метаноле выделилось 1176 мл газа (н. у.). Нам нужно найти количество моль водорода. n(H2)=V\22,4 (л\моль) = 1.176 (л)\ 22.4 (л\моль) = 0.0525 моль Значит, в реакции с метанолом выделилось 0.0525 — 0.0025 = 0,05 моль водорода n (метанола) = 0.1 моль 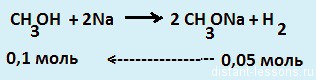 Находим массовую долю: m(фенола) = 0,05 (моль)*94 (г\моль) = 0,47 г m(метанола) = 0,1 (моль) * 32 (г\моль) = 3,2 г w(фенола) = m(фенола) \ (m(фенола) + m(метанола) )*100%= 0,47 (г)\ 3,67 (г)*100% = 12,8% | ||||||||||||||||||||||
