Биохимия. ВОТ КОНСПЕКТ АНДРЮША СТАВЬ 7. Происходит двумя путями
 Скачать 2.24 Mb. Скачать 2.24 Mb.
|
|
1. На какие группы подразделяются организмы в зависимости от вида потребляемой энергии. Общая схема использования органических веществ в качестве источника энергии в организме человека и высших животных.  2. Процессы в живом организме, требующие затраты энергии (не менее 5). Объясните понятия: электроны – носители энергии; органические вещества – консервы солнечной энергии. Какой компонент пищи – главный источник энергии для человека?  3. Биологическое окисление – ферментативный каталитический процесс: дегидрирование, прямое окисление. Энергетически сопряженные процессы: фотосинтез и биологическое окисление. Биологическое окисление – это совокупность окислительно-восстановительных реакций веществ в живых организмах. Происходит двумя путями: 1) дегидрированием – это окисление с образованием восстановленный форм НАД и ФАД (НАДН+Н, ФАД2Н) при этом от субстрата отщепляется 2 протона водорода и 2 электрона: -в случае с НАД он принимает 2 электрона, 1 протон, а второй протон идет в среду, из-за чего пишется НАДН+Н -ФАД получает 2 электрона и 2 протона, записывается ФАД2Н дальнейший путь электронов – ЭТЦ Пример реакции с НАД: 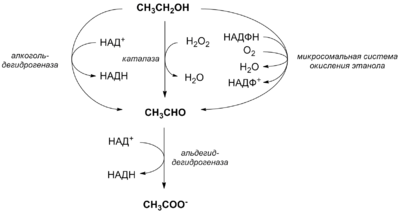 пример реакции с ФАД: 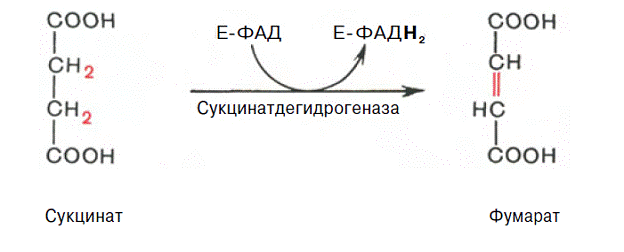 Дальнейшее окисление идет 2 путями: -в аэробных условиях – образуется вода в ЭТЦ -в анаэробных – из пирувата образуется лактат 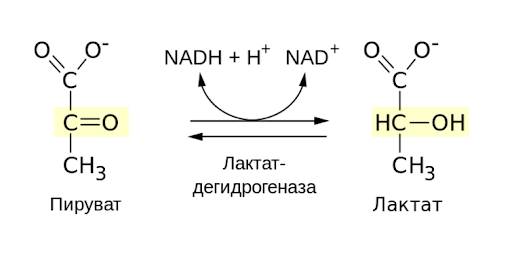 2) второй путь – это прямое окисление в этом случае от вещества напрямую отщепляются электроны и протоны пример – окисление ФАД2Н (ТУТ СПРАВА НАЛЕВО) 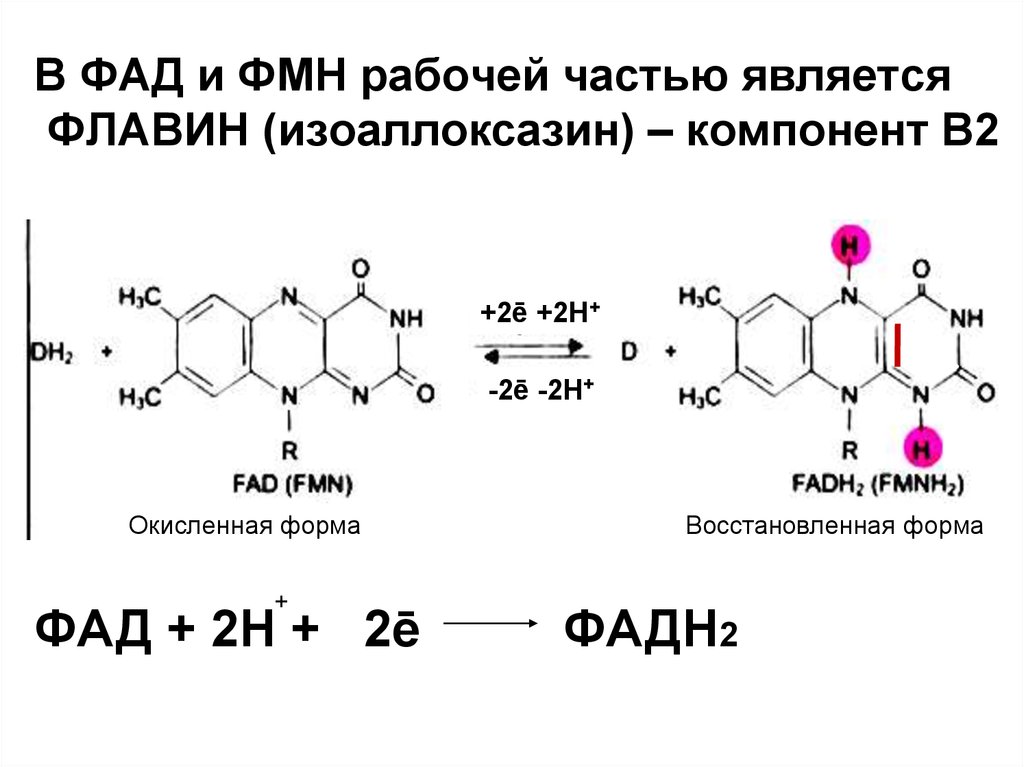 4. Локализация процессов окисления в клетке: процессы в цитоплазме и субклеточных структурах, коферменты дегидрогеназ (примеры, формулы) Примеры процессов в цитоплазме: Глицеральдегидфосфатная реакция – одна из реакций гликолиза: 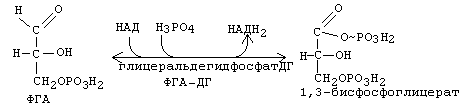 Образование фосфоенолпирувата: 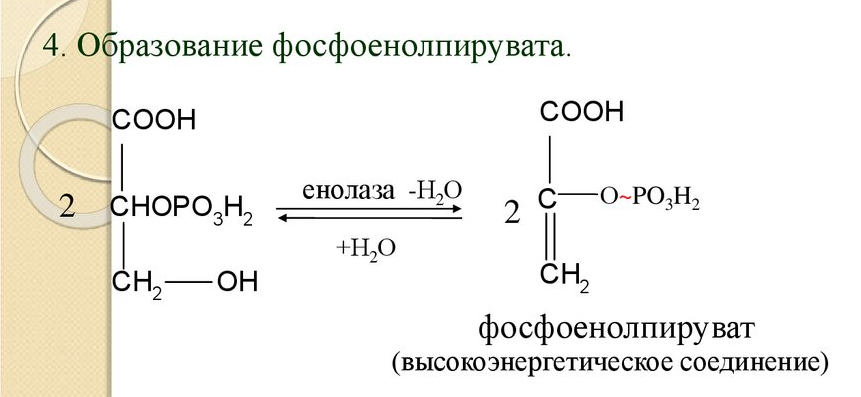 В митохондриях – цикл Кребса: -дегидрирование сукцината 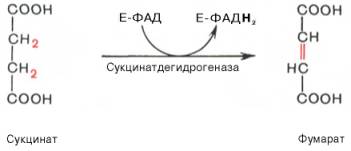 -дегидрирование малата 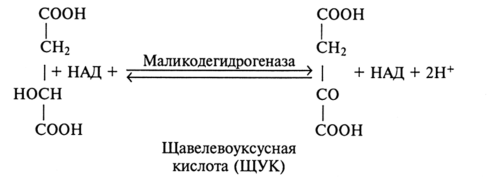 в пероксисомах – альфа-окисление жирных кислот  Коферменты дегидрогеназ: НАД 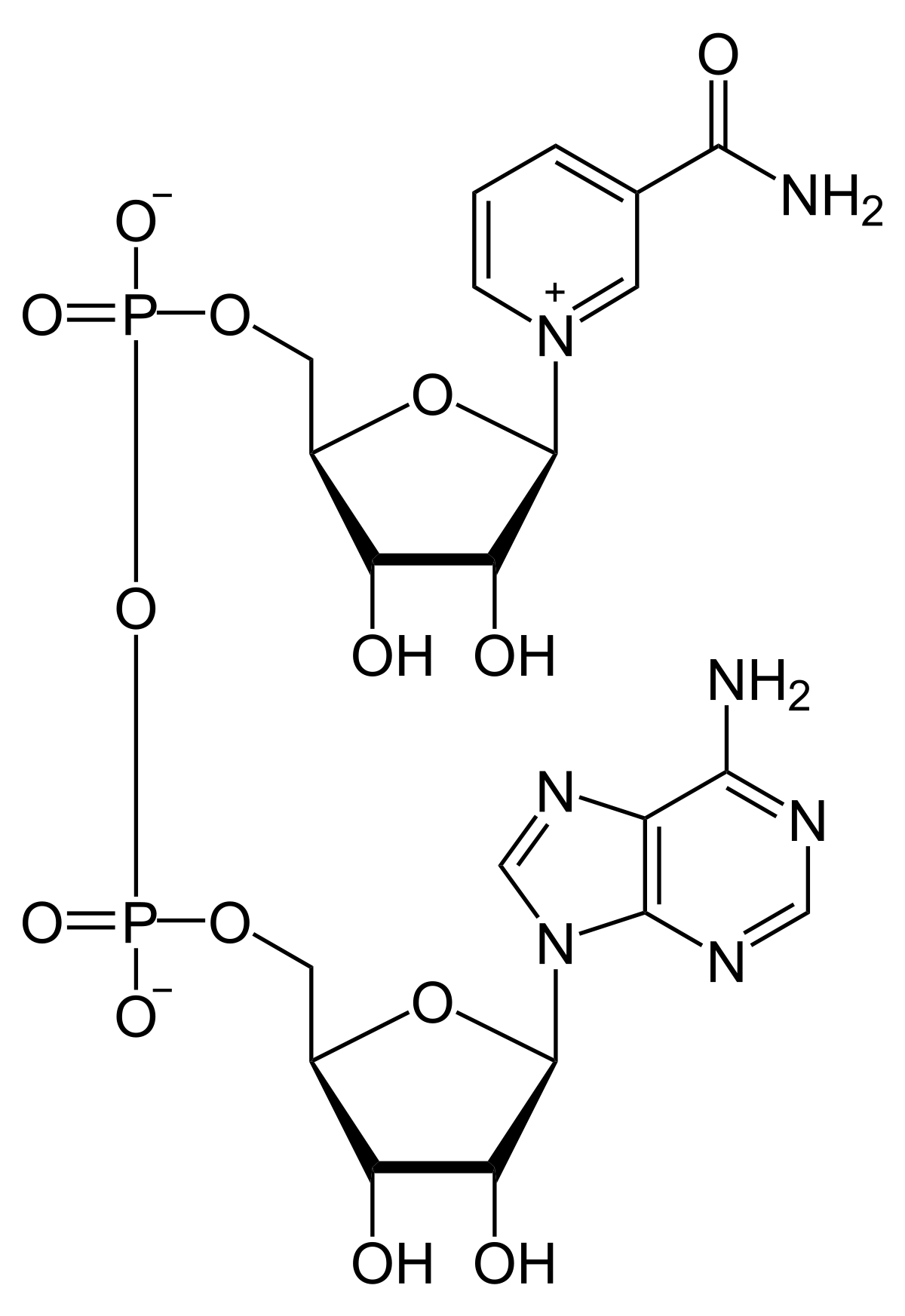 ФАД 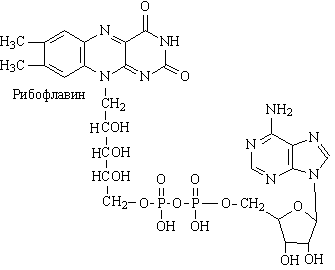 5. Общая схема обмена веществ на примере крахмала: синтез, гидролиз, окисление. Понятия анаболизма и катаболизма. При переваривании углеводов в желудочно—кишечном тракте происходит ферментативный гидролиз гликозидных связей и образование моносахаридов, главным из которых является глюкоза. Этапы углеводного обмена (в общем): Расщепление в пищеварительном тракте поступающих с пищей поли- и дисахаридов до моносахаридов, дальнейшее всасывание моносахаридов из кишечника в кровь. Синтез и распад гликогена в тканях, прежде всего в печени. Гликолиз — распад глюкозы. В настоящее время понятие «гликолиз» используется для описания распада глюкозы, проходящего через образование глюкозо-6-фосфата, фруктозо-1,6-дифосфата и пирувата как в отсутствие, так и в присутствии кислорода. В последнем случае употребляется термин «аэробный гликолиз», завершающегося образованием молочной кислоты или лактата. Анаэробный путь прямого окисления глюкозы или, как его называют, пентозофосфатный путь (пентозный цикл). Взаимопревращение гексоз. Анаэробный метаболизм пирувата. Этот процесс выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза — пирувата. Глюконеогенез — образование углеводов из неуглеводных продуктов (пирувата, лактата, глицерина, аминокислот, липидов, белков и т. д.). Под действием собственных ферментов человека крахмал гидролизуется до глюкозы, которая окисляется в клетках до углекислого газа и воды с выделением энергии, необходимой для функционирования живого организма. Гидролиз крахмала начинается в полости рта при участии амилазы слюны, которая частично расщепляет внутренние a —1,4—гликозидные связи, образуя менее крупные, чем крахмал молекулы — декстрины. Далее гидролиз крахмала продолжается в верхнем отделе кишечника под действием панкреатической амилазы, также расщепляющей a —1,4—гликозидные связи. В результате из крахмала образуются дисахаридные остатки мальтозы и изомальтозы (глк—( a —1,6)—глк). Гидролиз всех дисахаридов происходит на поверхности клеток кишечника и катализируется специфическими ферментами: сахаразой, лактазой, мальтазой и изомальтазой. Эти гликозидазы синтезируются в клетках кишечника.  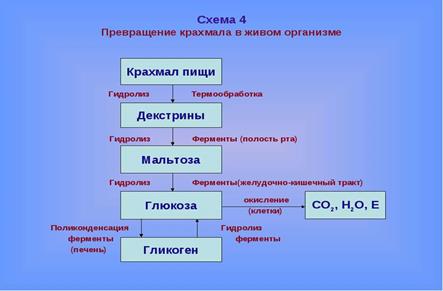 Уравнения (надеюсь это нам никогда не понадобится, но вот):  В сокращенном виде: 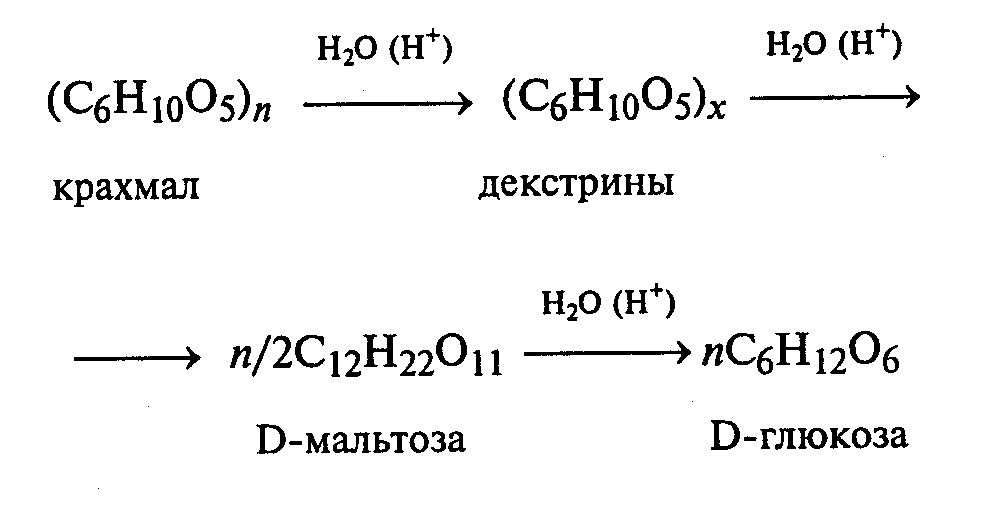 Биосинтез крахмала начинается с глюкозо-6-фосфата. Донором глюкозы служит сахароза. 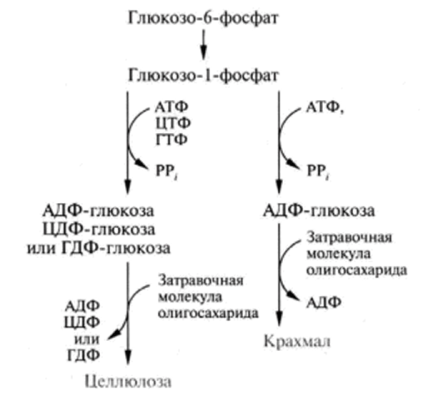 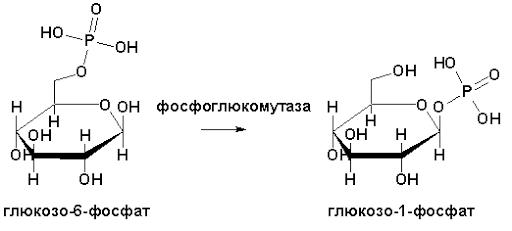 Анаболизм – это биосинтез белков, полисахаридов, липидов, нуклеиновых кислот и других макромолекул из малых молекул-предшественников. Поскольку он сопровождается усложнением структуры, то требует затрат энергии. Источником такой энергии является энергия АТФ. Также для биосинтеза некоторых веществ (жирные кислоты, холестерол) требуются богатые энергией атомы водорода – их источником является НАДФН. Молекулы НАДФН образуются в реакциях окисления глюкозо-6-фосфата и оксалоацетата. В реакциях анаболизма НАДФН передает свои атомы водорода на синтетические реакции и окисляется до НАДФ. Так формируется НАДФ-НАДФН-цикл. Катаболизм – расщепление и окисление сложных органических молекул до более простых конечных продуктов. Оно сопровождается высвобождением энергии, заключенной в сложной структуре веществ. Большая часть высвобожденной энергии рассеивается в виде тепла. Меньшая часть этой энергии "перехватывается" коферментами окислительных реакций НАД и ФАД, некоторая часть сразу используется для синтеза АТФ. 6. Этапы катаболизма, общая схема. Представление о частных и общих путях катаболизма. Примеры. 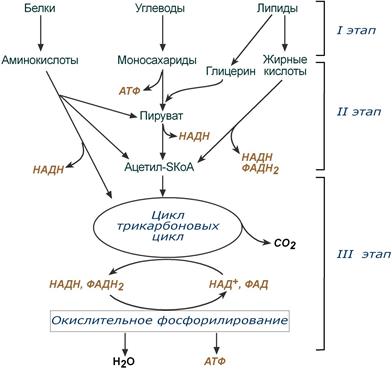 Весь катаболизм условно подразделяется на три этапа, включающие реакции общих и специфических путей. Первый этап Происходит в кишечнике (переваривание пищи) или в лизосомах (самообновление клеток) при расщеплении уже ненужных или лишних молекул. При этом освобождается около 1% энергии, заключенной в молекуле. Она рассеивается в виде тепла. Второй этап Вещества, образованные при внутриклеточном гидролизе или проникающие в клетку из крови, на втором этапе обычно превращаются: в пировиноградную кислоту (моносахариды в гликолизе), в ацетил-SKoA, в пируват и другие кетокислоты (в катаболизме аминокислот), в ацетил-SКоА (при β-окислении жирных кислот). Локализация второго этапа – цитозоль и митохондрии. На этом этапе выделяется около 30% энергии, заключенной в молекуле, и при этом запасается около 13% от всей энергии вещества (или примерно 43% от выделенной на этом этапе энергии). Под специфичными путями катаболизма понимают реакции, осуществляемые специфичными ферментами в специфичных, для разных классов веществ, реакциях 1 и 2 этапов. После того, как эти процессы закончатся, образуются пируват и ацетил-SКоА (в основном) и начинаются общие пути превращений. Подразумевается, что независимо от источника происхождения пирувата и ацетил-SKoA (из аминокислот, жирных кислот или моносахаридов) они попадают в общий путь катаболизма – 3 этап биологического окисления. Третий этап Все реакции этого этапа идут в митохондриях. Ацетил-SКоА (и кетокислоты) включается в реакции цикла трикарбоновых кислот, где углероды веществ окисляются до углекислого газа. Выделенные атомы водорода соединяются с НАД и ФАД, восстанавливают их и после этого НАДН и ФАДН2 переносят водород в цепь ферментов дыхательной цепи, расположенную на внутренней мембране митохондрий. Сюда же отдают свои атомы водорода молекулы НАДН и ФАДН2, образованные на втором этапе (гликолиз, окисление жирных кислот и аминокислот). В третьем этапе выделяется до 70% всей энергии вещества. Из этого количества усваивается почти две трети (66%), что составляет около 46% от общей. Таким образом, из 100% энергии окисляемой молекулы клетка запасает больше половины – 59%. На внутренней мембране митохондрий в результате процесса под названием "окислительное фосфорилирование" образуется вода и главный продукт биологического окисления – АТФ. 1-ая и 2-ая стадии катаболизма относятся к специфическим (частным) путям, которые уникальны для метаболизма белков, липидов и углеводов. Примеры: гликолиз (2 этап окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты); β-окисление жирных кислот: 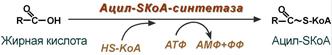 ; катаболизм аминокислот. ; катаболизм аминокислот.Заключительный этап катаболизма, сводится к окислению ацетил-КоА до СО2 и Н2О в реакциях цикла трикарбоновых кислот (цикла Кребса) – общий путь катаболизма. 7. Макроэргические молекулы (макроэрги) — биологические молекулы, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги — чаще всего ангидриды фосфорной и карбоновых кислот, а также слабых кислот, какими являются тиолы и енолы. Примеры: АТФ, ГДФ (Гуанозиндифосфат ), ацетил-КоА, сукцинил-КоА, креатинфосфат, 1,3-бисфосфоглицерат. Аденилатная система клетки. В энергообмене клеток всех типов центральная роль принадлежит аденилатной системе, которая включает трифосфат (АТФ), дифосфат (АДФ) и 5-моно-фосфат (АМФ) аденозина, а также неорганический фосфат (Pi) и ионы магния (Mg). Аденозинтрифосфат — термодинамически неустойчивая молекула, гидролизуется с образованием АДФ или АМФ. Неустойчивость молекулы АТФ обладает высоким потенциалом переноса, что позволяет АТФ выполнять функцию переносчика химической энергии, необходимой для удовлетворения большей части энергетических потребностей клеток. В молекуле АТФ фосфоангидридная (пирофосфатная) связь образуется путем соединения АДФ и неорганического фосфата в ходе ряда специфических реакций фосфорилирования. Эти реакции, протекающие в мембранах хлоропластов, митохондрий и бактерий, сопровождаются потреблением кислорода. Превращение АМФ в АДФ происходит путем переноса концевой фосфорильной группы с АТФ на АМФ. Эта реакция катализируется весьма активным ферментом аденилаткиназой, присутствующим во всех клетках. Ниже приводится схема превращения молекулы АМФ в молекулу АТФ (по Д. Мецлеру):  8. АТФ- аденозинтрифосфат. В состав АТФ входят рибоза, аденин, три остатка фосфорной кислоты. Фосфаты последовательно связаны между собой. При этом два последних связаны между собой так называемой макроэргической связью, разрыв которой обеспечивает клетку большим количеством энергии. Таким образом, АТФ выполняет в клетке энергетическую функцию.  Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Всё это реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны, в том числе и для создания трансмембранного электрического потенциала; осуществления мышечного сокращения. Помимо энергетической, АТФ выполняет в организме ещё ряд других не менее важных функций: 1.Вместе с другими нуклеозидтрифосфатами АТФ является исходным продуктом при синтезе нуклеиновых кислот. 2.Кроме того, АТФ отводится важное место в регуляции множества биохимических процессов. Являясь аллостерическим эффектором ряда ферментов, АТФ, присоединяясь к их регуляторным центрам, усиливает или подавляет их активность. 3.АТФ является также непосредственным предшественником синтеза циклического аденозинмонофосфата — вторичного посредника передачи в клетку гормонального сигнала. 4.Также известна роль АТФ в качестве медиатора в синапсах и сигнального вещества в других межклеточных взаимодействиях Гидролиз макроэргических связей молекулы АТФ, сопровождаемый отщеплением 1 или 2 остатков фосфорной кислоты, приводит к выделению, по различным данным, от 40 до 60 кДж/моль. В организме АТФ является одним из самых часто обновляемых веществ; так, у человека продолжительность жизни одной молекулы АТФ менее 1 мин. ежесуточно синтезируется 125 моль АТФ, или 62 кг (это неточная информация) |
