Работа 2 Определение нитрата с ионоселективным электродом
 Скачать 23.73 Kb. Скачать 23.73 Kb.
|
Работа 2 |
| Раствор | c(NO3), М | рc(NO3) | pNO3 | Еизм, мВ | Евыч, мВ |
| № 1 | 1∙10-2 | 2 | 4,00 | 400,0 | |
| № 2 | 1∙10-3 | 3 | 3,02 | 359,2 | |
| № 3 | 1∙10-4 | 4 | 2,04 | 294,7 | |
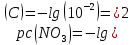
Результаты градуирования обрабатывают по линейному методу наименьших квадратов (МНК). Найденный в автоматическом режиме градуирования коэффициент наклона (S=58 мВ/pNO3) сравнивают с МНК-оценкой при ручных вычислениях, а также с теоретическим значением коэффициента в уравнении (1) и паспортными данными для электрода ЭЛИС-121NO3. Полученное по МНК уравнение линейной регрессии используют для вычислений Евыч. Затем по данным табл. 1 на миллиметровой бумаге строят график в координатах (pNO3, E). При этом точки, соответствующие Еизм изображают значками, а точки, соответствующие Евыч соединяют прямой.
Определение нитрата методом добавки при известной крутизне электродной функции.
mбюкса = 9,0774 г, mбюкса+10 капель = 9,3514 г
с=0,1М
E1=364,8 мВ +1 капля→ E2=361,1 мВ
+3 капли→ E3=356,4 мВ
+5 капель→ E4=351,0 мВ
+8 капель→ E5= 347,8мВ
+10 капель→ E6=343,3 мВ
+12 капель→ E6=340,5 мВ
Результат анализа вычисляют по формуле:
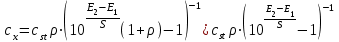 ,
,где = Vst/V, S – известный из паспорта электрода или установленный при градуировании коэффициент крутизны электродной функции.
