расчет сгорания. Расчет горения топливаметодичка по теплотехнике. Расчеты горения топлива обычно выполняются с целью определения
 Скачать 458.5 Kb. Скачать 458.5 Kb.
|
|
3.5. Примеры расчетов горения топлива. Для расчета горения топлива можно использовать два метода : -табличный; -расчетный. В рассмотренных ниже примерах будем использовать оба метода. Пример 1. Определить расход воздуха, состав и количество продуктов сгорания и калориметрическую температуру горения мазута. Его состав следующий, %: CР=85,6, НР=10,5, NР=0,7, ОР=0,5, SР=0,7, АР=0, WР=2. Провести расчет при величине коэффициента избытка воздуха n=1,15. Температура подогрева воздуха tВ=300 ˚ С. Решение: Расход воздуха, состав и количество продуктов сгорания определим, пользуясь табличным методом. Для удобства расчет горения жидкого топлива следует вести на 100 кг горючего. В основу расчета положены реакции полного сгорания отдельных элементов: С + О2 = СО2 Н2 + ½ О2 = Н2О S + О2 = SО2 Таблица 4 Форма таблицы для записи результатов определения расхода воздуха, количества и состава продуктов сгорания
Для определения калориметрической температуры необходимо знать теплоту сгорания топлива. Для жидкого топлива ее можно определить по формуле Д. И. Менделеева (см. табл. 3). Определим энтальпию продуктов сгорания при условии, что воздух подогрет до 300 ˚ С: I0= Задаемся возможной температурой горения tК = 1800˚ С. Для этой температуры энтальпия продуктов сгорания (см. приложение 3) будет равна: СО2 + SО2 . . . . . . . . . (0,1268+0,00039) ∙ 4360,67=553,81 Н2О . . . . . . . . . . . . . . . . . . . . . . . 0,0954 ∙ 3429,9=327,21 О2 . . . . . . . . . . . . . . . . . . . . . . . . .0,2609 ∙ 2800,48=730,65 N2 . . . . . . . . . . . . . . . . . . . . . . . . .0,7514 ∙ 2646,74=1988,76 –––––––––––––––––––––––––––––––––––––––––––––––– Итого . . . . . . . .. . . . . . . . . . . . . . . . . . . . . . . . . . . . 3600,43 кДж/м3 Поскольку I0 Примем tК = 1700 ˚ С, тогда энтальпия составит СО2 + SО2 . . . . . . . . . (0,1268+0,00039) ∙ 4087,1=519,06 Н2О . . . . . . . . . . . . . . . . . . . . . . . 0,0954 ∙ 3203,05=305,57 О2 . . . . . . . . . . . . . . . . . . . . . . . . .0,2609 ∙ 2632,09=686,71 N2 . . . . . . . . . . . . . . . . . . . . . . . . .0,7514 ∙ 2486,28=1868,19 –––––––––––––––––––––––––––––––––––––––––––––––– Итого . . . . . . . .. . . . . . . . . . . . . . . . . . . . . . . . . . . . 3380,05 кДж/м3 Поскольку I1800 ˚ С tК=1700 + Пример 2. Для случая сжигания смешанного газа (смеси коксовального и природного газов) с теплотой сгорания 12 МДж/м3 определить расход воздуха, состав и количество продуктов сгорания, калориметрическую температуру горения при коэффициенте расхода (избытка) воздуха n=1,2. Температура подогрева, воздуха 400 ˚ С. Составить материальный баланс процесса горения. Состав генераторного газа из тощих топлив (топливо А), %: СО2=6, СО=27, Н2=13, СН4=0,6, N2=53,4. Влажность топлива А WА=24 г/м3. Состав природного Бугурусланского газа (топливо Б), %: СН4=77,8, С2Н6=4,4, С3Н8=1,7, С4Н10=0,8, СО2=0,2, Н2S=1, N2=14. Влажность топлива Б WБ=4,5 г/м3. Решение: 1) Производим пересчет с сухой массы на влажную: Расчёт для газа А: 5,83 + 26,22 + 12,62 + 51,85 + 0,58 + 2,89 = 99,99 Расчёт для газа Б: 0,20 + 77,38 + 1,69 + 0,80 + 13,92 + 0,99 + 4,38 + 0,56 = 99,92 2) Определим теплоту сгорания каждого газа: Qрн = 127 СО + 108 Н2 + 358 СН4 + 590 С2Н4 + 555 С2Н2 + 635 С2Н6 + 913 С3Н8 +1185 С4Н10 + 1465 С5Н12 + 234 Н2S Qрн (А) = 127 · 26, 22 + 108 · 12, 62 + 358 · 0, 58 = 4900, 54 кДж/м3 Qрн (Б) = 358 · 77,38 + 635 · 4,38 + 913 ·1,69 + 1185 · 0,8 + 234 · 0,99 = =33205,97 кДж/м3 3) Определим состав смеси 2-х топлив: Для этого прежде всего определим долю топлива А в смеси, которую обозначим через а: 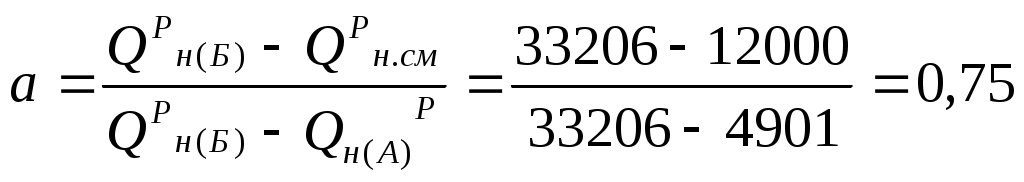 ХСМ=ХАа+ХБ(1-а) СО2см = СО2А а + СО2Б (1-а) = 5,83 · 0,75 + 0,20 · 0,25 = 4,42 % СОсм = 26,22 · 0,75 = 19,67 % Н2см = 12,62 · 0,75 = 9,47 % СН4см =0,58 · 0,75 + 77,38 · 0,25 = 19,78 % N2cм = 51, 85 · 0, 75 + 13, 92 · 0, 25 = 42, 38 % С3Н8см =1,69 · 0,25 = 0,42 % С4Н10см =0,8 · 0,25 = 0,20 % С2Н6см = 4,43 · 0,25 = 1,1 % Н2Sсм = 0.99 · 0,25 = 0,25 % Н2Осм = 2,89 · 0,75 + 0,56 · 0,25 = 2,31 % 4,42 + 19,67 + 9,47 + 19,78 + 42,38 + 0,42 + 0,20 + 0,25 + 1,1 + 2,31 = 99,99 4) определить расход воздуха, количество и состав продуктов сгорания: Определим расход воздуха, состав и количество продуктов сгорания в табличной форме. Расчет ведём на 100 м3 газа.
5) Для проверки правильности расчета составим материальный баланс. Расчет является верным, если погрешность не превышает 5%. Поступило, кг: Получено, кг: В том числе: Топливо СО2 =4,42 · 1,96 = 8,66 СО2 = 48.13 1.96 = 94.33 СО = 19,67 · 1,25 = 24,59 Н2О = 57.56 0.8 = 46.05 Н2 = 9,47 · 0,09 = 0,85 О2 = 21.18 1.43 = 30.29 СН4 = 19,78 ·0,71 = 14,04 N2 = 328.3 1.25 = 410.38 N2 = 42, 38 · 1, 25 = 52, 98 SO2 = 0.25 2.86 = 0.72 C3Н8 = 0, 42 · 1, 96 = 0, 82 –––––––––––––––––––––– C4Н10 = 0, 2 · 2, 59 = 0, 52 Итого 581,76 Н2S = 0,25 ·1,52 = 0,38 C2Н6 = 1, 1 · 1, 34 = 1, 47 Н2О = 2,31 · 0,8 = 1,85 Воздух О2 = 74,1 · 1,43 = 105,96 N2 = 277, 44 · 1, 25 = 346, 80 ––––––––––––––––––––––––– Итого 558,90 Погрешность | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
