Генетика №4. Различают изменчивость ненаследственную (или модификационную) Характерные черты
 Скачать 1.73 Mb. Скачать 1.73 Mb.
|
|
Различают изменчивость: – ненаследственную (или модификационную); Характерные черты: массовый характер изменений, затрагивающих большинство особей в популяции (например, воздействие ультрафиолетовых лучей на кожу человека приводит к изменению пигментации); адекватностью изменений воздействию среды — чем интенсивнее воздействие фактора, тем сильнее изменение (например, увеличение времени нахождения на солнце приводит к повышенной выработке пигмента); кратковременностью большинства модификаций (например, при прекращении пребывания на солнце пигментация кожи возвращается к обычному уровню). эволюционно закрепленной адаптивностью реакции организма в ответ на изменение условий внешней среды при неизменном генотипе; модификационная изменчивость ограничена нормой реакции. По выраженности нормы реакции признаки бывают пластичные (широкая норма реакции, зависят от ФВС) и непластичные (неизменными при любых условиях среды) – наследственную (или генотипическую) - онтогенетическую Изменения генетического аппарата: 1)рекомбинация генов (комбинативная изменчивость); 3 причины Кроссинговер как механизм рекомбинации эффективен лишь в том случае, когда соответствующие гены отцовской и материнской хромосом представлены разными аллелями Аа, гомозиготы не дают новых сочетаний аллелей (АА, аа); 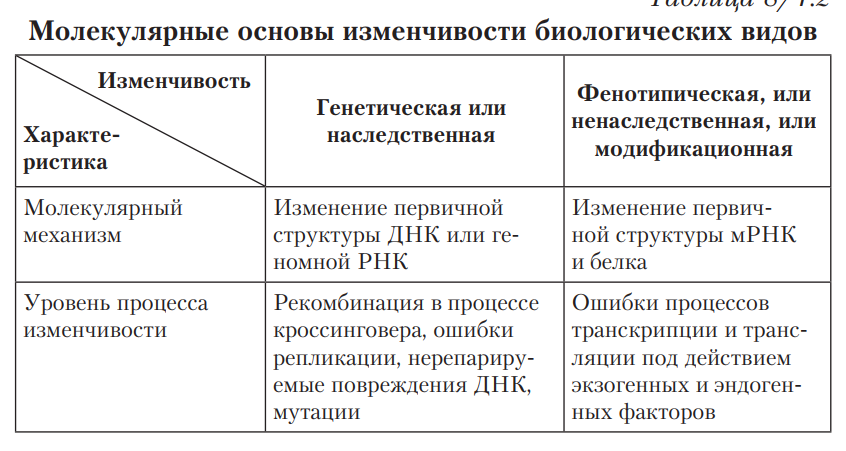 2)различные типы мутации (мутационная изменчивость) Гуго де Фриз (1901г.). Единицей мутации является мутон. Классификация мутаций по характеру 1) спонтанные (мутации в генах поддержания стабильности клеточного генома) 2) индуцированные (искусственный мутагенез) В эру становления генетики и борьбы с фальсификацией биологии и генетики представителями Т.Д. Лысенко было актуально выделять спонтанные и индуцированные мутации. К первым относили случаи, при которых вызывающий мутацию агент-мутаген был неизвестен в отличие от известного естественного или искусственного (экспериментального) мутагена для индуцированных мутаций. Сегодня эта классификация не имеет смысла, так как в обоих случаях действуют одни и те же факторы: естественная или искусственная радиация и ультрафиолет, вредные химические вещества, лекарства и др. по месту возникновения и характеру наследования различают мутации: 1)генеративные 2)соматические (барьер Вейсмана) влияния на жизнеспособность и плодовитость организма мутации бывают: 1)летальные 2)полулетальные (не доживает до репродукции) 3)условно летальные (разное проявление в разных условиях) 4)стерильные 5)нейтральные (в силу вырожденности генетического кода не всякая замена основания (аминокислоты) отразится на функциональной активности белка) по локализации измененного генетического материала мутации различают: 1) ядерные 2) цитоплазматические Концепция Р. Фон Борстела: Причины спонтанных мутаций – причины «трех P»: репликации, репарации, рекомбинации. При репликации возможно 2 типа ошибок: а) неправильное включение нуклеотидов, приводящие к замене нуклеотидов; 2) проскальзывание петли ДНК (матрицы) в области коротких тандемных повторов, приводящие к увеличению их числа( матрица сдвигается относительно новой комплиментарной цепи и часть матричной цепи либо пропускается, либо переходит машиной репликации дважды). Следствием этих мутаций является возникновение динамических мутаций – болезни экспансии повторов (синдром ломкой X-хромосомы). Мутации, обусловленные инсерцией (вставкой) протяженных мобильных элементов — транспозонов, на долю которых приходится до 5% ДНК всего генома. Проявления генных мутаций зависят от функций конкретного измененного гена: - опухоли (протоонкогены, антионкогены) - пороки развития (морфогены, отвечающие за органогенез) - нарушение процесса метаболизма (структурные гены) Нарушение процесса репарации ДНК: Существуют наследственные заболевания, возникающие вследствие дефектов ферментов пострепликативной (эксцизионной) и репликативной репарации. К первым относятся трихотиодистрофия (нарушение структуры белков из-за недостатка серы, особенно в волосах, инфантилизм) и пигментная ксеродерма. Оба заболевания обусловлены слабым удалением ультрафиолетовых димеров тимина. При ксеродерме (вероятен мутационный дефект УФ-эндонуклеазы) кожа очень чувствительна к солнечному свету, возникают дерматит, раны, язвы и рак кожи. При нарушении репликативной репарации возможны такие заболевания, как телеангиэктазия (синдром Луи—Барр) и синдром Блума. Последнее заболевание («красная бабочка» на лице) обусловлено дефектом фермента репликации ДНК-хеликазы. Экспансия тринуклеотидных повторов Динамические мутации –нарастанием триплетных повторов в кодирующих и некодирующих участках гена (ЦТГ, ЦГГ); (н. атаксия Фридрейха (Финляндия), хорея Гентингтона), повторы могут находиться в транскрибируемой (выключение гена) и нетранскрибируемой области, болезнь проявляется только после достижения порогового значения повторов – антиципация Генные мутации Нарушения работы ДНК-полимераз являются причинами возникновения генных мутаций. Точковые мутации (генные) – замены, вставки, выпадения нуклеотидов. Замена нуклеотидов: 1) миссенс- мутации ( серповидно-клеточная анемия); миссенс-мутации – изменяют смысл кода( не синонимичная замена ), появляется другая аминокислота, часто при ферментопатиях; бывают радикальные и консервативные нонсенс-мутации – сдвиг рамки считывания( н. синдром Дюшенна-Беккера, мукополисахаридов 1 типа , синдром Элерса-Данло - в зависимости от вида точковой мутации зависит тяжесть перенесения заболевания – н. муковисцидоз); сплансинговые мутации (однонуклеотидные замены на границе интронов и экзонов, обычно приводят к выпадению экзона или сохранению интрона, который часто несет стоп-кодон) – множественная эпифизарная дисплазия, синдром Элерса - Данло, синдактилия 2 типа, сплайсинговые мутации сгруппированы в определенном районе гена фибриллина замена оснований (транзиции и трансверсии) Также генные мутации делятся на: - односайтовые мутации – в одной точке - многосайтовые мутации – в нескольких Сдвиг рамки считывания происходит при вставке или выпадении нуклеотида (инсерция и делеция). Часто причиной вставки являются подвижные генетические элементы — протяженные нуклеотидные последовательности у эукариот и прокариот, которые самопроизвольно меняют свое положение. Сеймсенс-мутации –единичные синонимичные замены (Wooble-пары или неканонические пары). Функциональная дивергенция генов глобинов Положительное влияние дупликации: Условно выделяют дихотомическую эволюцию, т.е. появление новых генных локусов и генов в структуре ДНК (неравный кроссинговер, дупликации генов), и филетическую эволюцию. Последняя — это мутации идентичных, дуплицированных генов с возникновением новых генов. Гомологичные гены: Ортологи - гомологичные гены у разных организмов, возникшие в результате специализации Паралоги - у одного организма, возникшие в результате дупликации, накопления генных мутаций и последующего расхождения функций (дивергенции) Причины дупликаций: -неравномерный кроссинговер (появление одной хромосомы с делецией, другой с дупликацией) -мобильные элементы могут создать гомологичные участки, по которым возможен кроссинговер несестринских хроматид (н. дупликация генов лизоцима и лактальбумина (лизоцим дуплицировался у млекопитающих, но не у птиц) -дупликация экзона (появление дополнительного домена в белковой молекуле) Ошибки во время мейоза могут привести к дополнительным наборам хромосом (полиплоидия), чаще всего такие ошибки летальны, но в редких случаях могут способствовать эволюции генов. У полиплоидов необходимые им функции может обеспечить один набор генов, гены дополнительного набора могут дивергировать путем накопления мутаций, эти изменения могут сохраняться, т.о могут сформироваться гены с новыми функциями. МУЛЬТИГЕННОЕ СЕМЕЙСТВО ГЛОБИНОВ: Одно из этих семейств, расположенное на хромосоме 16 в организме человека, кодирует различные формы α-глобина; другое семейство, расположенное на хромосоме 11, кодирует формы β-глобина. В разное время в процессе развития экспрессируются различные формы каждого глобина, что позволяет гемоглобину эффективно функционировать в меняющихся условиях в развивающемся животном. Например, в организме человека эмбриональные формы гемоглобина имеют более высокое сродство к кислороду, чем взрослые формы, обеспечивая эффективную передачу кислорода от матери к плоду. Также в генном семействе глобинов обнаружено несколько псевдогенов. Воссоздание эволюционной истории глобиновых генов с использованием этого подхода указывает на то, что все эти гены произошли от одного общего предкового гена глобина, прошедшего дупликацию и дивергенцию в предковые α- и β-глобины около 450-500 миллионов лет назад. Каждый из этих генов был впоследствии дуплицирован несколько раз, после чего копии расходились друг от друга по последовательности, что привело к появлению нынешних членов семейства. Общий предковый ген глобина также дал начало миоглобину. 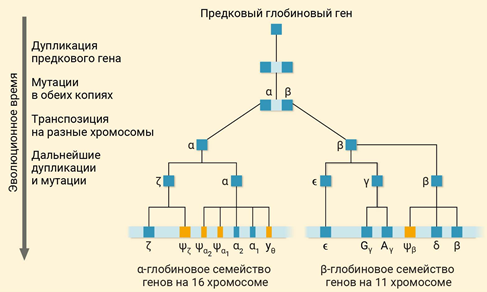 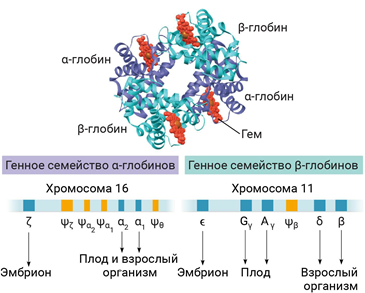 При развитии человеческого эмбриона и далее у взрослого человека серия генов (блок генов) в хромосоме 11, кодирующих второй глобин для гемоглобина (кроме D-глобина), подвергается последовательному выключению и включению на уровне транскрипции. В процессе онтогенеза происходит поэтапный синтез следующих гемоглобинов:  HbE – HbF – HbA - 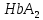 HbF(фетальный) имеет второй гемоглобин γ-глобин имеет 21 положении аминокислоту серин с незаряженным радикалом, а у HbA у β-глобулина эту позицию занимает гистидин с положительным радикалом, поэтому менее заряженный эмбриональный гемоглобин слабее образует ионные связи с БФГ(несет 5 отрицательных зарядов) и уменьшает сродство Hb к кислороду(повышает высвобождение кислорода). Образование изоформ белков также обусловлено одновременной транскрипцией разных аллельных генов(кодоминирование –два аллеля одного гена кодируют образование двух разных иРНК и соответственно двух разных изоферментов А и В (4 группа крови)   С биохимической точки зрения интересно сравнить основной гемоглобин взрослого человека HbA и эмбриональный HbF. У последнего второй глобин — J-глобин — имеет в 21-м положении аминокислоту серин с незаряженным радикалом, а в HbA у соответствующего E-глобина эту позицию занимает гистидин с положительно заряженным радикалом. Поэтому менее заряженный эмбриональный HbF слабее образует ионные связи с 2,3-бисфосфоглицератом, который несет 5 отрицательных зарядов и который уменьшает сродство Hb к кислороду. В итоге HbF более прочно связывает в плаценте кислород и перехватывает его HbA матери для эмбриона. Заболевания, связанные с гемоглобином: Существуют и другие мутации гена, приводящие к появлению аллелей, гомозиготные носители которых страдают бета-талассемией. При так называемом гемоглобине Кренстона существует длинная боковая цепь. Причиной заболевания служит инсерция (вставка) двух нуклеотидов в 145-й триплет гена бета-глобина. В результате «стоп-кодон» УАА при изменении образца считывания триплетов гена («кадровый сдвиг») превращается в кодон АЦУ. При этом синтез полипептидной цепи продолжается и заканчивается лишь после присоединения дополнительно еще 11 аминокислот, т.е. после образования цепи из 157 аминокислот. Слишком длинная цепь глобина формирует нестабильный гемоглобин. Персистенция фетального гемоглобина – заболевание считается относительно доброкачественным, хотя фетальный гемоглобин е позволяет организму полностью приспособится к взрослой жизни. Происходит мутация в некодирующей (регуляторной) части гена. Вероятно они принимают участие в регуляции транскрипции различных генных локусов, активируемых на разных стадиях развития. ! Приведенные примеры свидетельствуют, что в результате изменений нуклеотидных последовательностей генов, т.е. мутаций, в процессе эволюции возникают множественные аллели — разные версии первоначального гена. Мутации, вызванные заменой азотистых оснований, могут быть на молекулярном уровне двух типов: 1) простые замены — транзиции, когда один пурин замещается другим пурином, а пиримидин — другим пиримидином; 2)перекрестные замены — трансверсии, т.е. замена пурина на пиримидин, и наоборот. Неточковые мутации: делеции (не приводят к сдвигу рамки считывания – менее серьезные) , инверсии, дупликации, инсерции нуклеотидов – внутригенные перестройки (н. нейрофиброматоз, гемофилия А, миопатия Дюшенна). Хромосомные абберации: Сбалансированные – без потери наследственного материала Несбалансированные - с потерей наследственного материала При нарушении кроссинговера хромосомы могут обмениваться неравноценными участками хромосом. Это ведет к появлению новых групп сцепления, где отдельные участки могут выпадать (делеция) или удваиваться (дупликация) или перемещаться (транслокация). При таких перестройках изменяется число генов в группе сцепления. В зависимости от того, включает данный участок область центромеры или нет, различают: перицентрические и парацентрические инверсии (фрагмент хромосомы, отделившийся от нее при разрыве, может быть утрачен клеткой при очередном митозе, если он не имеет центромеры). Такой фрагмент может прикрепляться к какой-то негомологичной хромосоме путем транслокации. Нередко две поврежденные негомологичные хромосомы взаимно обмениваются оторвавшимися участками — реципрокная транслокация (конъюгация меняется, вместо бивалента образуется квадралент в виде фигуры креста) Иногда негомологические структуры хромосом объединяются в одну — робертсоновская транслокация (н. два плеча крупной 2-й хромосомы человека соответствуют двум разным хромосомам современных человекообразных обезьян: 12-й и 13-й — у шимпанзе, 13-й и 14-й — у гориллы и орангутана). Филадельфийская хромосома - транслокация между хромосомами 9 и 22, эта мутация вызывает 95 % случаев хронического миелолейкоза и является одной из самых распространённых при В-клеточном остром лимфобластном лейкозе взрослых Геномные мутации -гаплоидия -полиплоидия Причины: – нарушения расхождения хромосом при митозе; – слияния клеток соматических тканей, либо их ядер; – нарушений мейоза, приводящих к образованию гамет с нередуцированным числом хромосом. Анеуплоидия — это изменение числа хромосом, не кратное гаплоидному набору за счет потери одной хромосомы из пары (моносомия – н. синдром Шершевского-Тернера – крупные лимфедемы области головы и шеи, фетальная лимедема => крыловидные складки), двух из пары (нуллисомия) или добавления отдельных хромосом (полисомия – н. синдром Кляйнфельтера). Девочки с тремя Х-хромосомами не имеют физических отклонений, но часто возникают проблемы с обучением. Механизм анеуплоидии связан с нарушением расхождения хромосом при мейозе. У человека встречаются трисомии по 21, 18 и 13 хромосомам, их частота зависит от возраста матери, трисомия пр другим хромосомам не совместима с жизнью. Причина таких различий относительно низкая плотность генных локусов на хромосомах 21, 18, 13. Трисомия по 21 хромосоме может возникать у сублингов, это происходит из-за транслокации с участием хромосомы 21, чаще всего из-за центрического слияния с другой акроцентрической хромосомой (робертсоновская транслокация) ** по хромосомам 13 (синдром Патау) и 18 (синдром Эдвардса) Микроделеции – структурные хромосомные нарушения (с. кошачьего крика, примерно у 12% один из родителей ребенка имеет транслокацию, затрагивающую хромосому 5) Различают следующие мутагенные факторы (мутагены): – физической природы, к ним относятся различные виды излучений: R-, β-, γ- и α-лучи, космические лучи, ультрафиолетовый свет, в меньшей степени — температура. – химической природы — различные химические вещества, которые взаимодействуют с ДНК. – биологической природы — это вирусы, которые внедряют информацию в геном клетки (бактерии). Мутагенное действие ионизирующих излучений (физические мутагены) часто приводит к ковалентному сшиванию двух цепей ДНК. – разрывы углеводно-фосфатного скелета молекулы ДНК; – разрушение оснований, в результате чего происходит химическая пере- стройка оснований (чаще) - при УФ облучении происходит возникновение тиминовых димеров, при этом водородные связи образуются между соседними тиминами одной цепи ДНК, что блокирует работу ДНК-полимераз Мутагенное действие химических веществ: - алкилирующие соединения и окислители-восстановители Алкилирующие соединения вызывают поперечные сшивки цепей в молекуле ДНК, приводящие к разрыву хромосом и появлению хромосомных аберраций. Под действием алкилирующих веществ могут образовываться сшивки ДНК-белок - соединения, мутагенные только в отношении реплицирующейся ДНК. К ним относятся производные пуринов и пиримидинов, акридиновые красители. Аналоги оснований, по молекулярной структуре похожие на основания, входящие в цепи ДНК, приводят к мутациям, так как они могут существовать в альтернативных (таутомерных состояниях) - наиболее частые — это кето- и аминоформы, обеспечивающие нормальное спаривание оснований при репликации, и очень редкие окси- и иминоформы, нарушающие указанное выше правило. Исправление подобных эндогенных ошибок возможно до того момента, пока синтезированная нить ДНК не подверглась метилированию. ДНК-полимераза может вырезать ошибочный нуклеотид и далее его заменить на правильный комплементарный нуклеотид. Или существуют специальные белки mut, которые находят ошибку и также ее исправляют. Так происходит репликативная репарация. -акридиновые красители (акридин оранжевый, профлавин и др.) индуцируют мутации типа сдвига рамки считывания. Они внедряются между соседними основаниями в ДНК. Молекула ДНК увеличивается на длину одного нуклеотида и при последующей репликации напротив внедряющейся молекулы красителя встраивается дополнительный дезоксирибонуклеотид, что и изменяет рамку считывания. - среди лекарственных препаратов существуют вещества цитостатического действия, лечебный эффект которых часто связан с их мутагенными свойствами. Цитостатики вызывают повреждения ДНК всех активно делящихся клеток (опухолевых, стволовых) и останавливают клеточные деления. К таким препаратам относят циклофосфан (ЦФ) и нитрозометилмочевину (НММ), представляющие собой алкилирующие соединения. Они вызывают, например, алкилирование азотистых оснований (присоединение алкильных или чаще метильных групп), приводящее к мутациям типа замены оснований) ! Смысл применения цитостатиков при лечении онкологических заболеваний состоит в индуцировании мутаций в ДНК и в запуске апоптоза или механизма самоуничтожения дефектной клетки. Поскольку в первую очередь повреждаются активно делящиеся клетки, то они и погибают. На подобный эффект рассчитана не только химиотерапия, но и лучевая терапии рака, поскольку ионизирующее излучение также вызывает повреждения ДНК в активно делящихся клетках. Мутагенное действие биологических агентов: -вирусы черной оспы, кори, ветряной оспы, эпидемического паротита, гепатита способны вызывать разрывы хромосом, усиливать темпы мутации клеток хозяина за счет подавления активности репарационных систем. Например, причиной лейкоза могут быть вирусы лейкемии, поражающие клетки костного мозга, головного мозга, селезенки. Есть данные о возрастании числа хромосомных перестроек в клетках человека после пандемий, вызванных вирусами гриппа. Внутри собственного генома существуют факторы, вызывающие мутации и нестабильность. К таким факторам относятся транспозиции мобильных элементов и ретровирусов. МГЭ: В 1940 году Барбара МакКлинток открыла существование у кукурузы локуса, который вызывает повышение частоты хромосомных перестроек – контролирующего элемента (КЭ). В 1983 году ей была вручена Нобелевская премия по физиологии и медицине «за открытие мобильных генетических элементов». Положение мобильных элементов: Способность к перемещению, или транспозиции, осуществляется двумя путями: 1-й – с помощью специальных ферментов для вырезания и встраивания повтора в любой участок хромосом (транспозоны), «вырезание-вставка» 2-й – с помощью гена фермента – обратной транскриптазы, который обеспечивает построение дополнительной копии ДНК по матрице РНК, с последующим внедрением копии в хромосому с помощью рекомбинации (ретротранспозоны) «копирование-вставка». На самом деле ретровирусы, вероятно, являются производными ретротранспозонов. Ретровирусы способны при образовании новых вирусных частиц активированного провируса может захватываться часть генетического материала клетки хозяина и передаваться другим организмам, минуя межвидовые барьеры (провирус – встраиваемая в геном ДНК-копия) Участие мобильных элементов в эволюции генома: -обеспечивают рекомбинацию, нарушая последовательность генов или регуляторных элементов клетки -переносят отдельные отдельные экзоны в новые положения в геноме -отдельный вид ДНК-повторов – тандемные повторы. Большая часть их находится в теломерах и центросомах хромосом, предотвращая потерю генов при укорочении ДНК в каждом раунде репликации. Антимутагены Для того чтобы уменьшить токсическое действие цитостатиков на нормальные клетки при сохранении терапевтического действия препаратов используют антимутагены. К антимутагенам относят некоторые витамины (А, Е, С), мелатонин-содержащие препараты (способен связывать свободные жиро- и водорастворимые радикалы (за счет наличия в его составе ионов Fe 3+ ). кроме того, он активирует фермент глутатионпероксидазу, превращающую перекись водорода в воду и кислород, активирует гены других антиокислительных ферментов, например, глутатионредуктазы, разлагающий перекись водорода до воды и атомарного кислорода). Механизм действия витаминов как антимутагенов заключается в том, что провитамин А и витамин Е связывают жирорастворимые свободные радикалы, а витамин С – водорастворимые. Механизм действия антимутагенов: - нейтрализация мутагена до его взаимодействия с ДНК - предотвращение образования в процессе метаболизма активных мутагенных продуктов из нетоксичных предшественников - активация ферментных систем детоксикации - активация репарации Естественные биологические антимутационные механизмы 1. Парность хромосом (гомологичные хромосомы) Вновь возникшие гены, как правило, оказываются рецессивными по проявлению у гетерозигот. Требуется время для накопления их в популяции. При случайной встрече двух гетерозиготных организмов, появится шанс фенотипического проявления нового мутантного гена. 2. Избыточность генетического кода + Wooble пары !!! Кодоны ЦЦЦ, ЦЦА, ЦЦГ, ЦЦУ кодируют одну аминокислоты – пролин 3. Экзон-интронное строение гена эукариот (ДНК-нуклеосомная нить образует функциональные специфические участки — домены, каждый домен выполняет определенную функцию в белке и кодируется отдельным экзоном) 4. Системы репарации ДНК Изменение функциональной активности белка при мутации (возможные варианты): 1. Если при мутации (изменении первичной структуры ДНК) функция белка не изменилась, то, вероятно, измененная аминокислота не существенна для работы центра связывания белка или изменения в белке отсутствуют из-за вырожденности генетического кода. 2. При небольшом изменении функциональной активности белка (повышении или снижении) вероятны миссенс-мутации или делеции и вставки без сдвига рамки чтения кода. 3. Полная инактивация мутантного белка-фермента возможна при нонсенс-мутациях (синтезируется укороченный белок) и делециях и вставках со сдвигом рамки чтения кода. Не все мутации в ДНК реализуются фенотипически по следующим причинам: Соответствующие причины, нейтрализующие эти генные изменения: -вырожденность генетического кода -рецессивные мутации, -репарация ДНК, -обратные мутации, - 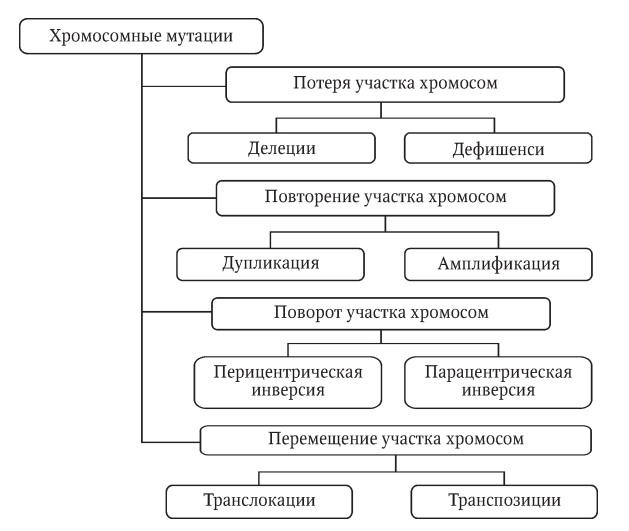 мутации, предотвращающие рождение нежизнеспособного потомства. мутации, предотвращающие рождение нежизнеспособного потомства.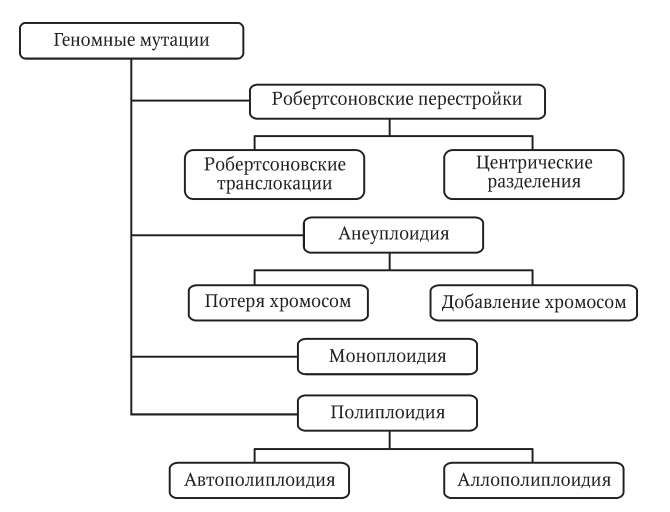 |
