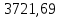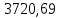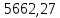Пример решения задач (1). Решение Уравнение реакции образования ацетилена CaC 2 2H 2 ОCa(OH) 2 c 2 h 2
 Скачать 36.79 Kb. Скачать 36.79 Kb.
|
|
1. Рассчитать материальный баланс процесса производства ацетилена из карбида кальция. Исходные данные: - производительность по ацетилену – 15 т/сут; - конверсия карбида кальция – 0,8; - конверсия воды – 0,6; - содержание примесей в карбиде кальция – 25%; - содержание примесей в воде – 10%. Решение: Уравнение реакции образования ацетилена CaC2+ 2H2О⟶Ca(OH)2+ C2H2↑ Молекулярные массы компонентов: Карбид кальция: CaC2= 64, Вода: H2О = 18, Гидроксид кальция: Ca(OH)2 = 74 Ацетилен: C2H2 = 26, По условию задачи производительность по ацетилену – 15 (т/сут) или 625 (кг/час). По массе целевого продукта C2H2cогласно стехиометрии определяем расход чистых реагентов CaC2 и H2О на целевую реакцию: 642*187426 CaC2 + 2H2О⟶ Ca(OH)2 + C2H2↑ 625 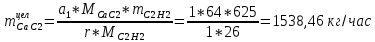 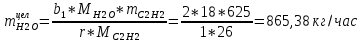 Помимо ацетилена, образовался гидроксид кальция: 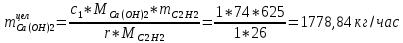 Учитываем конверсию реагентов: конверсия карбида кальция – 0,8; - конверсия воды – 0,6; 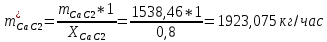 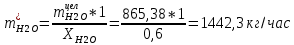 Определяем непревращенный остаток для каждого из реагентов, 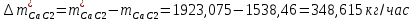 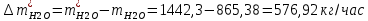 Найдем массу технического реагента CaC2 с учетом его состава: 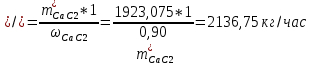 Рассчитаем массу технического реагента H2О с учетом его состава: 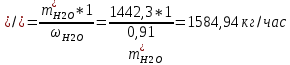 Масса примесей технического реагента CaC2и H2Оравна: 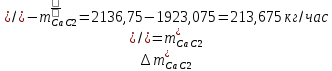 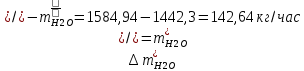 Составляем уравнение материального баланса 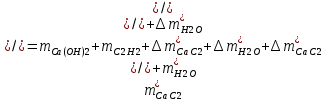 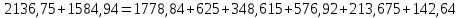 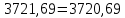 Составляем таблицу материального баланса:
2. Составить материальный баланс процесса производства хлорбензола (процесс сложный необратимый параллельный). Рассчитать расходные коэффициенты по сырью, селективность процесса, выход целевого продукта. Исходные данные: - производительность по техническому хлорбензолу – 60 т/сут; - содержание хлорбензола в целевом продукте – 70%; - содержание дихлорбензола в целевом продукте – 30%; - содержание примесей в бензоле – 10%; - содержание примесей в хлоре – 25%; - конверсия бензола – 0,8; - конверсия хлора – 0,6. Решение: Основная реакция C6H6 + Cl2 → C6H5Cl + HCl (1) Побочная реакции C6H6 + 2Cl2 → C6H4Cl2 + 2HCl (2) Молекулярные массы компонентов: Бензол: С6Н6= 78, Хлорбензол: С6Н5Cl = 112,5, Дихлорбензол: С6Н4Cl2 = 147 Хлор: Cl2 = 71, Хлороводород: HCl = 36,5. По условию задачи производительность по техническому хлорбензолу – 60 (т/сут) или 2500 (кг/час). Технический хлорбензол содержит 70% масс. хлорбензола и 30% масс. дихлорбензола. Определим массу каждого продукта в составе реакционной массы после протекания процесса (в техническом хлорбензоле): 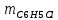 = 2500 · 0,7 = 1750 (кг/час) = 2500 · 0,7 = 1750 (кг/час)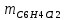 = 2500 · 0,3 = 750 (кг/час) = 2500 · 0,3 = 750 (кг/час)Проверяем правильность расчета: 1750кг/час + 750кг/час = 2500 кг/час По массе целевого продукта C6H5Clcогласно стехиометрии определяем расход чистых реагентов С6Н6 и Сl2 на целевую реакцию: 78 71 112,5 36 C6H6 + Cl2 → C6H5Cl + HCl 1750 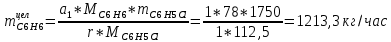 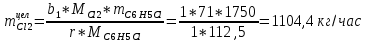 Помимо хлорбензола, образовался хлороводород: 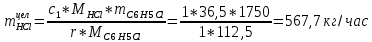 Определяем расход чистых реагентов С6Н6 и Сl2 на побочную реакцию: 78 2*71 1472*36 C6H6 + 2Cl2 → C6H4Cl2 + 2HCl 750 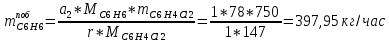 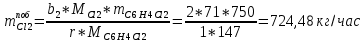 Помимо хлорбензола, образовался хлороводород: 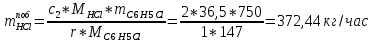 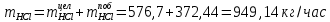 Суммируем массы каждого из реагентов, израсходованных на целевую и побочные реакции: 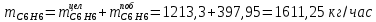 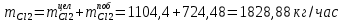 Учитываем конверсию реагентов: 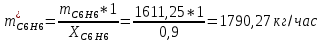 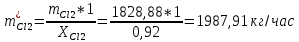 Определяем непревращенный остаток для каждого из реагентов, 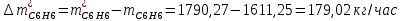 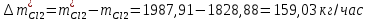 Найдем массу технического реагента С6Н6 с учетом его состава: 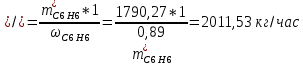 Рассчитаем массу технического реагента Сl2 с учетом его состава: 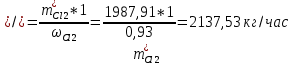 Масса примесей технического реагента С6Н6и Сl2равна: 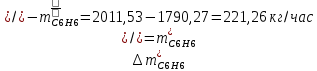 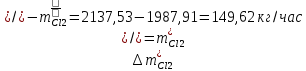 Составляем уравнение материального баланса 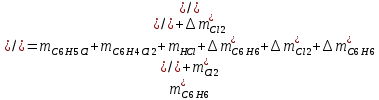 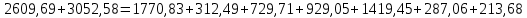 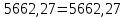 Составляем таблицу материального баланса:
Рассчитаем селективность процесса по реагентам: 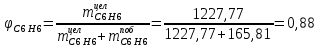 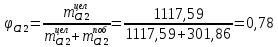 Выход на подданное сырье: 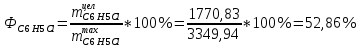 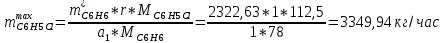 Выход на превращенное сырье: 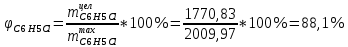 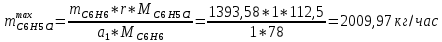 Расходные коэффициенты по сырью: - фактические: 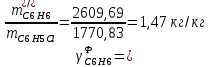 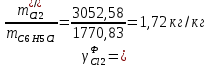 Теоретические 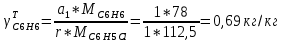 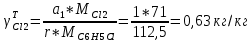 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||