Решение задач на вывод химических формул
 Скачать 66.5 Kb. Скачать 66.5 Kb.
|
|
Расчетные задачи «Решение задач: на вывод химических формул»IA Вычисление молекулярной формулы газа по массовым долям химических элементов и относительной плотности одного газа по другому.Формулы, используемые при решении данного типа задач: Д – относительная плотность одного газа по другому (1) (2) (3) Образец решения задачи Найти молекулярную формулу газа, содержащего по массе 85,7% углерода и 14,3% водорода. Относительная плотность паров этого газа по водороду равна 14.
IB Вычисление молекулярной формулы газа по массовым долям химических элементов и плотности вещества.Формулы, используемые при решении данного типа задач: (1) 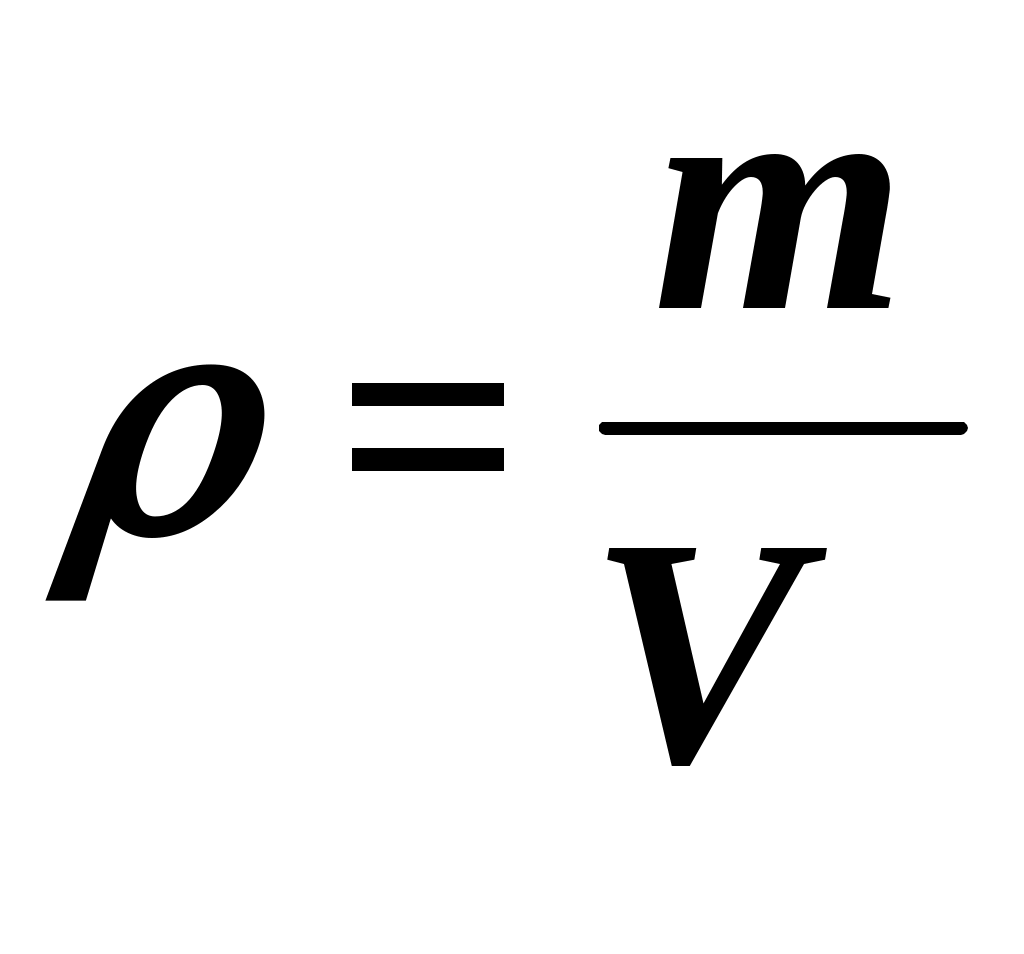 если взять количество вещества 1 моль, расчет по формуле: Образец решения задачи Найти молекулярную формулу газа, содержащего по массе 85,7% углерода и 14,3% водорода. Плотность вещества при нормальных условиях 1,875 г/л.
Решить задачи: 1) Найти молекулярную формулу вещества, если в его состав входят 80% углерода и 20% водорода. Относительная плотность паров этого вещества по водороду равна 15. Ответ: С2Н6 - этан 2) Найти молекулярную формулу газа, содержащего по массе 82,8% углерода и 17,2% водорода. Плотность вещества при нормальных условиях 2,59 г/л. Ответ: С4Н10 - бутан |