|
|
сабақ жоспары. 40 урок. Решение задач Расчет массовойобъёмной доли выхода продукта по сравнению с теоретически возможным выходом
Раздел:
|
9.3А Элементы 17 (VII), 16 (VI), 15 (V), 14 (VІ) групп и их соединения
|
ФИО педагога
|
|
Дата:
|
|
Класс: 9
|
Количество присутствующих:
|
Количество отсутствующих:
|
Тема урока
|
Решение задач «Расчет массовой/объёмной доли выхода продукта по сравнению с теоретически возможным выходом»
|
Цели обучения в соответствии
с учебной программой
|
9.2.3.3 -вычислять выход продукта реакции по сравнению с теоретически возможным
|
Цели урока
|
Изучить способ вычисления массовой / объёмной доли выхода продукта реакции по сравнению с теоретически возможным и применять его на практике
|
Ход урока
Этап урока/ Время
|
Действия педагога
|
Действия ученика
|
Оценивание
|
Ресурсы
|
Начало урока
5мин
|
Вызов. Прием «Найди соответствие»
1.Учащиеся читают ключевые термины и их определения
2. Соотносят термин и определение.
Теоретическая масса (объем, количество вещества)
|
это масса продукта реакции, которая получается в соответствии с расчетом по уравнению реакции
|
Практическая масса (объем, количество вещества)
|
это масса продукта, полученная в результате реакции с учетом потерь. Всегда меньше теоретической
|
Выход продуктов реакции в сравнении с теоретически возможным
|
это отношение практически полученной массы (объема, количества моль) к теоретической массе, рассчитанной согласно уравнению реакции.
|
Доля выхода продукта
|
обозначается ᵑ (эта) измеряется в процентах или долях
|
Определяет тему и цель урока.
|
Учащиеся отвечают на вопросы выходят к названию темы урока и целям урока.
|
2 балла
|
Карточки
|
Середина урока
20 мин
|
Глоссарий:
На русском языке
|
На казахском языке
|
На английском языке
|
Выход продукта
|
Өнімнің шығуы
|
product yield
|
Теоретическая масса
|
Теориялық массасы
|
theoretical mass
|
Практическая масса
|
Практикалық массасы
|
practical mass
|
Решение задач
|
Міндеттерді шешу
|
solution to the problem
|
формула
|
формула
|
formula
|
Алгоритмы решения задач трёх типов:
Определение выхода продукта в % от теоретически возможного.
1. Запишите уравнение химической реакции и расставьте коэффициенты.
2. Под формулами веществ напишите количество вещества согласно коэффициентам.
3. Практически полученная масса известна.
4. Определите теоретическую массу.
5. Определите выход продукта реакции (%), отнеся практическую массу к теоретической и умножив на 100%.
6. Запишите ответ.
Расчет массы продукта реакции, если известен выход продукта.
1. Запишите “дано” и “найти”, запишите уравнение, расставьте коэффициенты.
2. Найдите теоретическое количество вещества для исходных веществ. n =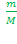
3. Найдите теоретическое количество вещества продукта реакции, согласно коэффициентам.
4. Вычислите теоретические массу или объем продукта реакции.
m = M * n или V = Vm * n
5. Вычислите практические массу или объем продукта реакции (умножьте массу теоретическую или объем теоретический на долю выхода).
Расчет массы исходного вещества, если известны масса продукта реакции и выход продукта.
1. По известному практическому объёму или массе, найдите теоретический объём или массу (используя долю выхода продукта).
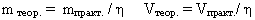
2. Найдите теоретическое количество вещества для продукта.
3. Найдите теоретическое количество вещества для исходного вещества, согласно коэффициентам.
4. С помощью теоретического количества вещества найдите массу или объем исходных веществ в реакции.
Решение задач у доски
Задача №1.При нитровании 4,48 л этана (н. у.) азотной кислотой получили 12 г нитроэтана C2H5NO2. Вычислите массовую долю выхода продукта. {Ответ: 80%.)
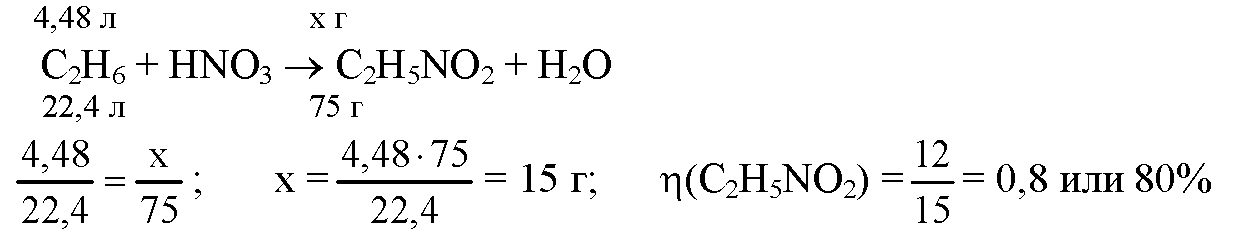
Задача №2.При нитровании гексана азотной кислотой при нагревании образуются нитрогексан C6H13NO2 и вода. Составьте уравнение этой реакции и рассчитайте, какую массу нитрогексана можно получить при нитровании гексана массой 43 г, приняв, что массовая доля выхода продукта составляет 80%. (Ответ: 52,4 г.)
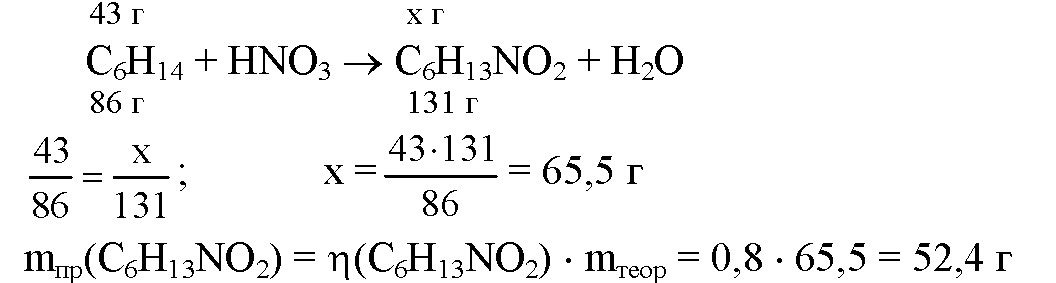
Задача №3.Для сжигания 30 л метана израсходовали 200 л воздуха, обогащённого кислородом. Рассчитайте объёмную долю кислорода в этом воздухе. (Ответ: 30%.)
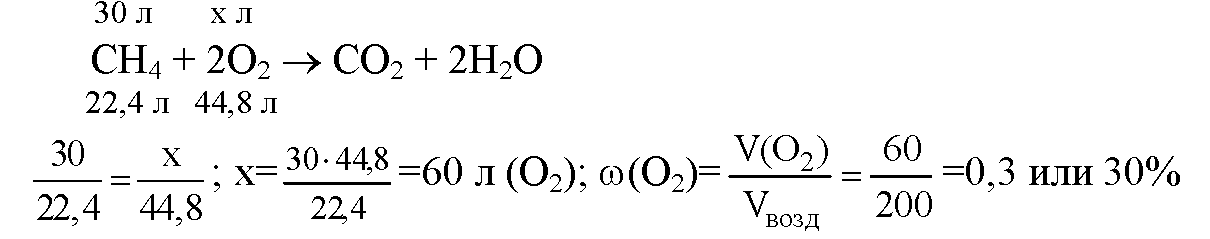
|
Учащиеся вначале знакомятся с глоссарием, затем выполняют задания в паре
|
5 баллов
|
Карточки,
|
Конец урока
10 мин
|
При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 4,5 г. Определите выход продукта реакции (%).
Определите, какая масса меди вступит в реакцию с концентрированной серной кислотой для получения оксида серы (IV) объёмом 3 л (н.у.), если выход оксида серы (IV) составляет 90%.
3.Определить верные/неверные утверждения о выходе продукта реакции (T/F):
1. Выход продукта реакции может быть больше 100%.
2. Зная практическую и теоретическую массу, можно вычислить выход продукта реакции
3. Массовую долю выхода продукта считают как отношение массы теоретической к массе практической.
4. Теоретическую массу продукта можно рассчитать по уравнению реакции.
5. Практическая масса продукта – это масса продукта, рассчитанная по уравнению реакции.
6. Выход продукта реакции можно рассчитывать в массовых долях или процентах
7. Теоретический выход всегда больше практического
8. При расчёте массовой доли выхода продукта реакции всегда нужно знать массу раствора.
9.Выход продукта реакции обозначается ᵑ (эта)
10. Для определения выхода продукта реакции необходимо знать заранее теоретическую массу.
Дескриптор:
− составляет сбалансированное уравнение химической реакции;
− вычисляет теоретическую массу (объем) продукта реакции;
− определяет массовую долю выхода продукта;
− вычисляет массу исходного вещества.
|
Выполняют задания для ФО
|
3 балла
|
карточки
|
Рефлексия
5 мин
|
Рефлексия «Музыкальная нота»

|
Обратная связь, комментарии учащихся и учителя
|
|
музыка
|
|
|
|
 Скачать 69.99 Kb.
Скачать 69.99 Kb.