Электрохимия. уз5 максимова х-210006. Рр 2 Кинетика простых реакций Учебное задание 5 Расчет константы скорости реакции второго порядка
 Скачать 46.24 Kb. Скачать 46.24 Kb.
|
|
РР 2 «Кинетика простых реакций» Учебное задание 5: «Расчет константы скорости реакции второго порядка» Вариант 1 Кинетика гомогенной реакции A + B = C описывается кинетическим уравнением второго порядка. Известна константа скорости и начальные концентрации исходных веществ: k = 0,00238 м3 моль-1 мин-1; сA,0 = 25 моль/м3; сB,0 = 50 моль/м3. Необходимо: 1) выразить зависимость концентрации реагирующих веществ и продуктов реакции от времени; 2) рассчитать текущие концентрации реагирующих веществ и продукта реакции; 3) построить кинетические кривые всех участников реакции в интервале времени от 0 до 60 мин с шагом 10 мин. Дано:
Решение: 1) Для реакции второго порядка при неравенстве концентраций исходных веществ плотность глубины реакции (х) рассчитывается по уравнению: 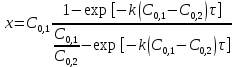   Рассчитаем плотность глубины реакции ко времени 10 мин.  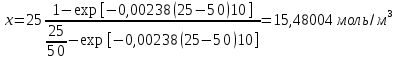 Тогда    Сведем данные в таблицу
Построим по данным таблицы кинетические кривые 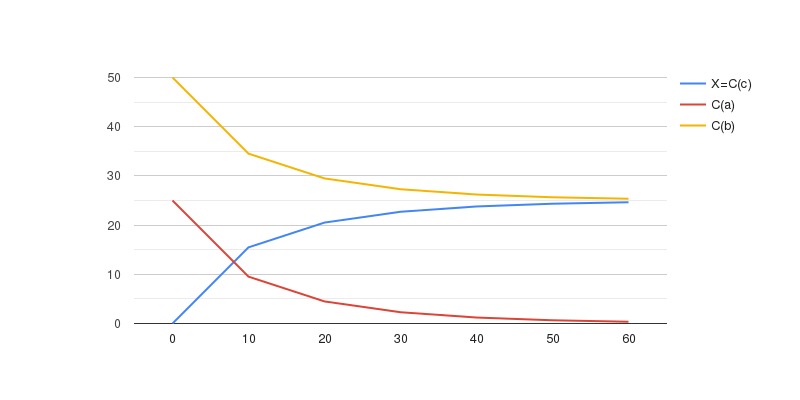 |



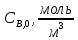
 моль/м3
моль/м3