Санкт-Петербургский государственный педиатрический медицинский университет
Кафедра общей и медицинской химии
|
Специальность
«Педиатрия»
|
Дисциплина «Химия»
|
Семестр 1
|
БИЛЕТ № 77
Вопрос №1 (Тест)
Как меняется прочность ковалентной связи Н-Э в ряду H2O → H2S → H2Sе → H2Те?
1) возрастает 2) уменьшается 3) не изменяется 4) растет, затем уменьшается
Диссоциация внутренней сферы комплексного соединения усиливается
1) с увеличением концентрации комплексного соединения 2) с повышением температуры раствора
3) с понижением температуры 4) при добавлении сахарозы
Степень диссоциации в растворах слабых электролитов – это отношение
1) количества продиссоциированных молекул к общему количеству молекул вещества
2) общего количества молекул вещества к количеству, продиссоциированных молекул
3) активной концентрации вещества к общей концентрации вещества в растворе
4) общей концентрации вещества в растворе к активной концентрации вещества
Усилить гидролиз соли KCN можно добавлением вещества, формула которого
1) NaOH 2) KCl 3) HCl 4) CH3COONa
Укажите, какая из приведенных смесей электролитов может проявлять буферные свойства?
1) Na2SO4, H2SO4 2) Na2CO3, NaOH 3) Na2CO3, NaHCO3 4) NaCl, HCl
Внутренняя поверхность клеточной мембраны в состоянии физиологического покоя
1) заряжена положительно 2) заряжена отрицательно
3) не заряжена 4) вначале заряжена положительно, затем отрицательно
Среди перечисленных веществ выберите ПИВ.
1) бутановая кислота 2) NaNO3 3) пальмитат калия 4) все перечисленные
Седиментация – это
1) оседание частиц под действием силы тяжести 2) образование агрегатов 3) отталкивание частиц 4) слипание частиц
Потенциал течения – это
1) потенциал на границе скольжения фаз
2) потенциал на поверхности частиц
3) разность потенциалов, возникающая при оседании частиц под действием сил гравитации
4) разность потенциалов при перемещении дисперсионной среды через капиллярно-пористую перегородку.
Процесс высаливания сопровождается
1) понижением температуры 2) понижением заряда
3) уменьшением растворимости полимера 4) увеличением давления
Вопрос №2
Необратимый гидролиз. Особенности гидролиза кислых солей (рассмотреть на примере солей фосфорной кислоты). Роль гидролиза в биохимических процессах. Гидролиз АТФ как универсальный источник энергии в организме.
Вопрос №3
Осмоляльность и осмолярность биологических жидкостей и перфузионных растворов. Гипо-, гипер- и изотонические растворы. Изотонический коэффициент. Понятия об изоосмии (электролитном гомеостазе).
Вопрос №4
При ожогах щелочами пораженный участок кожи сначала промывают водой, а затем нейтрализуют 1 %-ным раствором уксусной кислоты. Во сколько раз надо разбавить уксусную эссенцию (70 %-ный раствор уксусной кислоты) для приготовления 1 %-ного раствора? Сколько мл воды надо добавить к 5 мл эссенции для получения 1 %-ного раствора?
Вопрос №5
Рассчитайте константу гидролиза Кг бромида аммония. Вычислите рН и степень гидролиза h соли в 0,01 М растворе. и раствора (константа диссоциации (NH4ОН)= 1,76 ·10-5.
|
«Утверждаю»
Зав. кафедрой, профессор В.В.Хорунжий _______________________
|
Санкт-Петербургский государственный педиатрический медицинский университет
Кафедра общей и медицинской химии
|
Специальность
«Педиатрия»
|
Дисциплина «Химия»
|
Семестр 1
|
БИЛЕТ № 78
Вопрос №1 (Тест)
Если при увеличении температуры от 20 °С до 50 °С скорость реакции увеличилась в 8 раз, то температурный коэффициент равен
1) 2,67 2) 2 3) 3,67 4) 3
Диссоциация комплексного соединения с ионной внешней сферой в воде происходит
1) по типу сильного электролита 2) обратимо и ступенчато 3) на 50% 4) как у неэлектролита
Электролитом не является
1) КОН 2) азотная кислота 3) NaOH 4) этиловый спирт
Необратимому гидролизу (с образованием исходной кислоты и основания) подвергается
1) хлорид натрия 2) ацетат калия 3) сульфид алюминия 4) цианид натрия
Укажите, какая из приведенных смесей электролитов может проявлять буферные свойства?
1) NH2-CH2-COONa NH2-CH2-COOH 2) NaCl, NH2-CH2-COOH. 3) NaCl, NaOH 4) Na3PO4, NaOH
Чтобы записать выражение для константы равновесия, необходимо знать
1) стехиометрическое уравнение реакции с указанием агрегатных состояний участников
2) механизм прямой и обратной реакции
3) изменение энтальпии для реакции
4) кинетические уравнения для прямой и обратной реакции
К ПИВ относятся вещества, которые
1) не влияют на поверхностное натяжение на границе раздела фаз
2) не влияют на процесс адсорбции на границе раздела фаз
3) увеличивают поверхностное натяжение на границе раздела фаз
4) уменьшают поверхностное натяжение на границе раздела фаз
Потеря организмом воды приводит к
1) повышению осмотического давления 2) понижению осмотического давления
3) осмотическое давление остается постоянным 4) плазмолизу
Какой из электролитов окажет наибольшее коагулирующее действие на золь оксида марганца(IV) с положительно заряженными гранулами?
1) сульфид калия 2) ортофосфат натрия 3) сульфат алюминия 4) нитрат магния
Метод седиментации в центробежном поле используют для определения
1) осмотического давления 2) заряда частиц 3) молекулярной массы полимера 4) вязкости
Вопрос №2
Метод кислотно-основного титрования (метод нейтрализации). Основные положения. Применение. Титранты, стандартные и определяемые вещества. Кислотно-основные индикаторы и их характеристики. Кривые кислотно-основного титрования.
Вопрос №3
Явление осмоса и осмотическое давление. Закон Вант-Гоффа. Классификация растворов по осмотическим свойствам (изо-, гипер- и гипотонические растворы). Пазмолиз, гемолиз, тургор.
Вопрос №4
Для обработки ран используется 3 %-ный раствор пероксида водорода. Во сколько раз надо разбавить концентрированный (30 %-ный) раствор для приготовления 3 %-ного раствора? Сколько мл воды надо добавить к 10 мл концентрированного раствора?
Вопрос №5
Рассчитайте объемы растворов (мл) хлорида диэтиламмония и гидроксида диэтиламмония (рКд основания = 3,02) с одинаковыми молярными концентрациями эквивалентов, необходимых для приготовления 130 мл буферного раствора с pH, равным 11,2.
|
«Утверждаю»
Зав. кафедрой, профессор В.В.Хорунжий _______________________
|
Санкт-Петербургский государственный педиатрический медицинский университет
Кафедра общей и медицинской химии
|
Специальность
«Педиатрия»
|
Дисциплина «Химия»
|
Семестр 1
|
БИЛЕТ № 79
Вопрос №1 (Тест)
Для смещения равновесия в системе MgO(тв) + CO2(г) ⇄ MgCO3(тв); ∆rH° < 0 в сторону продуктов реакции необходимо
1) понизить давление 2) ввести ингибитор 3) ввести катализатор 4) понизить температуру
Формулы только слабых электролитов перечислены в ряду
1) CaCl2, H2Te, HI 2) H2CO3, NaCl, CH3COOH 3) HClO, KOH, MgSO4 4) NH4OH, H2S, H2SO3
Осмолярность плазмы крови в норме равна
1) 260-280 мОсм 2) 280-300 мОсм 3) 240-260 мОсм 4) 300-320 мОсм
Процесс гидролиза соли – это
1) растворение соли в воде 2) распад вещества на ионы
3) взаимодействие ионов соли с ионами воды 4) обменное взаимодействие ионов соли с молекулами воды
Укажите, какая из приведенных смесей электролитов может проявлять буферные свойства?
1) KNO3, HNO3 2) NH3·H2O, NaCl 3) HCOONa, HCOOK 4) NaH2PO4, Na2HPO4
Какие из следующих утверждений верны для реакций, протекающих в стандартных условиях? не надо
1) эндотермические реакции не могут протекать самопроизвольно
2) эндотермические реакции могут протекать при достаточно низких температурах
3) эндотермические реакции могут протекать при высоких температурах, если ΔS > 0.
4) эндотермические реакции могут протекать самопроизвольно
Величина потенциала кадмиевого электрода в с 0,1 М раствором Cd(NO3)2 при 298К (е°= -0,403 В) равна
1) -0,374 В 2) -0,432 В 3) -0,462 В 4) -0,344 В
К ПАВ относятся вещества, которые
1) не влияют на процесс адсорбции на границе раздела фаз
2) уменьшают поверхностное натяжение на границе раздела фаз
3) не влияют на поверхностное натяжение на границе раздела фаз
4) увеличивают поверхностное натяжение на границе раздела фаз
Формула мицеллы золя AgI в водном растворе AgNO3
1) (AgNO3) nNOn 2) [mAg+) nAgI] 3) {m(AgI)nAg+(n – x) NO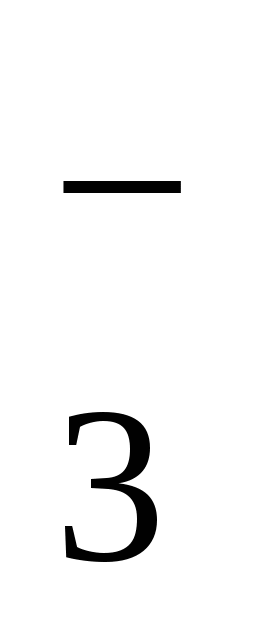 }x+x NO }x+x NO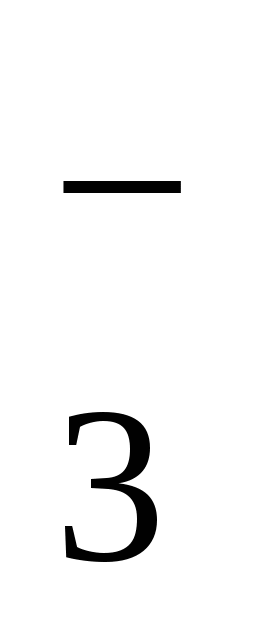 4) {m(AgI)nI–(n – x)K+}x- x I– 4) {m(AgI)nI–(n – x)K+}x- x I–
-
1) тиксотропией 2) денатурацией 3) коацервацией 4) синергизмом
Вопрос №2
Титриметрический анализ. Основные понятия: титрование, точка эквивалентности, индикаторы, титранты, стандартные вещества и растворы. Требования к реакциям в титриметрическом анализе. Классификация методов. Расчеты в титриметрическом анализе.
Вопрос №3
Особые случаи коагуляции. Коагуляция смесью электролитов: аддитивность, синергизм, антогонизм. Явление привыкания. Чередование зон устойчивости. Взаимная коагуляция.
Вопрос №4
Перманганатом калия можно лечить змеиные укусы (при отсутствии специальной сыворотки). В место укуса вводят шприцем примерно 1,0 мл 1 %-ного раствора KMnO4. Во сколько раз надо разбавить 10 %-ный раствор перманганата для приготовления 1 %-ного раствора? Сколько мл воды надо добавить к 15 мл 10 %-ного раствора, чтобы достичь 1%-ной концентрации? (ρ=1 г/мл)
Вопрос №5
Вдыхание нашатырного спирта (раствор NH4OH) вызывает учащение дыхания и повышение артериального давления. Рассчитайте рН и [OH-] 0,05 М раствора нашатырного спирта (Кд основания = 1,8·10-5).
|
«Утверждаю»
Зав. кафедрой, профессор В.В.Хорунжий _______________________
|
Санкт-Петербургский государственный педиатрический медицинский университет
Кафедра общей и медицинской химии
|
Специальность
«Педиатрия»
|
Дисциплина «Химия»
|
Семестр 1
|
БИЛЕТ № 80
Вопрос №1 (Тест)
Для смещения равновесия в системе CaCO3(тв) ⇄ CaO(тв) + CO2(г); ∆rH° > 0 в сторону продуктов реакции необходимо
1) увеличить давление 2) уменьшить температуру 3) ввести катализатор 4) увеличить температуру
Типу гибридизации валентных орбиталей комплексообразовыателя dsp2 соответствует ___ структура внутренней сферы комплексного соединения 1) тетраэдрическая 2) квадратная 3) линейная 4) октаэдрическая Повышение температуры кипения и понижение температуры замерзания раствора относительно растворителя пропорциональны
1) молярной концентрации 2) моляльной концентрации
3) молярной концентрации эквивалента 4) молярной доле растворенного вещества
Концентрация H+ не зависит от концентрации в растворе соли, формула которой
1) NH4CH3COO 2) KCN 3) NH4ClO4 4) Nа2S
Укажите, какая из приведенных смесей электролитов может проявлять буферные свойства?
1) NaOH, HC1 2) NH4CI,HC1 3) NaHCO3, CO2·H2O 4) КОН, К2СО3
Уравнение Нернста-Петерса е = е° + 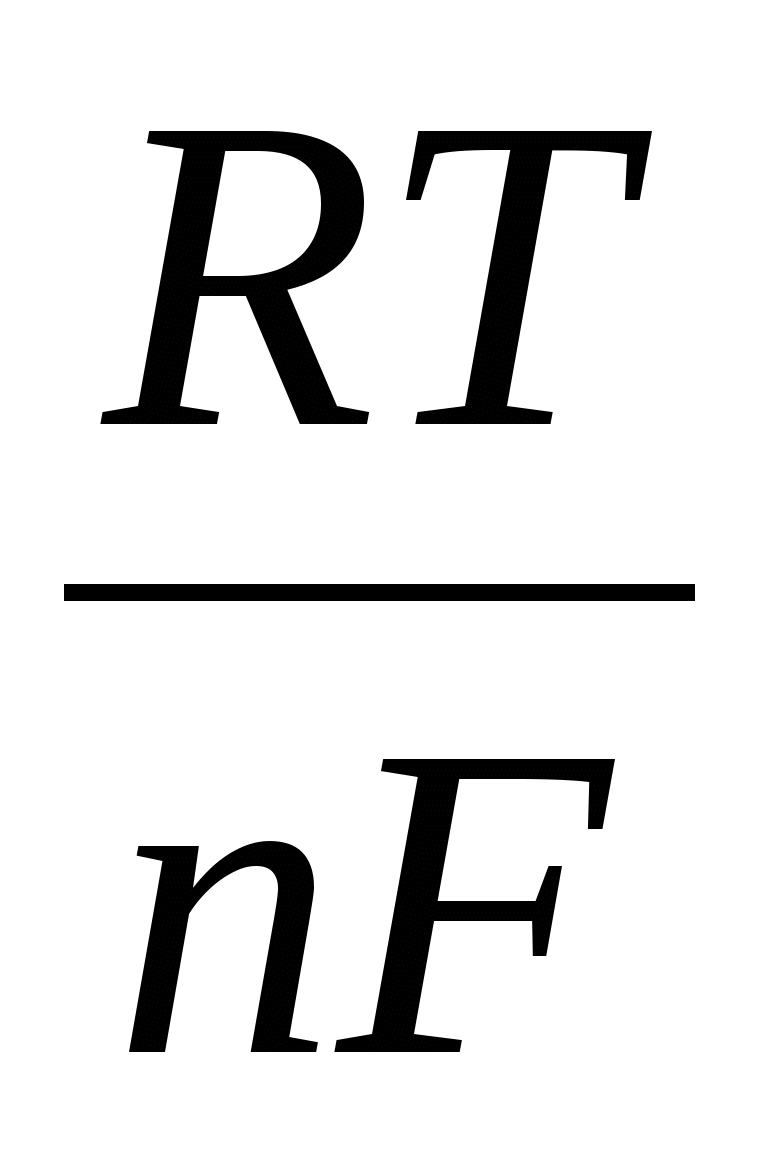 ln ln 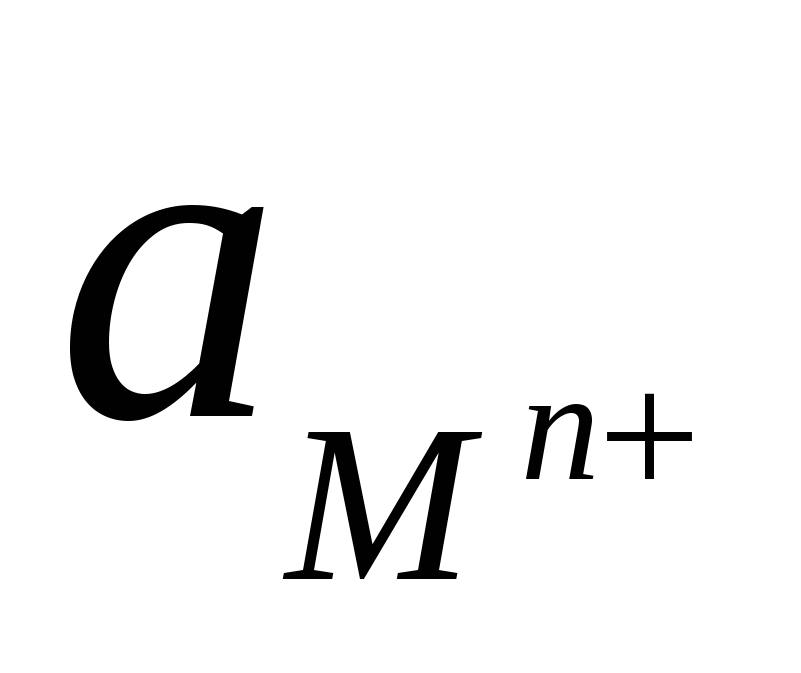 определяет величину _____ потенциала определяет величину _____ потенциала
1) мембранного 2) контактного 3) диффузионного 4) электродного
-
1) уменьшении поверхности и уменьшении поверхностного натяжения
2) увеличении поверхности и увеличении поверхностного натяжения
3) уменьшении поверхностного натяжения
4) увеличении поверхностного натяжения
По коэффициенту диффузии D можно определить
1) состав золя 2) вязкость золя 3) размер частиц 4) концентрацию золя
Коллоидные частицы Fe(OH)3 в водном растворе FeCl3
1) имеют заряд равный нулю 2) заряжаются отрицательно
3) заряжаются положительно 4) имеют заряд равный заряду катионов
Какой заряд имеет белок в растворе с рН = 6, если изоэлектрическая точка белка рI = 4,8?
1) отрицательный 2) положительный 3) нулевой 4) сначала положительный, затем отрицательный
Вопрос №2
Теория электролитической диссоциации. Сильные и слабые электролиты. Степень диссоциации. Равновесие в растворах слабых электролитов. Константа диссоциации (ионизации) слабого электролита. Закон разведения Оствальда.
Вопрос №3
Электрокинетический потенциал. Связь электрокинетического потенциала с зарядом гранулы, толщиной диффузного слоя. Факторы, влияющие на величину ξ-потенциала. Методы определения ξ-потенциала.
Вопрос №4
Для оттока раневого содержимого наружно используют 5 %-ный раствор хлорида натрия. Во сколько раз надо разбавить 20 %-ный раствор соли для приготовления 5 %-ного раствора? Сколько мл воды надо добавить к 20%-ному раствору, чтобы получить 80 мл 5 %-ного раствора NaCI?
Вопрос №5
Рассчитайте рН в растворе ацетата калия, если 2 л этого раствора содержат 98 г соли (Кд кислоты = 1,75 ·10⁻5)
|
«Утверждаю»
Зав. кафедрой, профессор В.В.Хорунжий _______________________
|
|
 Скачать 1.64 Mb.
Скачать 1.64 Mb.