тесты физика. Физика тесты. Сборник тестов по курсу общей физики иваново 2006 удк 53 Кудин Л. С. Сборник тестов по курсу общей физики
 Скачать 1.31 Mb. Скачать 1.31 Mb.
|
АТОМНАЯ ФИЗИКАПРИНЯТЫЕ ОБОЗНАЧЕНИЯ а - толщина R - постоянная Ридберга B - индукция магнитного по- ля с - скорость света S, P, D, r - радиус символы атомных термов F… - Е - энергия s, S- спин электрона (атома) е - элементарный заряд v- скорость g - фактор Ланде Z - порядковый номер элемента в периодической таблице Д.И. Менделеева ћ, h - постоянная Планка - -частица j, J - квантовое число полного момента импульса элек- трона/атома - приращение K, L, M…- символьное обозначение оболочки/серии - угол L - квантовое число орби- тального момента атома l - квантовое число орби- тального момента элек- трона - длина волны - магнитный момент Ml, Mlz- Ms, Msz- Mjz, Mjz- орбитальный момент им- пульса электрона и его проекция на ось z собственный момент им- пульса электрона и его проекция на ось z полный момент импульса электрона и его проекция на ось z Б - магнетон Бора J- полный магнитный момент атома S- спиновой магнитный момент m - масса, магнитное кванто- вое число, целое число - константа экранирования mе - масса электрона - время жизни N - число частиц - телесный угол n - концентрация, главное квантовое число, целое число - частота ТЕСТОВЫЕ ЗАДАНИЯАтом имеет размер порядка а) 10–6 см; б) 10 –8 см; в) 10 –10 см; г) 10 –13 см; д) 10 –15 см. Определению поставьте в соответствие математическое выражение. Определение Математическое выражение а) энергия водородоподобного атома в ⎛ Ze2 ⎞2d  стационарном состоянии 1) na⎜ 2⎟ 4 ⎝mv⎠ sin (/2) б) частота линии в спектре водородо- – meZ2e4 1  подобного атома 2) 2ћ2 n2  ћ2 2 в) формула Резерфорда 3) meZe2 n г) радиус стационарной боровской орбиты meZ2e4 ⎛1  ⎝ 4) 2ћ3 ⎜m2 1 ⎞ ⎠ – n2⎟ а) ; б) ; в) ; г) . Квантовым числам поставьте в соответствие значения, которые они принимают Квантовое число Значение а) главное квантовое число, n 1) 0, 1, 2, …, n – 1 б) орбитальное квантовое число, l 2) l+s, …, ⎢l–s⎪ в) магнитное квантовое число, ml3) – ½, + ½ г) спиновое квантовое число, ms4) 1, 2, 3, … д) квантовое число полного момента атома, mj5) – l, … 0, … l а) ; б) ; в) ; г) . д) . Кратность вырождения энергетического уровня с квантовым числом n равна а) 2n2; б) n 2; в) n. Максимальное число электронов в состоянии с n = 4 равно а) 8; б) 18; в) 32; г) 50. Значение, которое может принимать проекция момента импульса элек- трона на выбранное направление при заданном значении l, определяет- ся выражением а) lћ; б) – lћ; в) (2l + 1)ћ. Угловым моментам электрона (орбитальному, спиновому и полному) и их проекциям на направление оси zпоставьте в соответствие собствен- ные значения Угловой момент/проекция Значение  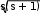 а) орбитальный момент импульса 1) ћ б) собственный момент импульса 2) ћm lв) полный момент импульса 3) ћ г) проекция орбитального момента импульса 4) ћmj а) орбитальный момент импульса 1) ћ б) собственный момент импульса 2) ћm lв) полный момент импульса 3) ћ г) проекция орбитального момента импульса 4) ћmj д) проекция собственного момента импульса 5) ћ l(l +1) д) проекция собственного момента импульса 5) ћ l(l +1)е) проекция полного момента импульса 6) ћm s. а) ; б) ; в) ; г) ; д) ; e) . Спектральной серии водородоподобного атома поставьте в соответст- вие формулу. Спектральная серия Формула а) Бальмера б) Брекета в) Лаймана г) Пфунда д) Пашена ⎛1 1) R⎜12 ⎝ ⎝ ⎛ 1 2) R⎜22 ⎝ ⎛ 1 3) R⎜32 ⎝ ⎛ 1 4) R⎜42 ⎝ ⎛ 1 5) R⎜52 – 1 ⎞ n2⎟ ⎠ n2⎟ – 1 ⎞ ⎠ n2⎟ – 1 ⎞ ⎠ n2⎟ – 1 ⎞ ⎠ n2⎟ – 1 ⎞ ⎠ (n = 2, 3, 4, …) (n = 3, 4, 5, …) (n = 4, 5, 6, …) (n = 5, 6, 7, …) (n = 6, 7, 8, …) а) ; б) ; в) ; г) . д) . Максимально возможная проекция момента импульса орбитального движения электрона, находящегося в атоме в d-состоянии, на направ- ление внешнего магнитного поля равна 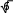 а) ћ; б) ћ ; в) 2ћ. а) ћ; б) ћ ; в) 2ћ.Чему равен момент импульса орбитального движения электрона, нахо- дящегося в атоме в р-состоянии? 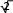 а) 0; б) ћ; в) ћ . а) 0; б) ћ; в) ћ .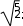 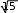 Терм атома 2Р3/2. Чему равен максимальный момент атома? Терм атома 2Р3/2. Чему равен максимальный момент атома?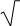 а) ћ ћ 3 2; б) в) ћ. 2 2. 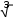 Электрон в атоме водорода находится р-состоянии. Максимально воз- можное значение полного момента импульса электрона равно Электрон в атоме водорода находится р-состоянии. Максимально воз- можное значение полного момента импульса электрона равно 2 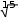 а) ћ а) ћ ; б) ћ ; в) ћ 2 Атом натрия, имеющий в своем составе одиннадцать электронов, мо- жет находиться в различных электронных состояниях: 1s 22s22p63s (I); 1s22s22p63p (II); 1s22s22p64s (III); 1s22s22p64p (IV); 1s22s22p63d (V); 1s22s22p65s (VI). Установите правильную последовательность состоя- ний в порядке возрастания энергии. а) I г) I Атомы лития, бериллия, бора и углерода находятся соответственно в состояниях 1s22s, 1s22s2p, 1s22s2p2, 1s22s22p2. Какие из перечисленных атомов находятся в возбужденном состоянии? а) Li; б) Be; в) B; г) C; д) Li, C; е) Be, B. Какие из приведенных утверждений называются правилами Хунда? низшей энергией обладает терм с наивысшей мультиплетностью, т.е. с высшим значением спина; атомные орбитали располагаются в последовательности возраста- ния суммы квантовых чисел (n + l), причем в группе уровней с данным значением (n + l) первыми следуют уровни с меньшим значением квантового числа n; из термов с одинаковой мультиплетностью низшей энергией обла- дает терм с высшим значением квантового числа L; термы атомов или ионов с четным числом электронов имеют не- четные мультиплетности; термы атомов или ионов с нечетным числом электронов имеют четные мультиплетности; при данном значении L и S низшей энергией обладает терм с мини- мальным J (=L – S), если подоболочка заполнена менее чем напо- ловину, и с максимальным J (=L + S), если подоболочка заполнена более чем наполовину. а) 1, 2, 3; б) 2, 4; в) 3, 5; г) 1, 3, 5. Мультиплетностью называется величина а) 2L + 1; б) 2J + 1; в) 2S + 1. Символ терма атома в состоянии с электронной конфигурацией 1s 22p3d запишется в виде а) 1P1; б) 3P2; в) 1D2; д) 3D3; е) 3F4. Какие из термов: 1S, 1P, 1D1, 3S, 3P, 3D не противоречат принципу Пау- ли? а) 1S; б) 1P; в) 1D; г) 3S; д) 3P; е) 3D. Какой из термов: 1S0, 3P0, 3P1, 3P2, 1D2 соответствует основному состоя- нию для конфигурации np2? а) 1S0; б) 3P0; в) 3P1; г) 3P2; д) 1D2. Основному состоянию атома бора B соответствует терм а) 2S1/2; б) 2P1/2; в) 2P3/2; г) 2D5/2; д) 4D7/2. Какой терм является основным для конфигурации np3? а) 2S1/2; б) 4S3/2; в) 2P3/2; г) 2D5/2. Сколько эквивалентных электронов находится в незаполненной подо- болочке атома, основной терм которого 3F2? а) 1; б) 2; в) 3; г) 4; д) 5. Определению физической величины поставьте в соответствие матема- тическое выражение. Определение Математическое выражение 1) а) момент импульса электрона e 2mec б) магнитный момент атома водорода 2) ћ 2 в) гиромагнитное отношение 3) evr г) магнетон Бора 4) mvr 2m д) ширина спектральной линии 5)eћ e а) ; б) ; в) ; г) ; д) . Физической величине поставьте в соответствие математическое выра- жение.  Физическая величина Математическое выражение а) орбитальный магнитный момент 1) – Б g Физическая величина Математическое выражение а) орбитальный магнитный момент 1) – Б gб) проекция орбитального магнитного момента атома на выбранное на- правление – 2БmS 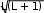 в) спиновой магнитный момент 3) – Б в) спиновой магнитный момент 3) – Бг) проекция спинового магнитного момента на выбранное направление 4) 1+ S(S+1)+J(J+1)–L(L+1) 2J(J+1) д) магнетон Бора 5) – БgmJ е) полный магнитный момент 6) – БmL 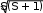 ж) проекция полного магнитного мо- мента на выбранное направление ж) проекция полного магнитного мо- мента на выбранное направление7) – 2Б 8) з) фактор Ланде eћ 2mec а) ; б) ; в) ; г) ; д) ; е) ; ж) ; з) . Энергия взаимодействия магнитного момента атома с внешним маг- нитным полем определяется выражением Эффект Пашена-Бака проявляется а) в слабом внешнем магнитном поле; б) в слабом внешнем электрическом поле; в) в сильном внешнем магнитном поле; г) в сильном внешнем электрическом поле. Какие из приведенных ниже утверждений справедливы? Аномальный эффект Зеемана наблюдается а) в том случае, когда исходные линии не имеют тонкой структуры, т.е. являются синглетными; б) в слабом внешнем магнитном поле при условии, что зеемановское расщепление уровней меньше мультиплетного расщепления; в) в случае, когда реализуется рассель-саундерская связь между орби- тальным и спиновым моментами импульса; г) в сильном внешнем магнитном поле, когда раз-рывается связь между орбитальным и спиновым моментами импульса, и они ведут себя не- зависимо друг от друга. Резонансные частоты спектра ЭПР лежат а) в области радиодиапазона; б) в ИК- области; в) в видимой области; г) в УФ- области. Утверждение: «в любом квантовом состоянии может находиться не бо- лее одного электрона» получило название а) принципа неопределенности; б) принципа суперпозиции состояний; в) принципа Паули; г) комбинационного принципа Ритца; д) принципа минимума энергии. На рисунке представлена схема спектра энергетических уровней на- трия. Какие из указанных переходов противоречат правилам отбора? S 2 1/2 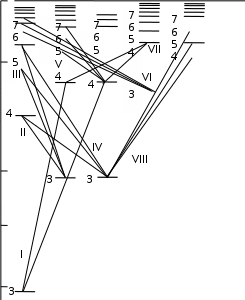 0 02P3/2 2P1/2 2D5/2 3/2 2F7/2 5/2 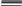 1 1 Энергия, эВ –2 –3 –4 –5 а) I, II; б) III, IV, VII; в) V; г) V, VI; д) V, VI, VIII. Эффектом Зеемана называется а) расщепление энергетических уровней энергии и спектральных ли- ний атома и других квантовых систем во внешнем магнитном поле; б) расщепление энергетических уровней энергии и спектральных ли- ний атома и других квантовых систем во внешнем электрическом поле; в) резонансное поглощение электромагнитной энергии веществами, содержащими парамагнитные частицы; г) избирательное поглощение электромагнитной энергии веществом, обусловленное ядерным парамагнетизмом; д) резонансное поглощение ядрами - излучения. Какие из приведенных ниже рисунков схематически отображают нор- мальный эффект Зеемана? B= 0 B 0 mJ 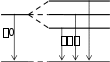 +1 +11 B= 0 B 0 mJ 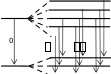 +2 +21D +1 P1 0 2 0 –1 –1 –2 1S 1P +1 0  0 00 a) 0 1  0+ 0 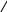 0 0 б) 0
–1 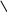 0+ 2P3 2P1 B= 0 B 0 mL ms mL+2ms 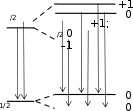 +1/2 +2 +1/2 +2+1/2 +1 –1 –1/2; +1/2 0 –1/2 –1 –1/2 –2 2S
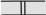 0 0 0 0+ в) +1/2 +1 –1/2 –1 B= 0 B 0 2P3/2 mJ g 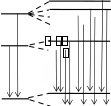 +3/2 +3/2+1/2 4/3 –1/2 –3/2 2P1/2 2S1/2 +1/2 –1/2 +1/2   –1/2 –1/22/3 2 Возбуждение K-серии Возбуждение L-серии 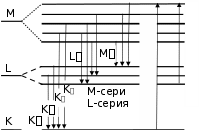 ристический спектр излучения. ристический спектр излучения. я a) mJ g l j 2 5/2 2 3/2 1 3/2 1 1/2 0 1/2 1 3/2 1 1/2 0 1/2 0 1/2 2P3/2 +3/2 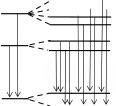 +1/2 4/3 +1/2 4/3–1/2 –3/2 +1/2 2P1/2 –1/2 2/3 2S1/2 б) 1/2 + –1/2 2 1 см 0 50000 10000 в) 113 4 n 5 13,53 13 12 11 10 9 8 3 2 7 6 5 4 3 2 1 1 0  Энергия, эВ Энергия, эВ |
