Сероуглерод и нитрометан
 Скачать 87.39 Kb. Скачать 87.39 Kb.
|
|
16.Сероуглерод и нитрометан. Области применения. Свойства данных растворителей. Пиридин. Особенности работы с данным растворителем. Перегонка пиридина. Сероуглерод и нитрометан Исключительная воспламеняемость Поэтому практически не применяется При открытии бутылки может сразу загореться из-за наличия кислорода в воздухе Нитрометан загорается от тепла руки Переливают в атмосфере аргона Сероуглерод применение 1. Хорошо растворяет жиры, масла, смолы, каучук, используют как экстрагент; растворяет серу, фосфор, иод, нитрат серебра. 2. Большая часть (80 %) производимого сероуглерода идёт в производство вискозы — сырья в производстве вискозного волокна («искусственного шелка»). Его применяют для получения различных химических веществ (ксантогенатов, четырёххлористого углерода, роданидов). Нитрометан применение 1.Основное применение нитрометана — в качестве растворителя (например, эфироцеллюлозных лаков, виниловых полимеров, цианоакрилатов (суперклей), некоторых красок), для экстракции ароматических углеводородов, в производстве хлорпикрина, некоторых взрывчатых веществ. 2.В качестве реактивного топлива 3. Также используется как добавка к топливу для калильных двигателей внутреннего сгорания (например у радиоуправляемых моделей). 4.В качестве топлива для гоночных болидов — «nitro», «Top fuel» (драгстеров). пиридин Пиридин: бесцветная, маслянистая жидкость, резко неприятная на запах (смесь приторного кленового и миндального сиропов) Ядовит. Обладает общим токсическим действием. Пиридин высушивают длительное время (12 часов) над гранулами КОН, затем перегоняют на ВаО. Очень гигроскопичен: образует азеотроп с водой и кипит при 93оС) 17.Осушающие агенты. Свойства осушающих агентов. Ряд осушающих агентов. Молекулярные сита. Виды молекулярных сит. Состав определенного вида молекулярных сит. Области их применения. Осушающие агенты P2O5 > ВаО > CaH2 > Mg(ClO4)2 > СаО > MgO > КОН > H2SO4 > CaSO4 > Al2O3 > silicagel > NaOH > CaCl2 > СuSO4 > Na2SO4 Молекулярные сита - кристаллические алюмосиликаты, имеющие трёхмерную структуру из тетраэдров оксида кремния и оксида алюминия и характеризующиеся точным и однородным размером пор. Поры в молекулярных ситах достаточно велики, чтобы пропускать небольшие молекулы, но в то же время они задерживают более крупные молекулы, что определило их использование в качестве осушителей и адсорбентов. Для восстановления активности молекулярных сит необходимо прогреть их либо продуть газом, чтобы удалить сорбировавшиеся вещества. Существенным фактором в этом процессе является температура сит. Молекулярные сита 3 Å требуют температуры 175—260 °С. Однако при такой температуре может происходить полимеризация молекул ненасыщенных сорбатов, если таковые присутствовали в очищаемом материале, поэтому рекомендуется постепенное повышение температуры, чтобы дать ненасыщенным молекулам возможность покинуть сита в более низком интервале температур. После прогрева сит требуется охлаждение, что удобно осуществлять, пропуская ток того же газа, но без подачи теплоты Молекулярные сита 3 Å Молекулярные сита 3 Å имеют состав 0,6 K2O : 0,40 Na2O : 1 Al2O3 : 2,0 ± 0,1 SiO2 : x H2O. Их получают путём замены ионов натрия в ситах 4 Å на ионы калия, что уменьшает эффективный размер пор. Такие сита находят применение в промышленной осушке углеводородов, включая крекинг-газ, пропилен, бутадиен, ацетилен. Также при их помощи осушивают полярные жидкости, такие как этанол и метанол, и удаляют воду и аммиак из потока N2/H2. 4 Å Молекулярные сита 4 Å имеют состав 1 Na2O : 1 Al2O3 : 2,0 ± 0,1 SiO2 : x H2O. Такие сита применяются для статической осушки газообразных или жидких систем, например, при упаковке лекарств и неустойчивых химикатов. Данные сита поглощают диоксид углерода, диоксид серы, сероводород, этилен, этан и пропилен. Эти сита считаются универсальным осушителем для полярных и неполярных растворителей. 5 Å Молекулярные сита 5 Å имеют состав 0,8 CaO : 0,2 Na2O : 1 Al2O3 : 2,0 ± 0,1 SiO2 : x H2O. Такие сита получают путём замены ионов натрия в ситах 4 Å на ионы кальция. Они применяются для разделения алканов нормального строения от разветвлённых и циклических алканов, а также для удаления сероводорода, меркаптанов и диоксида углерода из природного газа. 13X Молекулярные сита 13X имеют состав 1 Na2O : 1 Al2O3 : 2,8 ± 0,2 SiO2 : x H2O.Такие сита применяются для промышленной осушки газов и удаления из них сероводорода и меркаптанов. 18. Хроматография. Понятие хроматографии. История возникновения хроматографии. Классификация хроматографических методов. Достоинства и недостатки метода хроматографии. Хроматографическим методом- называется такой физико-химический метод разделения смесей, при котором компоненты разделяемой смеси распределены между двумя фазами, одна из которых является неподвижной фазой с большой поверхностью контакта, а другая фаза – поток, фильтрующийся через неподвижный слой. История: 1. В 1900-1901 гг. Михаилу Семеновичу Цвету удалось разделить сложную смесь растительных пигментов, пропуская петролейно-эфирную вытяжку из листьев растений через стеклянную колонку, заполненную порошкообразным карбонатом кальция. Смесь делилась на отдельно окрашенные зоны, как лучи света в спектре, давая возможность качественного и количественного определения. Такую картину он назвал хроматограммой, а методику – хроматографической. 2. В 1941 г. А.Дж.П.Мартин и Р.Л.М.Синг разработали новую разновидность хроматографии, в основу которой легло различие в коэффициентах распределения разделяемых веществ между двумя несмешивающимися жидкостями. Метод получил название «распределительная хроматография». 3. В 1947 году супруги Гапон и Ф.М. Шемякин нашли, что в основу хроматографического метода можно положить принцип ионного обмена для ионных веществ. Так возникла ионообменная хроматография. В 1948 году Гапоны показали, что если через слой сорбента пропускаются вещества, способные образовывать осадки, различающиеся растворимостью, то их можно разделить (осадочная хроматография). 4. В 1952 году Джеймс и Мартин предложили вариант разделения, основанный на распределении веществ разделяемой смеси между жидкостью и газом. Так возникла газо-жидкостная хроматография. 5. В 1951 году Жуховицкий А.А., Айвазов Б.В. предложили хроматермографию (один из вариантов газовой хроматографии, при которой для улучшения разделения смеси газов одновременно с движением подвижной фазы — газа, воздействуют на сорбент и разделяемую смесь движущимся температурным полем, имеющим определенный градиент по длине) 6.В 1957 году Голей предложил капиллярную хроматографию. Классификация хроматографических методов: 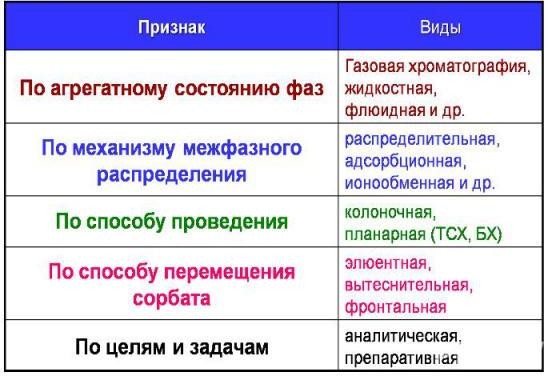 В зависимости от характера неподвижнойфазы: Адсорбционная хроматография: неподвижная фаза – твердое пористое вещество; подвижная фаза – газ или жидкость; Распределительная хроматография: неподвижная фаза – жидкость, которая находится на поверхности твердого носителя; подвижная фаза – газ или жидкость. По механизму разделения веществ: ГЕЛЬ-ФИЛЬТРАЦИЯ ИОНООБМЕННАЯ АФИННАЯ По геометрии сорбционного слоя неподвижной фазы Плоскослойная хроматография: ТСХ (тонкослойная хроматография и бумажная хроматография) Колоночная хроматография В зависимости от агрегатного состояния: 1) газо-твердофазную хроматографию, или газоадсорбционную хроматографию; 2) газо-жидкостную хроматографию (газо-жидко-твердофазную); 3) жидко-твердофазную хроматографию; 4) жидко-жидкофазную хроматографию; 5) флюидно-твердофазную хроматографию; 6) флюидно-жидко-твердофазную хроматографию.
В основе первых двух лежат сорбционные процессы, а двух последующих – распределительные. Достоинства и недостатки метода хроматографии: универсальность в смысле объектов анализа, возможность разделения веществ, близких по свойствам, отсутствие химических изменений в разделяемых веществах, высокая чувствительность. Общие недостатки По сравнению с другими методами (спектрофотометрия, колориметрия, гравиметрия), при проверке хроматографических методов мы обычно устанавливаем больший интервал точности, точности и неопределенности, что означает, что хроматографические методы имеют более низкую точность и точность и больший интервал неопределенности результатов анализа. Это компромисс между использованием динамического процесса разделения с онлайн-детекцией - это приводит к большей вариабельности результатов. Кроме того, по сравнению с другими методами, это требует более длительного периода обучения персонала лаборатории. Это неудивительно, учитывая более высокую сложность системы. Другим недостатком может быть стоимость приборов и их эксплуатации. Стоимость приобретения некоторых приборов с переносом может достигать 1 миллиона евро. недостатки газо-адсорбционной хроматографии сильное удерживание полярных и высококипящих веществ ⇒ большое время анализа, низкие, широкие пики возможность протекания каталитических процессов на поверхности сорбента сложность получения однородных сорбентов ⇒ плохая воспроизводимость времен удерживания, асимметричность хроматографических пиков Недостатки ГЖХ Можно определить только летучие соединения Нельзя определять термолабильные вещества Иногда требуется длительная подготовка |
