Сложные эфиры и жиры - конспект. Сложными эфирами называют производные карбоновых кислот, в которых атом водорода карбоксильной группы замещён углеводородным радикалом
 Скачать 163.59 Kb. Скачать 163.59 Kb.
|
|
Сложные эфиры и жиры Понятие о сложных эфирах
Способы получения и химические свойства сложных эфиров Процесс получения сложных эфиров носит название реакции этерификации. Эта реакция с использованием общих формул описывается уравнением  Именно реакцией этерификации в 1759 г. в результате взаимодействия уксусной кислоты с этиловым спиртом был получен первый сложный эфир — этиловый эфир уксусной кислоты: Обратите внимание на то, как строится название сложного эфира. Оно состоит из четырёх слов, указывающих на название углеводородного радикала и исходной кислоты. Например, продукт взаимодействия муравьиной кислоты с метиловым спиртом — метиловый эфир муравьиной кислоты: 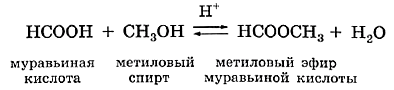 Катион водорода в схеме реакции указывает на то, что реакция этерификации протекает в присутствии кислоты в качестве катализатора. Сложные эфиры с небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости с характерным, часто приятным запахом. Они нерастворимы в воде, но прекрасно растворяют различные органические вещества. Реакции этерификации обратимы. В присутствии кислот сложные эфиры разлагаются водой — гидролизуются, что можно рассматривать как реакцию, обратную их получению: В присутствии щелочей гидролиз сложных эфиров необратим, так как образующаяся кислота связывается щёлочью с образованием соли, неспособной вступать в реакцию со спиртом: Нахождение в природе и применение сложных эфиров Сложные эфиры широко распространены в природе. Неповторимый аромат цветов и фруктов часто обусловлен присутствием веществ именно этого класса. Сложные эфиры с большой молекулярной массой представляют собой твёрдые вещества — воски. Пчелиный воск — это смесь сложных эфиров, образованных карбоновыми кислотами и спиртами с длинными углеводородными цепями. Синтетические сложные эфиры используют в пищевой промышленности в качестве добавок для придания фруктовых запахов напиткам и кондитерским изделиям. Благодаря хорошей растворяющей способности сложные эфиры входят в состав растворителей лаков и красок. Жиры
 Жиры образуются при взаимодействии глицерина и высших карбоновых кислот: 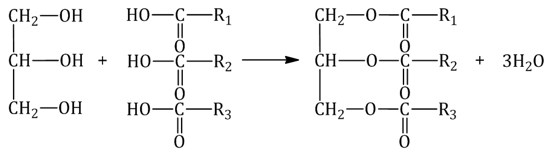
Номенклатура жировОбщее название жиров – триацилглицерины (триглицериды). Существует несколько способов назвать молекулу жира. Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:  Физические свойства жировЖиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
Химические свойства жиров1. Гидролиз (омыление) жиров Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов. 1.1. Кислотный гидролизПод действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
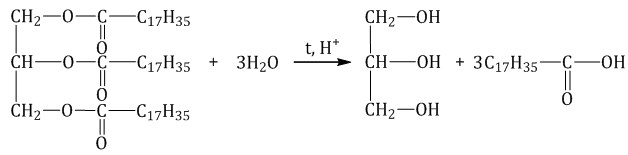 1.2. Щелочной гидролиз — омыление жировПри щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
 2. Гидрирование (гидрогенизация) ненасыщенных жировГидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира. При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
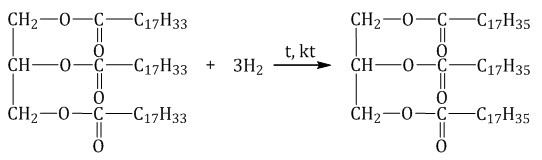
3. Мыло и синтетические моющие средстваПри щелочном гидролизе жиров образуются мыла – соли высших жирных кислот. Стеарат натрия – твёрдое мыло. Стеарат калия – жидкое мыло. Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca2+ и Mg2+ дают с высшими кислотами нерастворимые в воде соли.
Поэтому наряду с мылом используют синтетические моющие средства. Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты. Спирт реагирует с серной кислотой с образованием алкилсульфата. Далее алкилсульфат гидролизуется щелочью: Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках. | ||||||||||||||||||||||
