Оксокислоты. Способы получения оксокислот Получение оксокислот
 Скачать 173 Kb. Скачать 173 Kb.
|
|
Способы получения оксокислот
α-оксокислоты получают тремя основными способами:
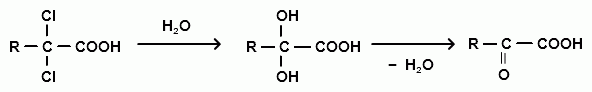
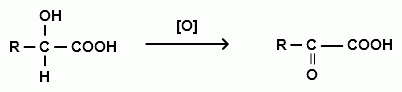
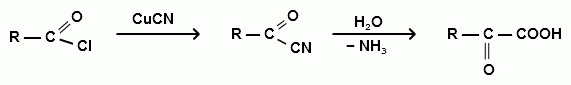 ацилхлорид α-оксонитрил α-оксокислота
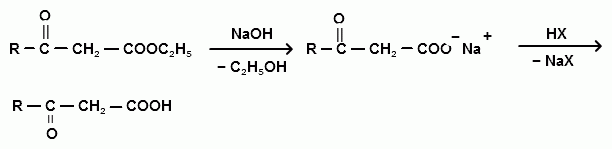
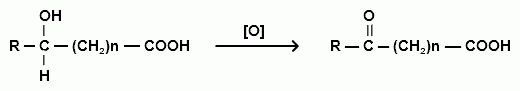 n = 2 (γ-), n = 3 (δ-) ХИМИЧЕСКИЕ СВОЙСТВА ОКСОКИСЛОТ
Для α-оксокислот характерны все реакции карбоновых кислот и карбонильных соединений. Только взаимное влияние карбоксильной и карбонильных групп увеличивает их реакционную способность. Типичными реакциями α-оксокислот являются:
Реакция декарбоксилирования происходит под действием разбавленной серной кислоты при слабом нагревании с получением альдегидов, а реакция декарбонилирования при нагревании с концентрированной серной кислотой с получением карбоновых кислот: 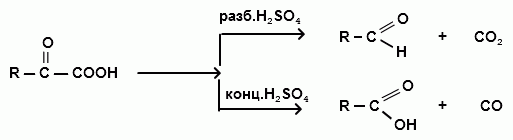
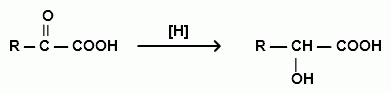
Глиоксалевая кислота вступает в реакцию Канниццаро: 
При нагревании все β-оксокислоты распадаются с выделением СО2 и образованием карбонильных соединений: 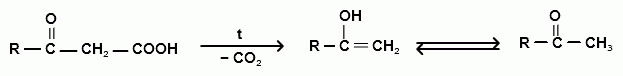
γ- и δ- оксокислоты обладают всеми свойствами карбоновых кислот и карбонильных соединений, но одновременно для них возможны также реакции внутримолекулярной циклизации: 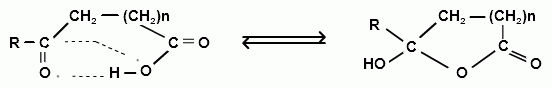 n = 1,2 АЦЕТОУКСУСНЫЙ ЭФИР (этиловый эфир ацетоуксусной кислоты) 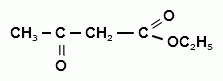 Способы получения
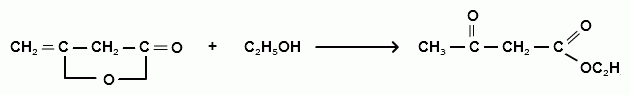
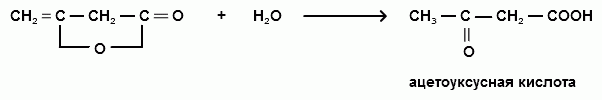
Ацетоуксусный эфир образуется при конденсации двух молекул этилацетата под действием этилата натрия:  ХИМИЧЕСКИЕ СВОЙСТВА
Ацетоуксусный эфир – классический пример соединения, способного к кето-енольной таутомерии. Одна из изомерных форм ацетоуксусного эфира содержит кетогруппу (кетоформа), другая – гидроксильную группу у ненасыщенного атома углерода (енольная форма):  92,3% 7,7% Кето-енольная таутомерия относится к прототропной таутомерии, так как она сопровождается переносом протона. Такое превращение возможно из-за наличия в кетонной форме СН2-группы, расположенной между двумя СО-группами, в результате чего атомы водорода в этой метиленовой группе приобретают значительную подвижность. В обычных условиях, при комнатной температуре, ацетоуксусный эфир содержит 92,3% кетонной формы и 7,7% - енольой формы. Енольная группировка энергетически менее выгодна, чем кетонная. Однако в данном случае при образовании енола возникает:
Выигрыш энергии за счет этих двух факторов компенсирует в некоторой степени затрату энергии на образование енола, благодаря чему склонность к енолизации возрастает. В химическом отношении ацетоуксусный эфир способен давать реакции как для кетонной, так и для енольной формы.
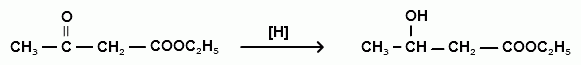 этиловый эфир β- гидроксимасляной кислоты
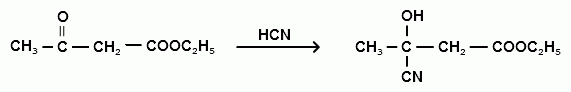 циангидрин кетоформы ацетоуксусного эфира
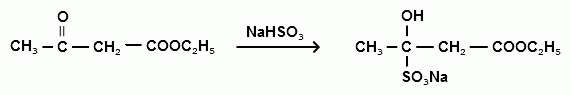 гидросульфитной производное кетоформы ацетоуксусного эфира
При взаимодействии с гидроксиламином образуется оксим кетоформы ацетоуксусного эфира, который является неустойчивым и, теряя молекулу спирта, легко превращается в метилоксазолон: 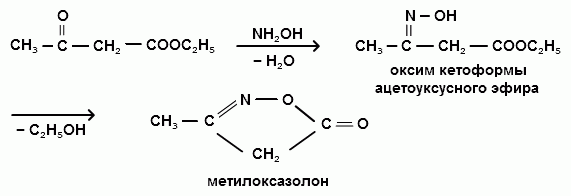
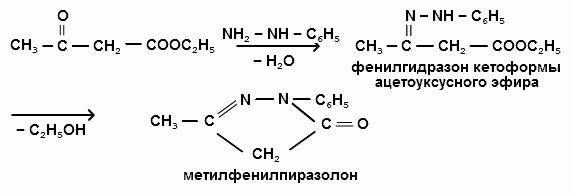
Для ацетоуксусного эфира характерна качественная реакция на енолы: при взаимодействии с раствором хлорида железа (Ш) FeCl3 происходит образование сложных комплексных солей железа, имеющих красно-фиолетовую окраску.
Присоединение брома происходит быстро на холоду. Образующийся дибромид, отщепляя бромистый водород, превращается в производной кетонной формы – α –бромацетоуксусный эфир: 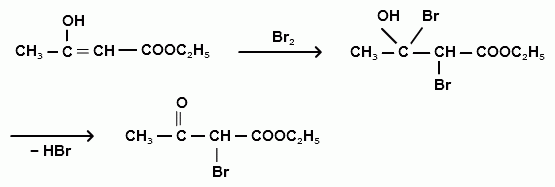 α – бромацетоуксусный эфир
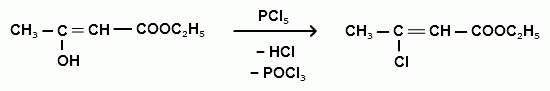 β- хлоркротоновый эфир
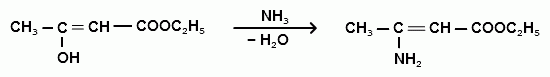 β- аминокротоновый эфир
Действием ацетилхлорида получают соответствующее О-ацетилпроизводное ацетоуксусного эфира: 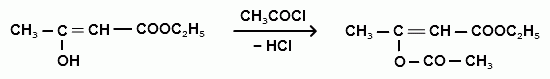 О-ацетилпроизводное ацетоуксусного эфира
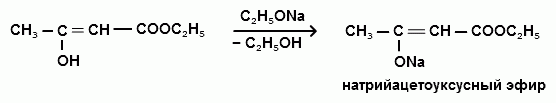 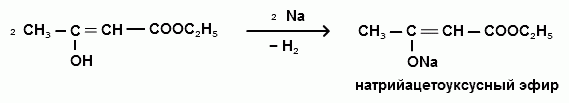 НАТРИЙАЦЕТОУКСУСНЫЙ ЭФИР Натрийацетоуксусный эфир имеет широкое применение в органическом синтезе для получения различных соединений. При алкилировании и ацилировании натрийацетоуксусного эфира наблюдаются реакции с переносом реакционного центра. В результате вместо ожидаемых О-алкил или О-ацилпроизводных ацетоуксусного эфира образуются соответствующие С-алкил или С-ацилпроизводные: 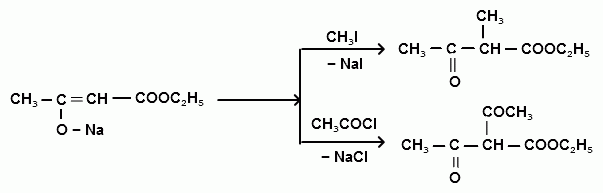 Алкилированные и ацилированные производные ацетоуксусного эфира представляют интерес в качестве исходных веществ для дальнейших превращений. Большое значение имеют реакции кетонного и кислотного расщепления этих соединений, а также расщепление самого ацетоуксусного эфира.
С-алкильных и С-ацильных производных. Кислотное расщепление осуществляется под действием концентрированного спиртового раствора щелочи (NaOH, KOH) и приводит к образованию различных карбоновых кислот – уксусной кислоты и ее гомологов, а также кетокислот:
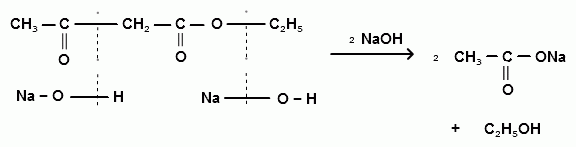
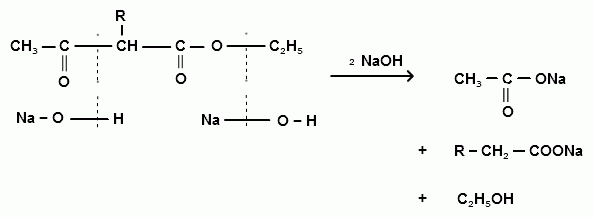
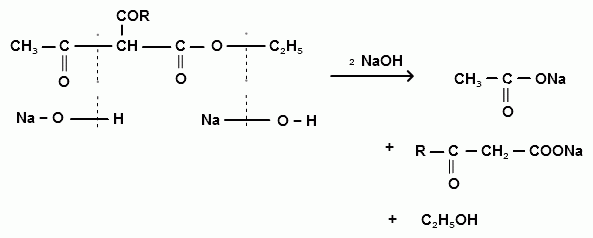
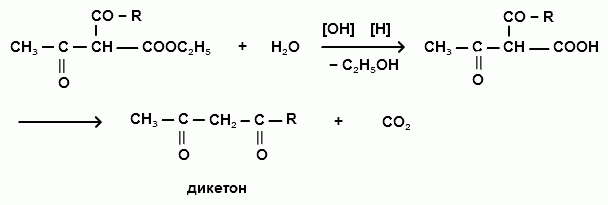
С-алкильных и С-ацильных производных. Кетонное расщепление осуществляется действием разбавленных растворов щелочей или кислот. Вначале происходит омыление эфира, а затем декарбоксилирование образующейся β- кетокислоты с образованием ацетона и его гомологов, а также дикетонов:
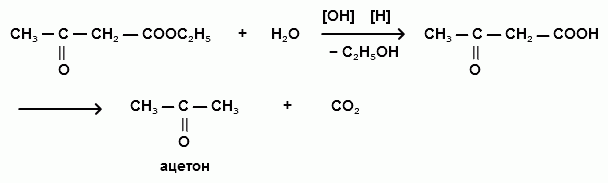
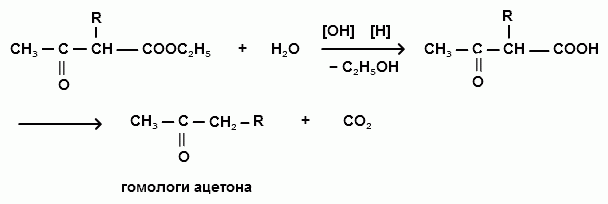
 |
