Химические покрытия. Тема Лекция. Химическое нанесение покрытий. Химические покрытия. Природа процесса химического нанесения металлических покрытий на детали металлокерамических корпусов.
 Скачать 227.44 Kb. Скачать 227.44 Kb.
|
|
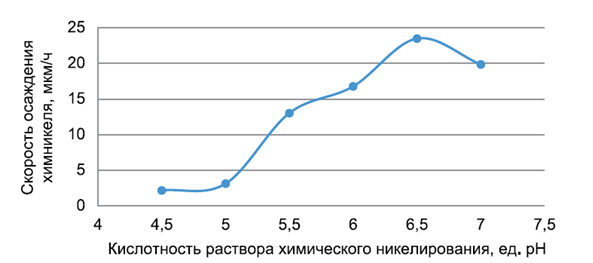
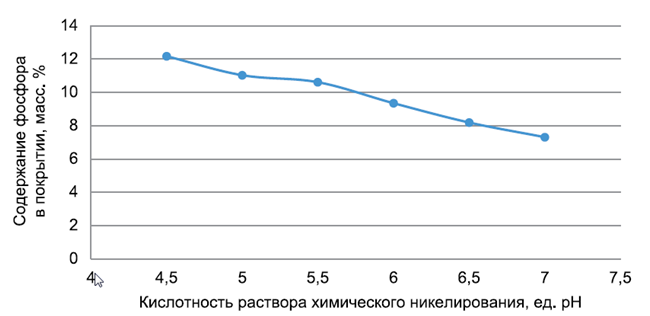
Тема 2. Лекция. Химическое нанесение покрытий. Химические покрытия. Природа процесса химического нанесения металлических покрытий на детали металлокерамических корпусов. Технология нанесения химических покрытий, основные технологические параметры. Химические покрытия Способ химического нанесения покрытий, т. е. без пропускания внешнего электрического тока, основан на восстановлении ионов металла на каталитически активной поверхности металлического или неметаллического электрода восстановителем, находящимся в растворе. Покрываемая поверхность может быть первоначально неметаллической, непроводящей; возможность нанесения покрытий на полимерные материалы, стекло, керамику и другие диэлектрики, а также на полупроводниковые материалы. Химическим способом могут быть восстановлены ионы никеля, кобальта, железа, хрома, кадмия, олова, палладия, платины, меди, серебра, золота, родия, рутения. Химическим осаждением можно получить как чистые металлы, так и сплавы металлов с неметаллическими компонентами, входящими в состав восстановителей: углеродом, фосфором, бором, а также сплавы двух металлов с этими элементами. Особое место занимают сплавы никель– фосфор (Ni-P), получаемые при гетерогенном каталитическом восстановлении никеля ионами гипофосфита (H2PO2- ). Химико-каталитическое, или электрокаталитическое, осаждение металлов осуществляется в результате передачи электронов ионам выделяемогометалла от присутствующего в растворе химического восстановителя. Этотпроцесс происходит на поверхностиизделия, которой предварительно придают каталитические свойства; в противном случае образуется порошок металла, распределенный повсему раствору. Чтобы обеспечить локализацию выделения компактногослоя металла на требуемой поверхности и непрерывность этого процесса,требуется, чтобы реакция восстановления металла была автокаталитической. Слой восстановленного металла должен быть способен катализировать дальнейший процесс. Именно потому, что поверхностьпостоянно обновляется, процесс приобретает черты автокаталитического ипокрытие можно наносить вплоть до значительной толщины. Например, по отношению к реакции химического никелирования каталитически активными металлами являются никель, палладий, железо, кобальт. Как и при электроосаждении, так и при химико-каталитическим осаждении возникает разность электрических потенциалов металл – раствор. Именно эта разность потенциалов, наряду с температурой и составом раствора, определяет скорость процесса нанесения покрытия и толщину покрытия. Процесс химической металлизации характеризуется основными реакциями восстановления ионов металла, находящихся в растворе, и окислением восстановителя, также присутствующего в растворе, на каталитически активной поверхности электрода. Химическое восстановление часто основано на простых окислительно-восстановительных реакциях типа: M n+ + R = M + Rn+, где R специально подобранный восстановитель. В качестве восстановителей могут быть использованы: гипофосфит натрия, формальдегид, гидразин, гидразинборан, диметиламин- и диэтиламинбораны. Потенциалы восстановления этих соединений в щелочной среде отрицательнее, что позволяет восстанавливать ионы металлов с достаточно высокими отрицательными значениями стандартных потенциалов. Помимо основных реакций протекают обратные реакции: ионизация осажденного металла с переходом его ионов в раствор и восстановление окисленных продуктов. Процесс осложнен окислением восстановителя с образованием продуктов различного химического состава и их химическим взаимодействием с водой, гидроксильными и гидроксониевыми ионами; на электроде возможно протекание параллельной реакции разряда-ионизации водорода. При металлизации металлов (медь, латунь, бронза, платина, серебро, золото), имеющих более положительные потенциалы по сравнению с никелем, поверхность которых не обладает каталитической активностью, необходимо сместить их потенциал в отрицательную сторону для начала процесса. Это достигается приведением их в контакт при погружении в раствор с более отрицательным металлом (никель, железо, алюминий) или кратковременной катодной поляризацией в растворе металлизации. Потенциал электроположительного металла также можно сместить в отрицательную сторону, вводя в раствор металлизации лиганды. Например, для химического никелирования меди может быть использован раствор, содержащий хлорид аммония. На поверхности металлов перед металлизацией также можно сформировать фосфорсодержащую пленку при их катодной поляризации в гипофосфитном растворе. Подобная пленка, содержащая фосфор, при внесении в раствор химического никелирования окисляется, в результате чего происходит восстановление никеля и поверхность приобретает каталитическую активность. Таким же методом можно активировать медь, платину, вольфрам, молибден, марганец, свинец, олово. Реакции химической металлизации обычно проводят при высоких температурах, при комнатных температурах реакция практически не протекает. Это указывает на то, что скорость металлизации лимитируется скоростью гетерогенных химических реакций, протекающих на каталитически активной поверхности. Преимущества метода химической металлизации без использования внешнего источника тока следующие: - получение равномерных покрытий на сложнопрофилированных изделиях; покрытия можно получать внутри полостей, куда затруднен подвод электрического тока. так как скорость химического осаждения равномерна на всех участках поверхности; - возможность нанесения слоев металла значительной толщины и с высокой прочностью сцепления. Осадки, полученные методом химической металлизации, могут обладать также рядом функциональных свойств: - повышенной микротвердостью; - коррозионной устойчивостью; - магнитными характеристиками, которые не могут быть достигнуты способом электроосаждения. Недостатки метода химической металлизации следующие: - частая замена растворов для химической металлизации; -сравнительно дорогие реактивы и достаточно сложное оборудование для проведения процесса; - снижение скорости процесса осаждения металла по мере эксплуатации раствора; -высокая температура проведения процесса; - большие затраты на нейтрализацию и регенерацию отработанных растворов. - сам технологический процесс химической металлизации является более сложным, чем электроосаждение металла, он состоит из большего числа операций, требует более строгого регулирования параметров: температуры, рН растворов, времени выдержки при промывке; растворы для химической металлизации недостаточно стабильны в работе, а процесс протекает при повышенной температуре и с невысокой скоростью. Несмотря на недостатки метода и его высокую себестоимость, зачастую он является единственно возможным для нанесения равномерных покрытий на металлы и диэлектрики, а также на сложнопрофилированные изделия. Химическое никелирование Свойства, назначение и получение никелевых покрытий Никелирование – это обработка поверхности материалов путем их покрытия слоем никеля. Обычно никелевый слой имеет толщину в пределах от 1 до 50 мкм. Никелированная поверхность имеет эстетичный внешний вид, покрытие может быть сатинированным, матовым или блестящим. Никелевое покрытие хорошо полируется, возможна сварка никелированной детали. Недостатком никелевого покрытия является высокая восприимчивость к соединениям серы и аммиаку, а также неустойчивость к ударным воздействиям. Никелевое покрытие относительно твердое, износостойкое, электропроводное. Области применения деталей с никелевым покрытием зависят от того, используется ли никелевое покрытие в качестве финишного или же выступает подслоем (подложкой) для нанесения других гальванических покрытий. Никелевое покрытие используют как самостоятельное для защиты от коррозии электрических контактов или механизмов, эксплуатирующихся во влажной среде, а также в качестве покрытия под пайку или в декоративных целях. Никелевое покрытие служит барьерным слоем под покрытия золотом, серебром, сплавом олово-свинец и другими металлами, предотвращая диффузию меди, цинка, железа и других металлов. Черное никелевое покрытие ( c коэффициентом отражения до 20%) применяется для придания деталям специальных оптических и декоративных свойств. Возможность восстанавливать никель гипофосфитом известна с 1844 года и установлена известным химиком Вюрцем. В результате восстановления никеля гипофосфитом на покрываемой поверхности выделяются сплавы Ni-P, содержащие от 1 до 15 масс. % фосфора, а иногда и больше. В процессах химико-каталитического никелированияприменяется гипофосфорная соль натрия NaH2PO2·H2O . Механизм процесса восстановления Ni2+гипофосфит-ионами довольно сложен. Электроны от восстановителя передаются не непосредственно окислителю, а переходят сначала в объем свежеосажденного сплава, компенсируя затрату электронов на восстановление никеля (фактически взамен внешнего источника электричества).При этом часть фосфора (Р+1) из H2PO-2 окисляется до фосфита H2PO- 3(P +3), другая часть фосфора восстанавливается – переходит в элементарную форму Р со степенью окисления нуль.Следствием этого и является результат процесса в целом – образованиетвердой фазы в виде не чистого никеля, а его сплава с фосфором. Часть гипофосфита, таким образом, включается в состав покрытия в виде элементарного фосфора (это наименьшая часть), часть расходуется на восстановление никеля и еще одна часть – на выделение водорода, а сам он при этом превращается в фосфит (H2PO-3), накапливающийся в растворе. Такое соосаждение неметалла в общем случае не является обязательным: так, азотсодержащиевосстановители (например, гидразин) дают чистый никель. Итак, при осаждении никель-фосфорного сплава одновременно, с одинаковой скоростью – и на одной и той же поверхности, – происходят два типа процессов: окисление восстановителя и восстановлениеметалла, водорода и фосфора. Они относятся к типу сопряженныхэлектрохимических процессов, при которых на электроде автономно,в процессе функционирования системы, устанавливается стационарный электродный потенциал и определенная скорость сопряженныхпроцессов. Скорости анодного процесса(перенос электронов на каталитической поверхности) выделения никеляпроисходят ниже предельной диффузионной скорости, особенно учитывая интенсивное выделение водорода, которое перемешивает раствор и снижает толщину диффузионного слоя. Значительная роль кинетических ограничений скорости приводит к тому, что органические кислоты и другие добавки, а также изменениярН и т. д. сильно влияют на скорость процесса выделения сплава никель –фосфор: в диффузионном режиме этого бы не было. Напротив, наблюдаласьбы сильная зависимость скорости процесса от интенсивности выделенияводорода, но в действительности такая зависимость невелика. Кроме того,перемешивание растворов относительно слабо влияет на скорость осаждения, что также говорит о сильных кинетических ограничениях. Иногда усиление перемешивания даже уменьшает скорость процесса, что, видимо, связано с удалением промежуточных частиц с поверхности растущего осадка. Равновесный потенциал пары реакций H2PO3– + 2H+ + 2e⇄H2PO2 – + H2O или H2PO3– + 2H2O + 2e⇄H2PO2 – + 3ОH- зависит от рН раствора и составляет в кислой среде около –0,6 В, а в нейтральной около –1 В. Равновесный потенциал восстановления никеля близок к –0,25 В (независимо от рН). Поэтому выделение никеля, как чисто электрохимическое , так и химико-каталитическое, обычно имеет место при потенциалах от –0,35 В до –0,75 В, что фактически соответствует сравнительно невысокому перенапряжению анодного процесса (то есть окисления гипофосфита), особенно в кислой области. В процессе окисления восстановителей, протекающем сопряженно с восстановлением металлов, потенциал смещается в положительном направлении, в то время как потенциал выделяемых металлов – в отрицательном направлении от их равновесных потенциалов. В результате поверхность приобретает некоторый компромиссный потенциал, при котором одновременно происходит окисление восстановителя и выделение металла. Как показано на рис.1 стандартные плотности тока обмена обоих процессов окисления – восстановления(как никеля, так и гипофосфита-фосфита) довольно низки, то есть для каждого из них справедливо уравнение Тафеля lg i = lg i0 + αnFΔE/(2,3RT), где i0 – плотность тока обмена данного процесса, α – соответствующий электрохимический коэффициент переноса (0 < α < 1), n – число электронов, переносимых в единичном процессе (в данном случае n = 2), ΔE – отклонениереального потенциала от равновесного для данной реакции. 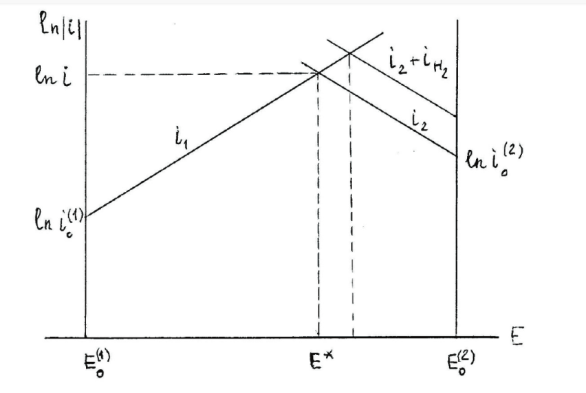 Рис. 1.Тафелевские кривые для окисления гипофосфита i1, для восстановления ионов никеля i2и выделения водорода i(H2), имеющие вид ln(i) = ln(io) + k(E – Eo) Из чисто геометрических соображений можно показать(без учета параллельного процесса выделения водорода), что в простейшем случае, когда α = 0,5(т. е. αn = 1), величина логарифма плотности тока при реальном смешанномпотенциале Е* (при котором равны токи окисления гипофосфита и восстановления никеля) составляет lg i = 0,5[lg i0(1) + lg i0(2)] + FΔE1-2/(4,6RT), где индексами 1 и 2 обозначены катодный и анодный процессы, i0(1) и i0(2) –плотности токов обмена анодного и катодного процессов, а ΔE1-2 – разностьмежду равновесными потенциалами реакцийвосстановления никеля и окисления гипофосфита, выраженная в вольтах. Таким образом, наблюдаемая скорость выделения металла больше всего зависит от этой разности потенциалов, а также от величин токовобмена, которые определяются каталитическими свойствами поверхности. Процесс выделения водорода приводит к некоторому смещению смешанного потенциала в отрицательном направлении. Еслискорость выделения водорода (в терминах плотности тока) равна скорости выделения металла, что довольно близко соответствуетдействительности, получается lg i (Ni) = 0,5lg [i0(1)i0(2)] + 6,85ΔE1-2 – 0,15 Механизм процесса электрокаталитического восстановления В ранних работах полагали, что металл непосредственно восстанавливается атомарным водородом, образуемым на каталитической поверхности измолекулы восстановителя, по такомумеханизму (Ni2+ + 2H = Ni + 2H+) катионы водорода должны были переходить в воду,а в действительности он выделяется в виде газа. В несколько упрощенном виде процесс, при котором восстановитель отдает электроны покрываемой каталитической поверхности (гетерогенныйгидролиз гипофосфита), записывается как H2PO2–+ HOН → H2PO3– + Н++ Hадс+ e; Этот процесс происходит в адсорбированном состоянии на каталитической поверхности. При простом растворении в воде гомогенный гидролиз гипофосфита идет очень медленно. Атом водорода в ионе H2PO2– , связанный непосредственно с атомом фосфора, замещается гидроксо-группой из молекулы воды, врезультате чего ион гипофосфита H2PO2–переходит в ион фосфита H2PO3–,отщепленный атом водорода адсорбируется на поверхности, а поверхностьприобретает электрон. Оставшийся ион водорода из воды присоединяет электрон вместе с адсорбированным атомом водорода, образуя газообразный водород: Н+ + Hадс + e = H2 Важно подчеркнуть, что ион металла получает электроны не прямо от молекулы восстановителя, а опосредованно – от всей поверхности электрода-катализатора. Другими словами, происходит обмен электронами через металл,который является резервуаром электронов. Именно это и дает возможностьизучать процессы путем их разделения на два – на катодный и анодный процессы.При этом скорость анодного окисления восстановителя очень сильно зависит от свойств каталитической поверхности металла, поэтомуи скорость всего процесса наиболее часто определяется этими свойствами. Кроме того, скорость электрохимического окисления восстановителя снижается при уменьшении рН (примерно вдвое при снижении рН на единицу)и очень мала при высокой кислотности (рН <3,0). Равновесная реакция гидролизагипофосфитакислой среде смещается в сторону образования гипофосфита, поэтому сильно кислые растворы на практике не применяются. Сопряженный процесс выделения никеля на каталитической поверхности: Ni2+ + 2e → Ni, причем этот процессвключает и образование каких-либо промежуточных частиц, то есть является на деле многостадийным. При рН >3скорость выделения никеля становится уже достаточно высокой.Одновременно с выделением водорода и металлического никеля на свежеобразованной каталитической поверхности происходит выделение элементарного фосфора, как часто предполагают, в результате реакции диспропорционирования: 4H2PO2- + H2O + Н+→ P + 3H2PO3 – + 2,5H2. В результате всех сопряженных процессов покрытие всегда содержит, кроме никеля, и элементарный фосфор, концентрациякоторого достигает 15 атомных процентов, а иногда и больше. Скоростьпроцесса образования фосфора несколько возрастает при увеличении кислотности, именно поэтому покрытия, полученные вкислой среде, содержат больше фосфора. Скорость выделения никеля, какуже было указано, в кислой среде, напротив, резко уменьшается. Таким образом, электроны, освобождаемые при гидролизе гипофосфита, идут на восстановление как никеля, так и водорода, и, кроме того, параллельно этим процессам выделяется фосфор. Поэтому суммарная реакция оказывается довольно сложной и в целом ее можно записать в общемвиде как xH2PO2- + (x–3)H2O +yNi2+ →(x–1) H2PO3- + (x– y–1,5) H2 + yNi + P + (2y–1)Н+(1) Отсюда видно, что происходит подкисление раствора (то есть образование новых ионов водорода Н+). При этом pH вблизи поверхности осаждаемого Ni-P сплава pHs может быть на 1–2 единицы ниже pHo в объеме раствора. В этом состоит существенное отличие от электрохимического осаждения Ni, когда происходит подщелачивание поверхностногослоя покрытия за счет восстановления водорода из воды. Подкисление приводит к уменьшению скорости процесса, а также влияет на состав и свойства покрытий; поэтому в растворы при многократном использовании необходимовводить буферирующие добавки. Полезным расходом гипофосфита считается его расход на восстановление никеля и фосфора. Например, при рН 4,3 и содержании фосфора в покрытии 16,9 ат.% на восстановление никеля израсходовано 75% гипофосфита, на выделение фосфора – 14 %, остальное – на гидролиз. Таким образом, коэффициент использования гипофосфита составил 89 %. В целом процесс для каждого из компонентов складывается из следующих стадий: диффузионный подвод реагента к поверхности, адсорбцияна поверхности, обмен с ней электронами, десорбция продукта реакции и обратная его диффузия в раствор (за исключением материала, осажденногона поверхности). Осадки, содержащие высокие концентрации фосфора, получаются нанокристаллическими или аморфными; они представляют собой твердые растворы замещения фосфора в никеле. Атомные радиусы никеля и фосфора близки (соответственно, 0,124 и 0,128 нм). , поэтому скорее всего это твердые растворы. Таким образом, можно сделать следующие выводы: 1 . Электрокаталитическое (химическое) выделение никеля является процессом, происходящим при смешанном потенциале, причем сопряженный анодный процесс – это окисление гипофосфита, а сопряженные катодныепроцессы – восстановление никеля и водорода. Одновременно имеет место диспропорционирование гипофосфита, сопровождающееся соосаждением элементарного фосфора. Параллельное выделение водорода аналогично процессу, происходящему при гидролизе гипофосфита. Процесс сопровождается подкислением раствора, образованием и накоплением в растворе малорастворимого фосфита. Толщина нернстовского диффузионного слоя, образованного вблизи поверхности, где образуется осадок, определяется в основном перемешиванием выделяющимся водородом и поэтому довольно мала. В этом слое имеет место перенос ионов никеля к поверхности и обратный перенос ионов водорода; эти два процесса практически компенсируются в смысле баланса заряда. Кроме того, перенос гипофосфита к электроду компенсируется переносом фосфита от электрода вглубь раствора. Градиенты потенциала, которые могут быть обусловлены концентрационными градиентами, практически отсутствуют, и вблизи рабочей поверхности электрического поля нет. Поэтому перенос вещества вблизи поверхности является чисто диффузионным, так как в отсутствие электрического поля миграции ионов не наблюдается. Основные компоненты растворов дляхимико-каталитического осаждения сплавов никель – фосфор, их концентрация и роль Соединения никеля Содержание солей никеля чаще всего соответствует 4–7 г/л по металлу (0,07–0,12 моль/л), причем наряду с хлоридом никеля (гексагидратом),который содержит 24,7 % никеля (в пересчете на массу металла), и сульфатом NiSO4·7H2O (20,9 % никеля) применяют также с и другие соли. При меньшем содержании солей никеля (и постоянной концентрации восстановителя) скорость осаждения покрытия пропорционально снижается; в то же время увеличение содержания никеля в техже условиях не приводит к ускорению процесса, а даже несколько замедляет его. Восстановитель – гипофосфит натрия Средняя величина концентрации гипофосфита натрия составляет20–30 г/л, или 0,2–0,3 моль/л. Дальнейшее увеличение содержания восстановителя, как и ионов никеля, не позволяет существенно повысить скорость процесса, да еще при этом отрицательно сказывается наустойчивости раствора (может начаться его самопроизвольное разложениес выделением порошка металла во всем объеме).Расход NaH2PO2·H2O составляет примерно 4–5 граммов на 1 грамм осажденного Ni-P сплава. Наилучшее мольное соотношение ионов гипофосфита к ионам никеля составляет 2,5–3,0; при меньшем содержании восстановителя снижается скорость процесса и количество фосфора в осадках, а при большемухудшаются их свойства. Ускорители, лиганды и буферирующие вещества Наряду с соединениями никеля и гипофосфитом натрия растворы содержат также некоторые дополнительные компоненты. Оптимальная кислотность растворов соответствует рН около 6, но почти всегда рекомендуют более высокую кислотность (рН 4,5–5,0), так какее легче регулировать и, кроме того, более кислые растворы стабильнее:они работают медленнее (замедляется основной процесс), но в них значительно выше растворимость фосфитов, меньше осаждаются гидроксиды и основные соли. Следует иметь в виду, что при подкислении не только снижается скорость процесса, но и возрастает содержание фосфора в покрытиях (поскольку выделение никеля замедляется при снижении рН, а при рН около3,0 прекращается). Влияние рН на содержание фосфора в покрытиях слабеевыражено в концентрированных по гипофосфиту растворах. Для поддержания кислотности (буферирования) и увеличения скорости осаждения применяют малоновую, янтарную, пропионовую, аминоуксусную, гликолевую или другие органические (как одноосновные, так и двухосновные) кислоты и их соли: ацетат натрия, цитрат аммония – то естьчаще всего те органические кислоты (соли), анионы которых образуют комплексные соединения с ионами никеля. Эти вещества обладают не только комплексообразующими, но и буферными свойствами (увеличивают буферную емкость растворов), они препятствуют быстрому снижению рН во время работы растворовв результате реакции (19). Они позволяют работать при более высоких рН, так как улучшают растворимость фосфита в этих условиях. Оптимальная концентрация этих веществсравнима с концентрацией гипофосфита. В результате комплексообразования они препятствуют выпадению осадка фосфита никеля (особенно аминокислоты), хотя и несколько снижают при этом скорость осаждения. Стабильность растворов для химического осаждения никель-фосфорныхпокрытий может быть нарушена из-за локального перегрева, повышеннойконцентрации восстановителя, а также присутствия следов постороннихэлементов в электролите, в результате чего опять-таки может начаться самопроизвольное разложение раствора. Именно поэтому в растворы и добавляют вещества, играющие роль стабилизаторов. Стабилизаторы – это тиомочевина, тиосульфат, сульфид (или хромат)свинца или висмута (2–3 мг/л), другие серосодержащие соединения и солинекоторых других металлов (сурьмы, олова, кадмия), триоксид молибдена(около 10 мг/л), уротропин, а также малеиновая кислота (или ее ангидрид).Они несколько повышают скорость образования покрытия (и сокращаютрасход гипофосфита), но в более высоких концентрациях резко снижаютскорость осаждения, ингибируя основные процессы – выделения никеляи водорода; эти вещества являются каталитическими ядами. Разложение растворов отчасти связано и с накоплением в растворе продукта окисления гипофосфита, а именно малорастворимого фосфита никеля (NiHPO3). Фосфит обычно начинает выпадать ориентировочно послеосаждения суммарно около 100 мкм покрытия (его растворимость в слабокислых растворах около 80 г/л). Выпадающие мелкие частицы, во-первых, попадают на поверхность покрываемых изделий и снижают качество покрытия, а во-вторых, на них начинает выделяться металлический никель,что и приводит к порче раствора. Стабилизаторы же адсорбируются на поверхности только что выпавших коллоидных частиц и, являясь каталитическими ядами, затрудняют образование там зародышей кристаллизацииникеля, тем самым не допуская самопроизвольного разложения раствора повсему объему. В последнее время по экологическим причинам от стабилизаторов, содержащих тяжелые металлы, стараются отказаться и вместо них используют пероксид водорода, тиомочевину или тиосульфат. Кроме того, добавляют смачиватели и блескообразователи – те же, что при электрохимическом осаждении, так как механизм их действия аналогичен. Происходит сглаживание микрошероховатостей. Этому процессу способствует образование на поверхности очень тонкой сорбционной пленки блескообразователя. Сильным блескообразующим действием обладают в разных растворах ацетиленовые спирты, ароматические альдегиды, красители разных типов, некоторые серосодержащие органические соединения. В целом растворы применяются главным образом слабокислые (рН 4–5), нейтральные (рН 6–7) и слабощелочные (рН от 8 до 9). Нейтральные и слабокислые растворы чаще используют при осаждении покрытий на магний, титан, некоторые неметаллы, а также при осаждении многокомпонентных сплавов. Интерес к щелочным растворам связан главным образом с тем, что их рабочая температура ниже по сравнению с кислыми, что позволяет наносить покрытия на материалы, которые не переносят высоких температур. Вследствие большей растворимости фосфита в щелочных растворах (более 300 г/л) рабочие ванные работают дольше, однако получаемые покрытия более пористы. Процесс составления растворов При составлении растворов для химического осаждения никеля все компоненты ванны растворяют отдельно, затем соединяют и корректируют рН кислотой (соляной или серной) или щелочью (содой, аммиаком). При этом раствор гипофосфита вводят лишь непосредственно перед началом осаждения в связи с опасностью разложения раствора. По мере работы растворов (как щелочных, так и кислых) скорость осаждения снижается в 1,5–2 раза уже после двух часов работы (рис. 2), а содержание фосфора в покрытиях возрастает. В связи с этим необходима корректировка состава ванн. 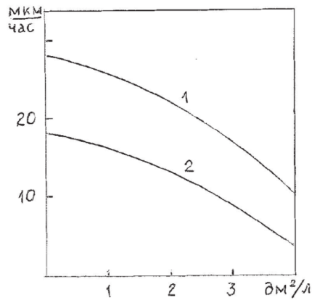 Рис. 2. Скорость осаждения в зависимости от плотности загрузки: 1 – в свежеприготовленном растворе, 2 – спустя 4 часа после начала работы Желательно работать по возможности с чистыми реактивами. Примеси в растворах, приводящие к различным неполадкам: ионы металлов: Pb, Cd , Zn, Cu, Fe, Al, Cr, анионы роданида и нитрата. В их присутствии образуются темные покрытия, снижается скорость осаждения, а иногда происходит разложение раствора. Ванны, температура, плотность загрузкиванн и причины низкого качества покрытий Покрытия получают в стальных эмалированных (либо футерованныхстойким материалом), стеклянных, полипропиленовых или фарфоровых ваннах, снабженных нагревателем и устройством для перемешивания раствора. Объем ванн – от лабораторных масштабов до тысяч литров. Температура процесса должна быть достаточно высокой; при низкихтемпературах скорость осаждения резко уменьшается. Рекомендуемая для подавляющего большинства процессов температура составляет 85–92 °С (при более высокой температуре возрастает вероятность разложения раствора). Скорость осаждения в рабочих условиях составляет 5–20 мкм/ч. Во время осаждения важно соблюдать плотность загрузки изделий, которая не должна превышать 3 дм2 поверхности на 1 л раствора. Скорость осаждения максимальна при плотности загрузки до 0,5 дм2/л; при возрастании плотности всего до 1,0 дм2/л она падает в 2–3 раза. При дальнейшем ее увеличении вплоть до 2,5–4,0 дм2/л скорость осаждения снижается незначительно (на 20–25 %), однако вновь возникаетопасность самопроизвольного разложения раствора. В среднем можно считать, что при оптимальных условиях осаждения увеличение плотности загрузки на 1 дм2/л приводит к снижению скорости осажденияна 8–10 мкм/час как в свежеприготовленных растворах, так и через несколько часов работы. Содержание фосфора в покрытиях в случае более высокой плотности загрузки несколько возрастает, особенно при длительной работе. Наряду с плотностью загрузки непрерывно контролировать рН ванны и температуру. Желательно постоянно фильтровать раствор через фильтр с порами диаметром 1–4 мкм. Причинами низкой скорости осаждения могут быть: низкие концентрации ионов никеля и гипофосфита, а также рН, пониженная температура и повышенная концентрация стабилизатора или наличие нежелательных примесей в растворе. Причинами получения неравномерного осадка являются: примеси посторонних металлов или органических веществ, отклонения от нормы концентраций компонентов, температуры и рН, неудовлетворительная подготовка поверхности. Если поверхность осадка грубо шероховатая или темная, то, вероятно, недостаточна фильтрация раствора или перемешивание, неудовлетворительна предварительная подготовка поверхности или, в раствор попали посторонние вещества . Причины низкой адгезии покрытия к основе – слишком долго работающий раствор, неудовлетворительная подготовка поверхности или загрязнение ванн обезжиривания и травления . Повышенная пористость наблюдается при наличии органических примесей или взвесей в растворе и при недостаточном перемешивании. Скорость осаждения, состав покрытий и их зависимость от различных факторов Основные факторы, влияющие на скорость осаждения и состав покрытий (т. е. содержание в них фосфора), это температура, рН и состав раствора, плотность загрузки, перемешивание и наличие загрязнений, а также длительность работы. От содержания никелевых соединений скорость осаждения слабо зависит в интервале 0,12–0,80 моль/л, однако при содержании менее 0,08 моль/л уменьшается, в то время как содержание фосфора в покрытиях возрастает, так как скорость его выделения слабо зависит от содержания никеля в растворе. Применение высоких концентраций никельсодержащих солей нецелесообразно; это не позволяет повысить скорость осаждения, ухудшая устойчивость растворов. От содержания гипофосфита скорость процесса зависит слабо в интервале концентрации 0,25–0,50 М, и поэтому применение высокой концентрации гипофосфита нецелесообразно. Но гораздо важнее соотношение никель/гипофосфит, которое оптимально должно составлять около 0,35–0,50 (рис. 3). 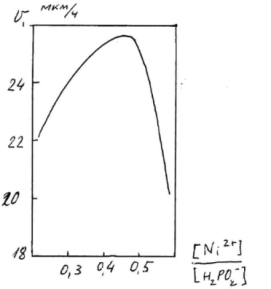 Рис. 3. Скорость осаждения как функция соотношения концентраций ионов никеля и гипофосфита Скорость осаждения существенно увеличивается от рН раствора (рис.4). Величина рН противоположным образом влияет на скорость осаждения покрытия и на концентрацию в нем фосфора (рис.5) .
Органические кислоты (молочная, янтарная, глутаровая, яблочная, гликолевая, лимонная, уксусная и другие) и их соли сильно ускоряют процесс. Оптимальная концентрация этих кислот может составлять от 5 до 40 г/л. Этому соответствуют мольные концентрации от 0,04 до 0,3 М, то есть они могут быть как вдвое ниже, так и вдвое выше посравнению с мольной концентрацией никеля. Подготовка поверхности Покрываемая поверхность, прежде всего, должна быть очищена от жировых и оксидных загрязнений, а также ей необходимо придать микрошероховатость, что способствует адгезии покрытия. Перед нанесением покрытия поверхность материала обезжиривают, декапируют (активируют) и очищают. Предварительная обработка, необходимая для осаждения никеля на непроводящую поверхность, состоит в том, чтобы сделать подложку гидрофильной, а затем активировать ее раствором соединения благородного металла, такого как хлорид палладия. В случае различных неметаллических поверхностей, в частности углеродных материалов, а также таких металлов, как медь, серебро, цинк, кадмий, свинец, олово, висмут, необходима сенсибилизация и активация поверхности. В других случаях нередко выполняется осаждение тонкого слоя никеля («страйк-никель») электрохимическим способом из кислого разбавленного раствора хлорида никеля (25 г/л шестиводного хлорида и 100 мл/л соляной кислоты плотностью 1,18 г/мл) при 5 А/дм2 в течение 2–3 минут. Применяют также предварительную металлизацию методом «вжигания» металлсодержащих паст. Сенсибилизация и активация Для того чтобы на поверхности началась кристаллизация металла, необходимо создать на ней каталитически активные центры, на которых в первый период никелирования возникнут кристаллические зародыши. Наиболее подходящим материалом для этого является палладий, а также платина, золото и серебро. Выделение палладия на поверхности производится обычно в две ступени. Необходимым начальным процессом, предшествующим нанесению сначала кластеров палладия, а затем и никель-фосфорного сплава на непроводящую (диэлектрическую) поверхность, является ее сенсибилизация. Этот процесс проводят при комнатной температуре в подкисленном соляной кислотой растворе хлорида олова. Раствор для сенсибилизации готовят путем растворения SnCl2·2H2O в разбавленной до нужной концентрации HCl. Предварительно подготовленную поверхность (очищенную, обезжиренную, высушенную и микрошероховатую) после выдержки в растворе сенсибилизации промывают в холодной воде, причем на ней (в основном в глубине микрошероховатостей) осаждаются частицы гидроксохлорида олова Sn(OH)1.5Cl0.5 .Вслед за этим выполняется промывка поверхности проточной водой или слабощелочным раствором, а затем активация поверхности, то есть выделение палладия. При погружении детали (изделия, платы и т. п.) в водныйраствор дихлорида палладия и соляной кислоты происходит выделение металлического палладия по реакции Pd2+ + Sn2+ = Pd + Sn4+, причем в течение 2–5 минут образуется весьма равномерный и очень тонкий слой палладиевого катализатора на поверхности. Растворы для активирования готовят путем растворения тонкоизмельченного хлорида палладия(0,75±0,25 г/л) в подготовленном горячем растворе соляной кислоты . Приблизительный расход палладия составляет 15–20 мг на 1 м2 покрытия. Это соответствует нескольким монослоям металла. Сенсибилизацию и активацию можно выполнить и в одну стадию, используя раствор 50 г/л хлорида олова (II), 1 г/л хлорида палладия, 200 мл/л соляной кислоты (плотность 1,18), хлорида калия 140 г/л. Корректирование растворов По мере работы электролитов в результате уменьшения рН и концентрации гипофосфита скорость осаждения уменьшается, а содержание фосфора в покрытиях возрастает. Поэтому растворы необходимо корректировать. Очевидно, что частота корректировки сильно зависит от плотности загрузки. Поскольку гипофосфит и соль никеля расходуются во время осаждения, необходимо периодически пополнять их содержание; в среднем на 1 г расхода никеля (по металлу) расходуется 4–5 г гипофосфита натрия. В силу того, что растворы в процессе эксплуатации подкисляются, это необходимо компенсировать добавлением щелочи. Стабилизаторы также расходуются, и их необходимо пополнять. Для корректировки составляют несколько раздельных достаточно концентрированных растворов: раствор никельсодержащейсоли, растворы щелочи, гипофосфита и стабилизатора. Добавляют их после частичного охлаждения рабочего электролита (примерно до 70 °С). В растворах происходит накопление в ионов фосфита, который сравнительно мало растворим в кислых растворах (около 50 г/л), и выпадение его в виде твердой фазы во всем растворе недопустимо, хотя стабилизаторы резко ослабляют вредное действие фосфита. В присутствии солей органических кислот, образующих комплексы, например, глицина и цитрата натрия, а также при повышении рН растворимость фосфита сильно увеличивается. Тем не менее, фосфит накапливается, и поэтому необходимо не только добавление расходуемых компонентов, но и периодическое удаление фосфита из раствора. По мере накопления фосфита увеличивается вязкость раствора, что несколько снижает скорость образования осадка (так как диффузионные ограничения все же имеют место). Вязкость (η) связана с концентрацией фосфита С как η ≈ 0.0425 С, где η выражено в МПа·с, а концентрация С в граммах на литр; уравнение справедливо при С от 50 до 120 г/л. Вообще опасность выпадения фосфита возникает после нанесения около 100 мкм покрытия и далее усиливается. Корректировать растворы удается только до определенного предела: примеси (фосфит и сульфат) неизбежно накапливаются до 100–150 г/л и более, а скорость осаждения постепенно снижается в 1,5–2 раза. Как правило, это соответствует 4–6 «оборотам» электролита, но некоторые растворы допускают работу до 10 «оборотов». Необходимо иметь ввиду, что по мере эксплуатации раствора не только замедляется процесс, но также возрастает концентрация фосфора в осадках, что особенно это выражено при низких рН и высокой плотности загрузки. Фосфиты можно удалить путем добавления к растворам хлорного железа, проведением электродиализа, или добавлением оксиэтилендифосфоновой или нитрилтриметилфосфоновой кислот, предотвращающих выпадение солевого осадка. При химико-каталитическом осаждении никель-фосфорных покрытий субзерна осадка имеют пластинчатую форму. По-видимому, первоначальные кластеры практически не содержат фосфора, но по мере их разрастания возникают периферийные области, обогащенные фосфором; при этом каталитическая активность поверхности снижается и их рост замедляется. Содержание фосфора, так и размер субзерен сильно зависит от величины рН раствора. По мере повышения кислотности от нейтральных растворов к кислым содержание фосфора в осадках резко возрастает (от 2–3 ат.% при рН 6,0–6,5 до 17–18 ат.% при рН 3,0–3,5, особенно резко при рН около 5,0) и одновременно уменьшается размер зерен (соответственно, от 10–20 нм до 2 нм и менее), то есть при рН от3 до 4 образуются аморфные осадки. Связана аморфизация не непосредственно с рН растворов, а с высоким содержанием фосфора в осадках; При понижении рН в осадке фосфора становится больше. При колебаниях рН покрытия приобретают слоистость, которая может быть удалена прогревом при 400–600 °С. Содержание фосфора в покрытиях несколько возрастает при увеличении концентрации гипофосфита в растворе и в менее концентрированных по никелю растворах. Скорость соосаждения фосфора слабо, но зависит от рН; скорость выделения никеля сильно зависит от рН. В результате состав сплава есть сложная функция температуры, рН и концентраций компонентов. Свойства никель-фосфорных покрытий. В технике используются никель-фосфорные покрытия с разным содержанием фосфора. Различают покрытия с низким содержанием фосфора ([P] = 1,5–8 ат.%), которые являются сравнительно крупнокристаллическими, а также средним ([P] = 8–15 ат.%) и высоким ([P] = 15–25 ат.%) содержанием фосфора – нанокристаллические, вплоть до аморфных. Такие покрытия различаются также и по свойствам, и по областям применения. В среднем границей перехода от мелкокристаллического состояния к аморфномуможно считать 7,5–8,0 % фосфора по массе. Осадки такого состава обладают максимальной прочностью и пластичностью. Аморфную фазу, формируемую при не слишком высоком содержании фосфора, более правильно считать нанокристаллической с большим количеством дефектов структур. Размер субзерен в кристаллических покрытиях 12–20 нм (в случае щелочных растворов несколько больше). При содержании фосфора более 10 % покрытия непосредственно после осаждения практически всегда аморфны. Формирующиеся покрытия химникеля в зависимости от содержания фосфора делят на три типа: - с низким содержанием P (1–3 масс.%); - средним (4–7 масс.%); - высоким (>7 масс.%). По стандарту IPC‑4552A они делятся на среднефосфористые (5–10 масс.%) и высокофосфористые (>10 масс.%). |